Powikłania neurologiczne po zastosowaniu cyklosporyny A u
Transkrypt
Powikłania neurologiczne po zastosowaniu cyklosporyny A u
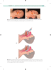
Powikłania neurologiczne po zastosowaniu cyklosporyny A u chłopca 337 Powikłania neurologiczne po zastosowaniu cyklosporyny A u chłopca z ogniskowym segmentalnym szkliwieniem kłębuszków – opis przypadku ELŻBIETA KUŹMA-MROCZKOWSKA, MAŁGORZATA PAŃCZYK-TOMASZEWSKA, MARIA ROSZKOWSKA-BLAIM Katedra i Klinika Pediatrii i Nefrologii Warszawskiego Uniwersytetu Medycznego, kierownik: prof. dr hab. med. M. Roszkowska-Blaim Powikłania neurologiczne po zastosowaniu cyklosporyny A u chłopca z ogniskowym segmentalnym szkliwieniem kłębuszków – opis przypadku Neurological symptoms in patient with focal segmental glomerulosclerosis treated with Cyclosporin A – case report Kuźma-Mroczkowska E., Pańczyk-Tomaszewska M., Roszkowska-Blaim M. Kuźma-Mroczkowska E., Pańczyk-Tomaszewska M., Roszkowska-Blaim M. Katedra i Klinika Pediatrii i Nefrologii Warszawskiego Uniwersytetu Medycznego Department of Pediatrics and Nephrology, Medical University of Warsaw Neurotoksyczność jest jednym z powikłań cyklosporyny A (CsA) stosowanej w leczeniu kłębuszkowych zapaleń nerek. Opis przypadku. U chłopca w wieku 9,7 lat rozpoznano zespół nerczycowy (zn) z krwinkomoczem. W biopsji nerki stwierdzono ogniskowe szkliwienie kłębuszków nerkowych. W leczeniu zastosowano prednizon doustnie (60mg/dobę) uzyskując remisję. Drugi nawrót białkomoczu nerczycowego leczono pulsami z metylprednisolonu (VI – 600 mg/puls) z dobrym efektem. Trzeci rzut zn, wtórnie sterydooporny, leczono cyklofosfamidem doustnie w dawce 140 mg/ kg/kurację – kuracja powikłana masywną grzybicą jamy ustnej oraz zapaleniem zatok. Następnie zastosowano cyklosporynę A uzyskując po 3 tygodniach ustąpienie białkomoczu. Po włączeniu leczenia CsA wystąpiły silne bóle głowy, oczodołów z nudnościami. Badanie neurologiczne bez odchyleń, w badaniu okulistycznym – niewielkie zmętnienie soczewek. Badanie EEG wykazało obecność zmian zlokalizowanych w tylnych okolicach mózgu, a tomografia komputerowa głowy niewielkie poszerzenie układu komorowego. W rezonansie magnetycznym (MRI-magnetic resonance imaging) głowy stwierdzono obecność ognisk o wzmożonym sygnale położonych podkorowo w istocie białej. Zakończono podawanie CsA po 4 miesiącach leczenia, prednison miesiąc później. Kontrolne badanie MRI głowy po 6 miesiącach wykazało utrzymywanie się zmian w istocie białej. Chłopiec pozostaje pod opieką poradni neurologicznej i nefrologicznej, nie ma nawrotów białkomoczu i objawów neurologicznych. Wniosek. U pacjentów leczonych CsA wystąpienie bólów głowy może sugerować neurotoksyczność leku. Cyclosporin A using in treatment glomerulonephritis can cause neurological side effects. Case report. Nephrotic syndrome (NS) with microscopic hematuria was recognized in a boy in the age of 9.7 years. In kidney biopsy focal and segmental glomerulosclerosis was found. Remission was obtained on oral prednisone (60mg/24hrs). Second relapse of NS was treated with methylprednisolone pulse (VI pulses – 600 mg/pulse) with a good effect. Third relapse of NS (secondary steroidoresistency) was treated with oral cyclophosphamide in a total dose 140 mg/kg/therapy – the treatment was complicated by a massive oral cavity mycosis and sinusitis. 3 weeks after starting cyclosporine A (CsA) proteinuria subsided. During CsA treatment severe headaches and pains in orbits with nausea appeared. In neurological examinations no abnormalities were found, in ophthalmological examination – slight opacification of the lens was found. EEG revealed lesions localised in a posterior cerebral parts, and CT of the head showed slight dilatation of ventricles. In MRI foci of signal intensification were found in subcortical white substance. CsA was stopped after 4 months of the treatment and prednisone was stopped a month later. Control MRI after 6 months revealed maintenance of the foci in white substance. The patient is under nephrological care, has no proteinuria and no neurological symptoms. Conclusion. In patients treated with CsA appearance of headaches may suggest medication neurotoxicity Słowa kluczowe: cyklosporyna, neurotoksyczność, zespół nerczycowy, dzieci Pol. Merk. Lek., 2009, XXVI, 154, 337 Key words: cyclosporine, neurotoxicity, nephrotic syndrome, children Pol. Merk. Lek., 2009, XXVI, 154, 337 Cyklosporyna A jest szeroko stosowana jako lek immunosupresyjny w transplantologii oraz w leczeniu kłębuszkowych zapaleń nerek. Jej skuteczność oraz korzyści wynikające z zastosowania są jednak ograniczone przez liczne działania niepożądane. Do najczęstszych działań ubocznych należą: nefrotoksyczność, hepatotoksyczność, nadciśnienie tętniczego, przerost dziąseł a także neurotoksyczność potęgowana przez hipomagnezemię [4]. Częstość występowania neurotoksyczności u dorosłych biorców narządów wynosi nawet do 40% [2]. U dzieci z zespołem nerczycowym opublikowano pojedyncze doniesienia [6, 9, 10]. Objawy neurologiczne dotyczą zarówno ośrodkowego jak i obwodowego układu nerwowego. Mogą występować w krótkim czasie po włączeniu leczenia cykosporyną, jak i w trakcie jej przewlekłego stosowania. W pierwszym przypadku przeważają objawy ogniskowe ze splątaniem, ślepotą korową, padaczką, natomiast w drugim – drżenia, ataksja z towarzyszącym niedowładem kończyn dolnych, splątaniem i depresją [8]. Wystąpienie w/w objawów ubocznych poprzedzają najczęściej bóle głowy oraz podwyższenie wartości ciśnienia tętniczego [3]. OPIS PRZYPADKU Chłopiec (K.R.) w wieku 9,7 lat został przyjęty do Kliniki Nefrologii z powodu narastającego od 3 miesięcy białkomoczu i pojawienia się krwinkomoczu (erytrocyty 8 w polu widzenia). Przy przyjęciu chłopiec był w stanie ogólnym średnim z uogólnionymi obrzękami. 338 Kuźma-Mroczkowska E., Pańczyk-Tomaszewska M., Roszkowska-Blaim M. W badaniach dodatkowych stwierdzono cechy pełnego rzutu zespołu nerczycowego: białkomocz 90 mg/kg/dobę, obniżone stężenie białka całkowitego – 5,2 g/dl, albumin – 2,4 g/dl, podwyższone stężenie cholesterolu – 304 mg/dl, fibrynogenu – 5,97 g/dl, obniżone stężenie immunoglobulin klasy G oraz krwinkomocz 15-20 w polu widzenia. Parametry funkcji nerek, wątroby oraz jonogram były prawidłowe, a wartości pozostałych klas immunoglobulin, składowych dopełniacza C3, C4 – w normie. Wyniki badań w kierunku chorób układowych były negatywne. W biopsji nerki rozpoznano wczesną fazę ogniskowego szkliwienia kłębuszków nerkowych. W leczeniu zastosowano doustnie prednizon w dawce 60 mg/dobę uzyskując ustąpienie białkomoczu po 13 dniach. Drugi nawrót białkomoczu nerczycowego wystąpił w trakcie infekcji górnych dróg oddechowych, w czasie stosowania prednizonu w dawce 60 mg co II dzień. Wobec utrzymywania się białkomoczu mimo ustąpienia cech infekcji i codziennego podawania prednizonu, zastosowano 6 pulsów z metylprednisolonu (600 mg/puls) uzyskując ustąpienie białkomoczu po 4 pulsie. Trzeci nawrót białkomoczu nerczycowego wystąpił w czasie stosowania prednizonu w dawce 60 mg co II dzień, bez cech infekcji. W leczeniu zastosowano cyklofosfamid w łącznej dawce 140 mg/kg/kurację. Kuracja była powikłana masywną grzybicą jamy ustnej i zapaleniem zatok. Wobec utrzymywania się białkomoczu do leczenia włączono cyklosporynę A uzyskując ustąpienie białkomoczu po 3 tygodniach. Dawkę leku modyfikowano pod kontrolą stężenia cyklosporyny we krwi, które wynosiło od 86,8 ng/ml do 214 ng/ml. Funkcja nerek, wątroby, stężenie kwasu moczowego, proteinogram były prawidłowe. Stwierdzano utrzymywanie się podwyższonego stężenia cholesterolu oraz triglicerydów. Niskie stężenie magnezu (1,8-1,5 mg/dl) było wskazaniem do suplementacji doustnej. Wobec stwierdzenia cech sterydotoksyczności niewielkiego zmętnienia soczewek w badaniu okulistycznym oraz nieco gorszego uwapnienia kręgosłupa w odcinku lędźwiowym w badaniu densytometrycznym (L2-L4 Z-score – 1,8) rozpoczęto redukcję dawek glikokortykosteroidów. Po 3 miesiącach leczenia cyklosporyną A pacjent zgłosił występowanie silnych bólów głowy, połączonych z bólem oczodołów i nudnościami (5 epizodów). Chłopiec był konsultowany neurologicznie oraz okulistycznie, poza zmętnieniem soczewek, nie stwierdzono odchyleń. W badanie EEG czynność podstawową stanowiły fale alfa 10-11 Hz o amplitudzie do 60 uV, pomiędzy którymi rejestrowały się pojedyncze rozsiane fale Theta o amplitudzie do 60 uV. Wobec obecności rozsianych zmian w okolicach tylnych mózgu w zapisie EEG oraz dyskretnego poszerzenia układu komorowego mózgu w tomografii komputerowej (TK) głowy wykonano rezonans magnetyczny głowy (MRI-magnetic resonans imaging). Badanie uwidoczniło obecność w istocie białej obu półkul mózgu nielicznych, położonych podkorowo ognisk o wzmożonym sygnale (ryc. 1). Leczenie cyklosporyną A zakończono po 4 miesiącach podejrzewając neurotoksyczność leku. Miesiąc później zakończono podawanie prednizonu. W wykonanym po 6 miesiącach kontrolnym badaniu MRI stwierdzono utrzymywanie się opisywanych poprzednio zmian w istocie białej (ryc. 2). Po zakończeniu leczenia cyklosporyną bóle głowy ustąpiły. Obecnie pacjent pozostaje pod opieką poradni nefrologicznej i neurologicznej. Nie ma nawrotów białkomoczu oraz bólów głowy. OMÓWIENIE Występowanie u naszego pacjenta bólów głowy mających czasowy związek ze stosowaniem cyklosporyny nasuwało podejrzenie neurotoksyczności leku. Mogła to być faza prodromalna poprzedzająca rozwinięcie ciężkiej postaci leukoencefalopatii lub izolowany objaw neurologiczny [7]. W diagnostyce wykorzystaliśmy badanie EEG, które wykluczyło Ryc. 1. MRI- projekcje T2 – zależne. Ogniska o wzmożonym sygnale podkorowo w istocie białej Fig. 1. T2-weighted MRI. Hyperintense focals subcortical in white matter Ryc. 2. Kontrolne badanie MRI po 6 miesiącach wykazało utrzymywanie się zmian w istocie białe Fig. 2. Control MRI after 6 months revealed maintenance of the foci in white matter obecność zmian napadowych. Badanie tomograficzne głowy, poza niewielkim poszerzeniem układu komorowego, było prawidłowe. Z literatury wiadomo, że tylko u niektórych pacjentów z objawami neurotoksyczności stwierdza się w TK obecność ognisk hipodensyjnych w istocie białej. Badaniem rekomendowanym do rozpoznawania zmian w istocie białej mózgu jest MRI. Jest to badanie czułe i pozwala na wykrycie zmian już w okresie prodromalnym [11]. W T2-zależnych projekcjach stwierdza się obecność rozsianych zmian w istocie białej z dominacją w obszarach ciemieniowo-potylicznych [5]. Wykonanie MRI u naszego pacjenta potwierdziło obecność ognisk o wzmożonym sygnale położonych podkorowo w okolicach ciemieniowo-potylicznych (ryc. 1) Za rozpoznaniem neurotoksyczności przemawiało także ustąpienie dolegliwości bólowych głowy po odstawieniu cyklosporyny. Utrzymywanie się zmian w istocie białej po 6 miesiącach u naszego pacjenta (ryc. 2) jest zgodne z doniesieniem Garcia-Escring Powikłania neurologiczne po zastosowaniu cyklosporyny A u chłopca M i wsp., który obserwował nieprawidłowy obraz w MRI przez 2 lata od odstawienia cyklosporyny i ustąpienia objawów neurologicznych [1]. WNIOSKI 1. Bóle głowy u pacjentów leczonych cyklosporyną mogą sugerować wystąpienie objawów neuroksycznych. 2. Objawy neurologiczne u tych pacjentów wymagają wykonania MRI głowy. PIŚMIENNICTWO 1. Garcia-Escring M., Martinez J., Fernandez-Ponsati J.I. wsp.: Severe central nervous system toxiticity after chronic treatment with cyclosporine. Clin. Neuropharmacol., 1994, 17, 298-302. 2. Gijtenbeek J.M., van den Bent M.J, Vecht C.J. Cyclosporine neurotoxicity: review. J. Neurol., 1999, 246, 339-346. 3. Kozłowska I., Różański J., Ciechanowski K. Neurotoksyczne powikłania cyklosporyny. Wiad. Lek., 2006, 59, 516-520. 4. Magnasco A., Rossi A., Catarsi P. i wsp.: Cyclosporin and organ specific toxicity: clinical aspects, pharmacogenetics and perspectives. Curr. Clin. Pharmacol., 2008, 3, 166-173. 339 5. Minn A.Y., Fisher P.G., Barnes P.D. i wsp.: A sydrome of irreversible leukoencephalopathy following pediatric allogenic bone marrow transplantation. Pediatr. Blood Cancer 2007, 48, 213-217. 6. Nakahara C., Hasegawa N., Izumi I. i wsp.: The use of cyclosporine in a boy with a priori episode of posteriori encephalopathy. Pediatr. Nephrol., 2005,20,657-661. 7. Reece D.E., Frei-Lahr D.A., Shephard J.D. Neurogic complications in allogenic bone marrow transplant patients receiving cyclosporine. Bone Marrow Transplant., 1991, 8, 393-401. 8. Schwartz R.B., Bravo S.M., Klufas R.A. i wsp.: Cyclosporine neurotoxicity and its relationship to hypertensive encephalophathy: CT and MR findings in 16 cases. AJR 1995, 165, 627-631. 9. Shimizu C., Kimura S, Yoshida Y. i wsp.: Acute leukoencephalophaty during cyclosporin A therapy in a patient with nephrotic syndrome. Pediatr. Nephrol., 1994,8,483-485. 10. Taque S., Peudenier S., Gie S. i wsp.: Central neurotoxicity of cyklosporine in two children with nephrotic syndrome. Pediatr. Nephrol., 2004, 19, 276280. 11. Trullemans F., Grignard F., Van Camp B. i wsp.: Clinical findings and magnetic resonance imaging in severe cyclosporine-related neurotoxicity after allogenic bone marrow transplantation. Eur. J. Haematol., 2001, 67, 94-99. Adres do korespondencji: Elżbieta Kuźma-Mroczkowska, Katedra i Klinika Pediatrii i Nefrologii Warszawskiego Uniwersytetu Medycznego, 00-576 Warszawa, ul. Marszałkowska 24, tel.: 022 629 34 23, faks: 022 621 98 63 XVIII Konferencja Naukowo-Szkoleniowa Polskiego Towarzystwa Nefrologicznego „Nerka – od biologii molekularnej do pacjenta” 4-6 czerwca 2009, Warszawa Przewodniczący Komitetu Naukowego: prof. Leszek Pączek Przewodniczący Komitetu Organizacyjnego: prof. Joanna Matuszkiewicz-Rowińska Konferencja będzie poprzedzona dwoma kursami: Kurs 1: „Genetyka i immunologia dla nefrologa” Kurs 2: „Dializa Otrzewnowa” Organizator: Polskie Towarzystwo Nefrologiczne oraz Katedra i Klinika Nefrologii, Dializoterapii i Chorób Wewnętrznych WUM Biuro Organizacyjne: 02-097 Warszawa, ul. Banacha 1a, tel.: (022) 599 26 58, faks: (022) 599 16 58 e-mail: [email protected]; www.nefroplatforma.pl