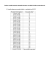Zeolity - Erem.com.pl
Transkrypt
Zeolity - Erem.com.pl
Uzdatnianie wody
Zeolity
W dniu dzisiejszym(06.12.2004) dopisano informacje o właściwościach fizykochemicznych naturalnego
klinoptylolitu ze złóż zeolitowych środkowego Mexyku, którego jesteśmy gen. dostawcą i
przedstawicielem na terenie Polski
{mosimage|m:m|a:42|t:1|ti:3;3|x:9|y:9|} Heulandyt i Klinoptylolit to dwa zeolity naturalne o
identycznej strukturze glinokrzemianowej, oznaczonej symbolem HEU.
Rozróżnia się je na podstawie stosunku Si/AI, zawartości kationów wymiennych oraz stabilności
termicznej.
Stosunek Si/AI zmienia się od ok. 2,7 dla heulandytu do ok. 5,3 dla klinoptylolitu.
Typowe kationy wymienne to wapń, sód i potas, rzadziej występują stront i bar. Klinoptylolit naturalny
charakteryzuje się wartością stosunku Si/AI wyższą od 4 oraz zawartością kationów (Na+K) >
(Ca+Ba+Sr).
Ponadto zeolit ten cechuje wysoka pojemność sorpcyjna i jonowymienna, selektywność jonowymienna,
właściwości sitowe na poziomie molekularnym, aktywność katalityczna rozmaitych form kationowych oraz
wysoka termostabilność strukturalna w temp. do700-750°C.
Występowanie klinoptylolitu w złożach naturalnych
Klinoptylolit jest zeolitem najbardziej rozpowszechnionym w przyrodzie i tworzącym największe zasoby.
Miejsca występowania: USA (Arizona, Nevada, Altoona, Washington, Oregon, Kalifornia), Syria, Austria,
Bułgaria, Kanada, Niemcy, Szwajcaria, Włochy, Japonia, Nowa Zelandia, Indie.
Natomiast w Polsce rozległe pokłady iłów zasobnych w klinoptylolit rozpoznano na Dolnym Śląsku i we
'wschodniej części fliszowych Karpat.
Minerały te nie są obecnie eksploatowane, chociaż zasoby zeolitonośnych łupków ilastych szacuje się na
kilkaset milionów ton, a klinoptylolit stanowi w nich główny składnik.
Najczęściej spotykane są następujące minerały towarzyszące: kalcyt, aragonit, tenardyt, kwarc, apofylit,
opal, piryt, halit, mordenit, heulandyt, chabazyt, analcym, erionit, ferieryt, harmotom, filipsyt i glina.
Praktyczne zastosowania klinoptylolitu
Klinoptylolit jest z powodzeniem stosowany w wielu gałęziach przemysłu, w rolnictwie i ochronie
środowiska.
Jego właściwości sorpcyjne i jonowymienne wykorzystuje się przy oczyszczaniu gazów i cieczy,
wzbogacaniu powietrza w tlen, dezaktywacji ścieków promieniotwórczych, uzdatnianiu wody do picia i do
celów technicznych, w tym do oczyszczania ścieków.
Ponadto wykorzystuje się go w przemyśle papierniczym, gumowym i tworzyw sztucznych.
Klinoptylolit łatwo adsorbuje amoniak oraz inne trujące gazy z powietrza i wody, dlatego jest szeroko
stosowany w filtrach, zarówno z powodów zdrowotnych, jak i w celu usunięcia przykrych zapachów.
Służy też jako dodatek do pasz dla zwierząt hodowlanych, gdyż adsorbuje toksyny wytwarzane przez
pleśnie i pasożyty.
Natomiast jego ewentualne wykorzystanie jako dodatek do żywności jest jeszcze na etapie badań.
Klinoptylolit krystalizuje w układzie jednoskośnym, grupa symetrii Cm.
{mosimage|m:m|a:42|t:1|ti:3;3|x:9|y:9|} Parametry komórki elementarnej:
a = 177 b = 17,9 c = 7,4 A B = 116°
Rodzaje kanałów:
•10-członowe o wielkości 7,6 na 3,0 A •biegnące wzdłuż płaszczyzny [001]
•8-członowe o wielkości 4,6 na 3,3 A •biegnące wzdłuż płaszczyzny [001]
Materiał badawczy
Badany minerał pochodzi ze złóż zeolitowych Centralnego Meksyku (Villa de Reyes, stan San Luis Potosi).
Jest to bardzo czysty klinoptylolit zawierający stosunkowo mało sodu, za to znaczną ilość potasu.
http://www.erem.com.pl
Kreator PDF
Utworzono 2-03-2017, 12:46
Uzdatnianie wody
Może to być szczególnie ważne w przypadku zastosowań w rolnictwie.
rys. Struktura klinoptylolitu widok wzdłuż płaszczyzny (001)
Skład chemiczny klinoptylolitu, zbadany przez ACTLABLS (Toronto, Kanada) przedstawiono w poniższej
tabeli:
Składnik
Zawartość
% wagowy
Zawartość
ilosć moli
izowany stosunek molowy
SiO2
66,470
1,1280
10,349
AloOo
10,93
0,1090
1,000
Fe2O3
1,463
0,0093
0,085
MnO
0,0245
0,0004
0,004
MgO
0,486
0,0123
0,113
CaO
1,949
0,0354
0,325
N2O
0,692
http://www.erem.com.pl
Kreator PDF
Utworzono 2-03-2017, 12:46
Uzdatnianie wody
0,0114
0,105
K2O
4,635
0,0501
0,459
TiO2
0,136
0,0017
0,016
P2O5
0,0245
0,0002
0,002
Straty prażenia (H2O)
12,66
0,614
5,633
Właściwości sorpcyjne
Powierzchnia właściwa wyznaczona metodą BET wynosi 34,5 m2/g.
Izotermy adsorpcji i desorpcji azotu wykazująhisterezę.
W minerale występują mezopory o przeważającej średnicy ok. 3,8 nm.
Całkowita objętość porów w minerale niemodyf ikowanym wynosi 0,135 cm3g.
Badania termograwimetryczne
Aparat Universal V2.3C TA Instruments, szybkość narostu temperatury 10 °C /min, atmosfera
beztlenowa (argon).
Ubytek masy do temperatury 1100 °C -12.66 %.
Próbka wstępnie prażona w temperaturze 100 °C wykazuje dwa efekty endotermiczne w temperaturach
90 i 171 °C.
Są one związane z wydzielaniem wody zaadsorbowanej fizycznie.
NMR
Widmo jąder krzemu dla klinoptylolitu składa się z 4 sygnałów o następujących przesunięciach
chemicznych względem TMS-u: -112,8; -106,7; -102,1 i -96,0 ppm.
Sygnały te są złożeniem ugrupowań 5\(nA\) położonych w nierównocennych pozycjach
krystalograficznych.
Jedynie sygnał przy -112,8 ppm odpowiada ugrupowaniom S'\(OA\).
W widmie jąder glinu pojawia się pojedynczy sygnał odpowiadający glinowi o koordynacji tetraedrycznej.
W preparacie nie występuje glin pozasieciowy. Sygnały oznaczone gwiazdkami to pasma boczne.
Poniższy artykuł pochodzący z EKOLOGIA I TECHNIKA, Vol. VIII, nr 2, 31 - 41 (2000) publikujemy za
zgodą autorów.
Zeolity naturalne i ich zastosowanie
w oczyszczaniu wody oraz ścieków
http://www.erem.com.pl
Kreator PDF
Utworzono 2-03-2017, 12:46
Uzdatnianie wody
Autorzy: A. M. Anielak, K. Piaskowski
Zakład Technologii Wody i Ścieków, Wydział Budownictwa i Inżynierii
Środowiska Politechnika Koszalińska, ul. Racławicka 15-17, 75-620 Koszalin 1. Wprowadzenie
5.3. Oczyszczanie wody z zanieczyszczeń ropopochodnych i olejowych
2. Charakterystyka
5.4. Oczyszczanie ścieków
3. Występowanie
5.5. Usuwanie metali ciężkich w technologii oczyszczania ścieków przemysłowych
4. Kierunki zastosowań zeolitów
5.6. Usuwanie metali ciężkich z osadów ściekowych
5. Oczyszczanie wody i ścieków
5.7. Dezaktywacja ścieków promieniotwórczych
5.1. Usuwanie azotu amonowego z wody i ścieków
6. Podsumowanie
5.2. Usuwanie THM-ów z wody
1. Wprowadzenie
Obserwowane obecnie wzrastające zanieczyszczenie już nie tylko wód powierzchniowych, ale również
podziemnych przy jednoczesnej wzrostowej tendencji zapotrzebowania na wodę o wysokich parametrach
jakościowych, zmusza do tworzenia coraz efektywniejszych
i ekologicznie bezpiecznych metod oczyszczania wody oraz ścieków.
Poszukiwania nowych rozwiązań są kierowane również w stronę wykorzystania naturalnych minerałów. W
tym kontekście duże możliwości stwarza współcześnie bardzo dynamicznie badany pod kątem
wszechstronnego zastosowania, a znany już prawie 250 lat niepozorny glinokrzemian. Odkryty przez
szwedzkiego uczonego Fryderyka Axela Cronstedta w kopalni miedzi w Lappmar wzbudził zaciekawienie
osobliwym zachowaniem. Podczas ogrzewania kryształów tego minerału jego powierzchnia pokrywa się
pęcherzykami podobnymi do tych, jakie powstają na powierzchni wrzącej wody. Tak właśnie zachowują
się zeolity, co w języku greckim oznacza „wrzące kamieniem.
Cechą zeolitów odkrytą przez Cronstedta jest obecność w ich składzie cząsteczek tzw. wody zeolitowej,
http://www.erem.com.pl
Kreator PDF
Utworzono 2-03-2017, 12:46
Uzdatnianie wody
która podczas ogrzewania usuwana jest z jego struktury pozostawiając jednak bez zmian otwartą
szkieletową konstrukcję kryształu. Taka budowa minerałów zapewnia unikatowe właściwości molekularnositowe, sorpcyjne i jonowymienne, które znalazły zastosowanie w wielu dziedzinach życia: w przemyśle,
rolnictwie, medycynie, ochronie środowiska naturalnego. Ich zastosowanie można określić
stwierdzeniem: „od składnika pasty do zębów aż do unieszkodliwiania odpadów nuklearnych".
Nieustannie prowadzone badania wykazują coraz to szersze możliwości wykorzystania tego minerału w
technologii wody i ścieków. Oprócz znanych dotychczas jego zastosowań, takich jak: usuwanie jonu
amonowego i pierwiastków radioaktywnych czy mechanicznej filtracji, podejmuje się próby wykorzystania
zeolitów do usuwania z wody związków chloroorganicznych (np. THM, MX), metali ciężkich wraz z ich
immobilizacją, zanieczyszczeń ropopochodnych. Jego skuteczność oraz bezpieczeństwo (ekologiczne)
użycia w procesach technologicznych skłaniają do bliższego zapoznania się z niezwykłymi cechami
zeolitów, będących w dużej mierze inspiracją wielu rozwiązań we współczesnych technologiach.
2. Charakterystyka
Od XVIII wieku, kiedy odkryto pierwszy z zeolitów stilbit, do chwili obecnej znaleziono już ponad 40
typów naturalnych zeolitów stanowiących najliczniejszą grupę wśród krzemianów. Te wyjątkowe
glinokrzemiany pierwiastków alkalicznych (Na, K, rzadziej Li) i pierwiastków ziem alkalicznych (Ca, Mg,
Bar, rzadziej Sr) różnią się między sobą budową strukturalną oraz właściwościami fizyczno-chemicznymi.
Najbardziej charakterystyczne parametry wybranych zeolitów przedstawiono w Tabeli 1. Tabela 1
Charakterystyka wybranych zeolitów.
[%]
Skład komórki elementarnej
Porowatość
Największe
prześwity kanalików
[nm]
Gęstość
[g/cm3]
Zdolność
wymienna
[mval/g]
Mordenit
Na8[(AIO2)8(SiO2)40]*24H2O
28
0,67-0,7
2,12-2,15
2,29
http://www.erem.com.pl
Kreator PDF
Utworzono 2-03-2017, 12:46
Uzdatnianie wody
Klinoptylolit
Na6[(AIO2)6(SiO2)30]*24H2O
34
0,47
2,16
2,54
Chabazyt
Ca2[(AIO2)4(SiO2)8]*13H2O
47
0,37-0,42
2,05-2,10
3,81
Analcym
Na16[(AIO2)16(SiO2)32]*16SH2O
18
0,26
2,24-2,29
4,54
Zeolity, podobnie jak najważniejsze minerały skałotwórcze - skalenie, charakteryzują się specyficzną
strukturą szkieletową (tektosilikatową), która zadecydowała o rosnącym zainteresowaniu nimi
przedstawicieli współczesnej nauki i techniki.
Podstawową jednostką trójwymiarowej krystalicznej struktury zeolitu są tetraedry (Si, Al)O4,
charakteryzujące się zmiennym stosunkiem krzemu do glinu i tworzące różne konfiguracje wielościenne jednostki oktaedryczne (tzw. kubooktaedry). W zeolitach naturalnych stosunek Si:Al w sieci krystalicznej,
tzw. moduł zeolitu kształtuje się w granicach 1¸6. Tetraedry AlO4 nie mogą się łączyć ze sobą wspólnym
atomem tlenu. Przy stosunku Si:Al=1 tetraedry AlO4 i SiO4 występują na przemian (Rysunek 1). {mosimage|m:m|a:42|t:1|ti:3;3|x:9|y:9|} Rys. 1. Schemat struktury zeolitu naturalnego.
Moduł zeolitu może znacznie się zmieniać w ramach jednego typu strukturalnego w zależności od składu
roztworów wyjściowych i warunków krystalizacji.
Centrum tetraedrów zajmują atomy krzemu lub glinu, naroża zaś zajmują cztery atomy tlenu. Każdy
atom tlenu jest wspólny dla dwóch różnych tetraedrów, dlatego też zbiór wszystkich czworościanów
krzemowo-tlenowych i glinowo-tlenowych łączy się ze sobą w powtarzające się nieskończenie w trzech
http://www.erem.com.pl
Kreator PDF
Utworzono 2-03-2017, 12:46
Uzdatnianie wody
kierunkach sekwencje, tworząc ciągłą sieć przestrzenną o strukturze szkieletowej. Takie powiązanie w
pierścieniowe zespoły ułożone w strukturze kryształu zeolitu powoduje powstanie wyjątkowo dużej ilości
wolnych przestrzeni, mających postać różnorodnych kanałów i komór. Komory przyjmują zwykle kształt
wielościanów (Rysunek 2), wewnątrz których istnieją obszerne wolne przestrzenie (pory). W zależności
od typu zeolitu, przyjmują one różne wielkości (typ A: 0,4 [nm], typ X: 0,9 [nm]).
{mosimage|m:m|a:42|t:1|ti:3;3|x:9|y:9|} Rys. 2. Przykłady schematów komór zeolitu typu A(a) i typu X(b).
Natomiast systemy kanałów powtarzają się w zależności od symetrii kryształu (Rysunek 3). Na przykład
równoległy system kanałów w analcymie (Rysunek 4a) składa się z 4 wiązek kanałów równoległych do
trójkrotnych osi sześcianu. System ten jest jednak jednowymiarowy, ponieważ kanały nie przecinają
się.
W kanałach i komorach szkieletu zeolitu obecne są kationy i cząsteczki wody. Najczęściej kationy są
otoczone zarówno cząsteczkami wody, jaki i atomami tlenu. Na przykład jon Mg znajduje się jedynie w
otoczeniu cząsteczek wody, natomiast jony K i Ba z reguły są otoczone atomami tlenu. W warunkach
standardowych cząsteczki wody wypełniają całą wolną objętość kanałów i komór struktury zeolitu w ilości
stechiometrycznej. Na podstawie objętości wody wydzielonej w czasie ogrzewania można obliczyć
objętość wolnych przestrzeni zeolitu. Przykładowo klinoptylolit posiada objętość porów równą 0,34
wody/cm3 kryształu. Woda oddawana jest z zeolitu bez zmiany jego struktury. {mosimage|m:m|a:42|t:1|ti:3;3|x:9|y:9|} Rys. 3. Systemy kanałów w: analcymie (a), mordenicie (b), fojazycie (c),
paulingicie (d), chabazycie (e) i gmelinicie (f).
{mosimage|m:m|a:42|t:1|ti:3;3|x:9|y:9|} Rys.4. Rozmieszczenie kationów wymiennych i cząsteczek
wody (puste kółka) w strukturze offretytu.
Podczas ochładzania minerału w środowisku wilgotny: woda zostaje ponownie wchłonięta. Ilość
cząsteczek wody zeolitowej przypadających na cząsteczkę minerału waha się w granicach od 1 (analcym,
zeolit sodowy) do 34 (zeolit strontowo-wapniowo-potasowo-so-dowy). Jednak obecność cząsteczek wody w strukturze zeolitów nie sprowadza się jedynie do wypełnienia
swobodnych przestrzeni. Jest ona szczególnym stabilizatorem porowatej struktury szkieletu
glinokrzemianowego. W kanałach wraz z cząsteczkami wody tkwią także tzw. wymienne kationy metali
jedno lub dwuwartościowych - głównie sodu, potasu, wapnia
i baru, które łatwo ulegają reakcji wymiany (Rysunek 4).
Rozmiary wolnych przestrzeni w strukturze zeolitu są tak znaczne, że kationy i cząsteczki wody mogą w
nich nie tylko tkwić, ale i swobodnie wędrować pod wpływem czynników fizycznych i chemicznych.
Przyjmuje się. że 1g zeolitu długość wszystkich porów osiąga wartość rzędu 200 milionów kilometrów.
Woda może być przez minerał oddawana i ponownie wchłaniana, zaś kationy mogą być wymieniane.
Zeolity w stanie wysuszonym wykazują własności sorpcyjne, katalityczne i molekularno-sitowe.
O tym, które kationy i cząsteczki mogą wejść do przestrzeni wewnątrz kryształu, a które muszą pozostać
na zewnątrz decyduje rozmiar oraz kształt kanałów wewnętrznych. W szkielecie zeolitu część jonów Si
(IV), w przeciwieństwie do kryształów kwarcu, zastąpiona jest przez Al (III). Powoduje to ujemny
ładunek szkieletu zeolitu, który równoważony jest przez wymienne kationy. Kationy te mogą być
wymieniane na drodze wymiany jonowej z dużej ilości związków chemicznych. Minerały o większej
zawartości glinu są zwykle hydrofilowe, natomiast zeolity, w których przeważa krzem są hydrofobowe.
Własności hydrofilowe są wynikiem niepełnej kompensacji nadmiaru ładunku ujemnego, występującego w
zeolitach glinowych (Rysunek 5.) http://www.erem.com.pl
Kreator PDF
Utworzono 2-03-2017, 12:46
Uzdatnianie wody
{mosimage|m:m|a:42|t:1|ti:3;3|x:9|y:9|} Rys. 5. Schemat struktury zeolitu naturalnego: a) hydrofobowego, b) hydrofilowego
Fizykochemiczne badania powierzchni niektórych zeolitów wykazały, że charakteryzuje je ujemny
potencjał elektrokinetyczny. Na przykład zeolit o nazwie handlowej Purolite MZ-10 przyjmuje w
określonych warunkach wartość potencjału równą -122 mV.
Skład chemiczny zeolitów (Tabela 2) determinuje ich zachowanie w określonych warunkach. W
środowisku alkalicznym minerały te ulegają rozkładowi-rozpadają się włókniste kryształy zeolitu, z
modernitu na przykład może powstać analcym. W środowisku kwaśnym natomiast można całkowicie
zdekationować, a następnie zdealuminować zeolit, w konsekwencji otrzymując tylko uwodniony
amorficzny szkielet krzemowy, zachowujący jednak wyjściowy kształt kryształu.
Tabela 2
Przeciętny skład chemiczny ukraińskiego klinoptylolitu z kopalni Sokirnica.
Składnik
Zawartość [%]
Składnik
Zawartość [%]
SiO2
69,43
Fe2O3
1,05
Al2O3
13,04
TiO2
0,18
K2O+Na2O
5,24
MnO
0.17
CaO
2,10
3. Występowanie
Powierzchniowe zaleganie zeolitów osadowych, a w związku z tym stosunkowo proste ich wydobycie,
stworzyły doskonałe warunki do szerszego ich wykorzystania. Produkcja światowa zeolitów naturalnych
na świecie w 1990 roku była szacowana na 800 tys. ton (bez byłego ZSRR). Zasoby globalne nie zostały
jeszcze ustalone, wiadomo jednak, że bardzo rozpowszechniane są na obszarach objętych wulkanizmem
http://www.erem.com.pl
Kreator PDF
Utworzono 2-03-2017, 12:46
Uzdatnianie wody
(Iran, Japonia, Nowa Zelandia i in.). Zeolity spotyka się w utworach magmowych, metamorficznych i osadowych. Głównymi grupami złóż są
osady jezior alkalicznych, solniska i gleby alkaliczne, osady dna oceanów, zzeolityzowane formacje
wulkaniczne. Minerały te występują na ogół w niewielkich ilościach, stanowią jednak istotne, a nawet
główne składniki zzeolityzowanych tufów, skał ilastych itp. Rodzaj i zawartość zeolitów w głównej mierze
zależą od struktury i składu skał otaczających, ich wieku geologicznego, składu wód porowych oraz
temperatury.
Eksploatacja złóż tego surowca prowadzona jest w wielu krajach Ameryki, jak np. Stany Zjednoczone z
największymi pokładami zeolitów pochodzenia sedymentacyjnego. W Europie krajem eksploatującym
pokłady zeolitów na wielką skalę są Węgry. Poza tym przemysł wydobywczy zeolitów jest dobrze
rozwinięty w Bułgarii, Słowacji i Jugosławii. Na Ukrainie we wsi Sokirnica wielkość zasobów zakarpackich
zeolitów ocenia się na powyżej 1 mld ton. W Polsce natomiast rozległe pokłady iłów zasobnych w
klinoptylolit rozpoznano na Dolnym Śląsku i we wschodniej części fiszowych Karpat. Obecnie minerały te
nie są jednak wydobywane, a prognostyczne zasoby zeolitonośnych łupków ilastych szacuje się na
kilkaset milionów ton, i to głównie klinoptylolitu. Stosunkowo ogromne i bogate w zeolity są osady denne
oceanów, lecz pokłady te są dla człowieka jak dotąd niedostępne.
Zasobne złoża zeolitów występujących w ilościach i czystości kwalifikującej je do rozpatrywania jako
bogactwo naturalne, tworzy jedynie 8 minerałów: klinon, tylolit, mordenit, ferrieryt, chabezyt, analcym,
lomontyt, z czego tylko dwa ostatnie nie znalazły jak dotąd zastosowania. Najbardziej
rozpowszechnionym i tworzącym największe zasoby jest zeolit wysokokrzemowy - klinoptylolit należący
do grupy z szeregu heulandytu, charakteryzujący się wartością stosunku Si:Al większą od 4 oraz
zawartością kationów (Na+K) > (Ca+Ba+Sr). Zeolit ten cechuje się szerszym zasobem specyficznych
cech fizykochemicznych, jak: wysoka pojemność sorpcyjna i jonowymienna, selektywność jonowymienna,
zdolność molekularno-sitowa, aktywność katalityczna (szczególnie w formie wodorowej) oraz
termostabilność strukturalna w temperaturach do 700-750°C, które to właściwości są wykorzystywane w
wielu dziedzinach współczesnej techniki.
4. Kierunki zastosowań zeolitów
Zeolity znalazły olbrzymie zastosowanie w różnych dziedzinach, takich jak: przemysł chemiczny,
mikroelektronika, optyka, medycyna, ochrona środowiska i rolnictwo. Największa liczba opisanych
dotychczas zastosowań zeolitów jest związana z przemysłem. W budownictwie zeolitonośne tufy można
wykorzystać do wyrobu cementu lub jako dodatek do klinkieru portlandzkiego. Zeolity szeroko stosuje się
jako nośniki katalizatorów w przemyśle petrochemicznym, przy prowadzeniu m.in. procesów krakingu,
alkilacji, uwodorowieniu w przeróbce ropy naftowej i gazu ziemnego. Właściwości adsorpcyjne zeolitów są
powszechnie wykorzystywane do osuszania i oczyszczania gazów, np. gazu ziemnego z H2S, metanu z
CO2, NxOY, H2S i pary wodnej, a także do rozdziału gazów i węglowodorów. Za pomocą klinoptylolitu
można odwadniać alkohole oraz mieszaniny olejowo-freonowe do urządzeń chłodniczych.
Zeolity okazały się „ekologicznie czyste” w porównaniu z zeolitami syntetycznymi,
dominującymi w sektorze środków piorących. Wynika to głównie z ich dużej zdolności do szybkiego,
preferencyjnego kompleksowania jonów wapnia w roztworach wodnych, w podwyższonej temperaturze.
Zeolity sztuczne, zastępujące w środkach piorących tripolifosforanowe wypełniacze zostały poddane
krytyce ze względu na zanieczyszczenia kanałów, rzek i plaż. Jednocześnie trwają intensywne badania
nad przydatnością zeolitów naturalnych dla środków piorących.
W przemyśle farmaceutycznym i drogeryjnym klinoptylolit jest dogodnym środkiem polerującym we
fluorkowych pastach do zębów oraz lekiem stabilizującym pracę układu trawiennego. Stosowany w
http://www.erem.com.pl
Kreator PDF
Utworzono 2-03-2017, 12:46
Uzdatnianie wody
postaci tamponu zawierającego zeolit służy do pochłaniania azotu, co pozwala zastąpić butle tlenowe w
szpitalach, a nawet podczas wspinaczek wysokogórskich. Szczególnym przypadkiem zastosowania
zeolitów jest osuszanie i oczyszczanie powietrza i tlenu w kabinach pojazdów kosmicznych i w maskach,
w których oddychają kosmonauci. Niestety, nie wszystkie zeolity można uznać za całkowicie bezpieczne
dla zdrowia użytkowników. Należy bowiem wykluczyć z bezpośredniego użycia zeolity o pokroju
włóknistym i o sztywnych włóknach, jak np. orionit, któremu ostatecznie przypisano działanie
rakotwórcze.
W rolnictwie zeolity znalazły bardzo różnorodne zastosowanie jako dodatki paszowe i nawozowe oraz
kondycjonery gleby. Składniki odżywcze dla roślin sadowią się w kanałach struktury zeolitów, co pozwala
na powolne przekazywanie ich do gleby i zapobiega zbyt szybkiemu ich wypłukiwaniu. Zdolność
jonowymienna i pojemność sorpcyjna naturalnych zeolitów może być również efektywnie wykorzystana
przy stosowaniu ich jako nośników pestycydów oraz herbicydów. Zeolity wykorzystano w zapobieganiu
eutrofizacji wód stawów rybnych, a także do aeracji kultur rybnych tlenem uzyskanym przy separacji z
powietrza.
Szczególnie istotną rolę glinokrzemiany odgrywają w ochronie środowiska. Okazały się one być skuteczne
w pochłanianiu tetraetylku ołowiu, trującego związku, składnika gazów spalinowych, klinoptylolit i
mordenit zastosowano do usuwania SO2 ze strumieni gazów i dymów z kominów fabrycznych poprzez
zeolitowe adsorbery-katalizatory.
W dziedzinie energii odnawialnej zeolity mogą służyć jako wymienniki ciepła. Uczestniczą one bowiem w
absorpcji i uwalnianiu ciepła z promieniowania słonecznego użytkowanego zarówno do regulacji
temperatury powietrza, jak i grzania wody. Dehydratacja zeolitu w dzień i jego rehydratacja w nocy,
połączone z efektem cieplnym, mogą wystarczyć do klimatyzacji domów. Obliczono, że 1 tona zeolitu
rozłożona na dachu o powierzchni 19,6 m2 zdolna jest klimatyzować 1 t powietrza. W jednej z
niemieckich szkół w 1996 roku zainstalowano 7 ton zeolitu, który będzie magazynował energię cieplną
pobieraną z miejscowej sieci grzewczej w godzinach pozaszczytowych i oddawał ją w godzinach szczytu.
Zmagazynowana w ten sposób energia powinna wystarczać do ogrzania budynku o powierzchni 1600 m2
przez około 13 godzin przy temperaturze zewnętrznej - 16°C.
Zeolity stosuje się w dezaktywacji odpadów nuklearnych i innych niebezpiecznych odpadów
przemysłowych. W mieszaninie z cementem portlandzkim są efektywnym czynnikiem stabilizującym,
natomiast w przypadku metali ciężkich - immobilizującym. Zeolitów używa się do gaszenia pożarów
chemicznych i usuwania substancji radioaktywnych, czego przykładem jest pożar elektrowni w
Czarnobylu, kiedy to z powietrza zrzucono ponad 200 tys. ton klinoptylolitowych tufów. Przez sorpcję
cezu i strontu w glebie mogły one zapobiec przedostawaniu się radionuklidów do wód gruntowych, a
następnie do rzek.
Rosnące zagrożenia zasobów hydrosfery budzą w ostatnich latach również nadzieje technologów na
szersze wykorzystanie właściwości glinokrzemianów do oczyszczania wody i ścieków.
5. Oczyszczanie wody i ścieków
Zeolity naturalne można wykorzystać na różnych etapach procesu oczyszczania wody i ścieków, takich
jak: koagulacja, flotacja, sedymentacja, adsorpcja, filtracja mechaniczna i wymiana jonowa.
Dotychczasowe zastosowanie sprowadza się do sorpcji jonów amonowych (ze ścieków komunalnych i
przemysłowych), usuwania pierwiastków promieniotwórczych (ze ścieków nuklearnych) oraz metali
http://www.erem.com.pl
Kreator PDF
Utworzono 2-03-2017, 12:46
Uzdatnianie wody
ciężkich (ze ścieków kopalnianych i ścieków pochodzących z hutnictwa żelaza i innych metali). Ostatnie
wyniki badań wskazują na możliwości użycia zeolitów także do usuwania związków chloroorganicznych
zanieczyszczeń olejowych oraz w procesie biologicznego oczyszczania ścieków.
W praktyce najczęściej stosowanym zeolitem w oczyszczaniu wody jest klinoptylolit, jako że posiada
doskonałe właściwości pod względem wymiany jonowej, adsorpcji, stabilności i trwałości struktury. Te
wyjątkowe cechy coraz częściej są dodatkowo modyfikowane, w zależności od przeznaczenia
klinoptylolitu. Najczęściej poddawany jest on procesom:
wstępnej wymiany jonowej,
obróbki termicznej,
działania kwasami, zasadami,
działania roztworami soli (NaCI, NH4CI).
Dzięki tym zabiegom naturalny zeolit zastosowany w procesach oczyszczania wody
i ścieków uzyskuje korzystną jednojonową formę (najczęściej sodową), selektywność względem
określonego rodzaju jonów, zwiększoną zdolność adsorpcyjną i pojemność jonowymienną oraz
wzmocnienie wytrzymałości mechanicznej, termicznej i kwasowej, stanowiących w dużej mierze o
skuteczności zastosowania minerału.
Uzdatnianie wody
Dosyć często podczas mechanicznego oczyszczania wody stosowany jest jako wypełnienie filtrów piasek
kwarcowy, charakteryzujący się małą porowatością. Może on być z powodzeniem zastąpiony przez zeolity
http://www.erem.com.pl
Kreator PDF
Utworzono 2-03-2017, 12:46
Uzdatnianie wody
naturalne. Badania nad zdolnością filtracyjną tufów zawierających klinoptylolit wykazały wiele zalet
takiego złoża, m.in.: większą porowatość, a w konsekwencji dłuższy cykl pracy, prawie 2-krotnie
mniejszy spadek ciśnienia hydrostatycznego w złożu, mniejsze zużycie wody do przemywania filtru,
możliwość oczyszczania wody o dużej zawartości zawiesin. Znaczna porowatość zeolitów zapewnia
usuwanie z wody cząstek koloidalnych pochodzenia mineralnego i organicznego. Połączenie chlorowania,
ozonowania i koagulacji kontaktowej z pracą filtrów z wypełnieniem klinoptylolitowym prowadzi do
efektywniejszego oczyszczania wody do picia, niż przy użyciu na przykład filtrów dwuwarstwowych.
Usuwane dodatkowo są fitoplankton oraz bakterie. Ponadto cykl pracy filtrów z zeolitem wydłuża się o 46 h w porównaniu z wypełnieniem filtrów piaskiem kwarcowym.
Przydatność klinoptylolitu zakarpackiego wykorzystano także przy odżelazianiu i odmanganianiu wody.
Proces ten prowadzony jest dwustopniowo. Na pierwszym filtrze z wypełnieniem naturalnym
klinoptylolitem usuwana jest zasadnicza część związków żelaza. Następny jest filtr również
klinoptylolitowy, ale dodatkowo modyfikowany MnO2, co w połączeniu z jonowymiennymi właściwościami
naturalnego zeolitu pozwoliło na równomierne rozłożenie warstwy utleniającego katalizatora w postaci
klastrów o wysokiej dyspersji. Na skalę przemysłową do odmanganiania stosowany jest tzw. piasek
zielony, zeolit o różnych nazwach handlowych np. Purolite MZ-20. Badania prowadzone przez Anielak i
Nowaka na Politechnice Koszalińskiej pokazały, że filtracja wody przez aktywne złoże zeolitu pozwala
uzyskać wysoką efektywność procesu odmanganiania, co skutecznie zastępuje wstępne utlenianie
manganu np. nadmanganianem potasu.
Zeolity zastosowano także do zmiękczania wody. Po wprowadzeniu do wody, o dużej zawartości jonów
wapnia i magnezu, glinokrzemianu w formie sodowej, następuje proces wymiany jonowej, przedstawiony
przez autorów na Rysunku 6.
{mosimage|m:m|a:42|t:1|ti:3;3|x:9|y:9|} Rys. 6. Schemat przebiegu reakcji wymiany jonowej w strukturze zeolitu.
Jony sodu przechodzą do roztworu, a ich miejsce w strukturze zeolitu zajmują jony wapnia. Wymiana jest
możliwa ze względu na prawie jednakowy promień jonowy Ca2+ (0,99 A) oraz Na+(0,97 A). Regenerację
zużytego zeolitu można wielokrotnie przeprowadzać roztworami soli sodowych. W praktyce jednakże
stosowanie zeolitów naturalnych do zmiękczania wody wydaje się mało zasadne z powodu:
-
niskiej pojemności jonowymiennej zeolitu,
-
utrudnionej regeneracji (szczególnie trudnych do usunięcia z wysyconej matrycy zeolitu
jonów wapnia i magnezu). To skłania technologów do stosowania raczej organicznych jonitów syntetycznych w procesie zmiękczania
wody.
http://www.erem.com.pl
Kreator PDF
Utworzono 2-03-2017, 12:46
Uzdatnianie wody
5.1. Usuwanie azotu amonowego z wody i ścieków
Jednym z poważnych zagrożeń środowiska wodnego są zanieczyszczenia związkami azotu. Z chwilą
pojawienia się jonów amonowych w wodzie zmniejsza się efektywność niektórych procesów uzdatniania
wody, np. odmanganiania czy chlorowania, natomiast w przypadku ścieków komunalnych, w których jon
amonowy jest stałym składnikiem, jego usunięcie jest obligowane przepisami w celu zapobiegania
zanieczyszczenia wód powierzchniowych - eutrofizacji.
Dotychczas stosowane metody usuwania azotu amonowego, oparte na procesach fizykochemicznych i
biologicznych nie zawsze dawały zadowalające rezultaty, stąd zainicjowane zostały szerokie badania nad
wykorzystaniem do tego celu zeolitów naturalnych głównie klinoptylolitu. Zeolit ten wykazał się wyższą
selektywnością w stosunku do jonów jednowartościowych. Opisuje to szereg wymienialności podany
przez Amesa:
Cs+ > Rb+ > K+ > NH4+ > Ba+2 > Sr+2 > Ca+2 > Fe+3 > AI+3 >Mg+2, z którego wynika, że
usuwanie jonów amonowych z wody może być bardziej skuteczne niż w przypadku syntetycznych
kationitów. Usuwanie jonów amonowych zeolitem zachodzi poprzez wymianę jonową; zgodnie z reakcją:
NH4+ + Na[zeolit] <=> NH4[zeolit] + Na+, albo wskutek adsorpcji w porach szkieletu
glinokrzemianowego.
W przypadku stosowania złóż zeolitowych istotna jest zawartość czystego klinoptylolitu w minerale,
determinująca jego przydatność w procesie usuwania jonów amonowych. Przykładowo słowacki
klinoptylolit wykazuje około 40% przewagę nad polskim (rzeszowskim). Decydujący wpływ na zdolność
jonowymienną klinoptylolitu wobec kationu NH4+ ma obecność innych jonów w roztworze. Szczególnie
dotyczy to jonów powodujących twardość wody. Jony wapnia i magnezu z dużą skutecznością
zatrzymywane przez zeolit mogą blokować do 80% jego dynamicznej pojemności wymiennej (DRI).
Proces ten jest wysoce skuteczny (zdolność jonowymienna zeolitów może zmaleć 2,5 razy) w przypadku,
gdy ich stężenie znacznie przewyższa stężenie jonów NH4+.
Klinoptylolit, ze względu na niską pojemność wymienną 3 mval/g wymaga częstych regeneracji oraz
dużej ilości roztworu regeneracyjnego (około 4-5 razy więcej niż w powszechnie stosowanych
kationitach), co przy dość krótkiej pracy złoża zeolitowego (około 150 objętości złoża) jest uciążliwe ze
względu na rosnące koszty eksploatacyjne oraz powstawanie większych ilości ścieków
poregeneracyjnych. Jest to główna przyczyna ograniczonego zastosowania zeolitu w większej skali.
Regenerację zeolitów po procesie usuwania jonów amonowych, prowadzić można metodami fizycznymi
(np. termiczną - desorpcja amoniaku w temp. 500- 600°C), chemicznymi ( układzie HCl-NaOH-NaCl) i
biologicznymi (długotrwałe napowietrzanie, nitryfikacja z wykorzystaniem osadu czynnego). Zużyty zeolit
można wykorzystać w rolnictwie jako pełnowartościowy materiał nawozowy.
Wpływ na proces usuwania jonów amonowych z wody ma również jej odczyn. Wzrost pH powoduje
wydzielanie nie ulegającego wymianie jonowej NH3, natomiast spadek pH, czyli wzrost stężenia jonów
wodorowych stwarza warunki konkurencji w stosunku do jonów NH4+. Stąd też optymalne warunki
odczynu do usuwania jonów amonowych na klinoptylolicie zawierają się w przedziale pH=5-8. Przy
średnim stężeniu 6 mg NH4+/L w wodzie zeolit wykazuje 98% sprawności, o ile wcześniej w procesach
filtracji na złożu piaskowym i z masą aktywną usunięte z wody zostaną jony żelaza i manganu .
Największe efekty uzyskuje się w przypadku zastosowania złoża zeolitowego o granulacji 0,3-0,75 mm,
co wynika z większego dostępu do centrów aktywnych zdolnych do wymiany jonowej.
http://www.erem.com.pl
Kreator PDF
Utworzono 2-03-2017, 12:46
Uzdatnianie wody
Klinoptylolit może z powodzeniem pełnić zarówno rolę wymiennika jonowego dla kationów NH4+ jak i
filtru biologicznie aktywnego. Próby przeprowadzone w układzie łączącym proces wymiany jonowej i
biologicznej nitryfikacji wykazały bezpośrednie i bardzo skuteczne usuwanie z wody, bez opóźnienia
wynikającego z rozwojem błony biologicznej na filtrze. Zeolit zawierający po wymianie jonowej kation
NH4+ stawał się dla bakterii źródłem azotu amonowego, co w efekcie tworzyło stabilny biofiltr w
warunkach wyczerpania się zdolności jonowymiennych złoża.
Ciekawą możliwością jest również zastosowanie dodatku w postaci silnie bądź słabo zasadowego anionitu,
który łącznie z klinoptylolitem jest w stanie jednocześnie usunąć obok jonów amonowych ponad 90%
fosforanów oraz skuteczniej eliminować związki organiczne. Odpadem takiego procesu są MgNH4PO4
oraz NH4NO3, możliwe do rolniczego wykorzystania w celu poprawy fizycznych i chemicznych właściwości
gleb gliniastych. W przypadku regeneracji zużytego zeolitu kwasem siarkowym otrzymywać można
siarczan amonu, nadający się do wykorzystania jako nawóz.
5.2. Usuwanie THM-ów z wody
Związki chloroorganiczne, THM-y powstające w wyniku reakcji chloru z naturalnie występującymi
składnikami organicznymi - kwasami humusowymi stwarzają coraz poważniejsze problemy w technologii
uzdatniania wody, wynikające również z ich toksycznego zagrożenia.
Prowadzone badania nad usuwaniem z wody chloroformu (najczęściej występującego przedstawiciela
trihalometanów), wykazały wysoką skuteczność klinoptylolitu. W przypadku rozcieńczonych roztworów
chloroformu (10-1000 mg CHCl3 /m3) w ciągu pierwszych 60 sekund prawie 75% chloroformu ulegała
adsorpcji na klinoptylolicie, natomiast w ciągu 30 minut nastąpiło praktycznie pełne usunięcie
(efektywność rzędu 97-99%). Jednocześnie nie wykazano wpływu pH na przebieg adsorpcji, co daje
możliwości prowadzenia procesu bez wstępnej neutralizacji oczyszczanej wody.
5.3. Oczyszczanie wody z zanieczyszczeń
ropopochodnych i olejowych
Szczególnie interesującym zastosowaniem zeolitów w ostatnich latach jest oczyszczanie wody z
zanieczyszczeń olejowych (związków ropopochodnych), olejów smołowych pochodzących z przerobu paliw
stałych, niektórych rozpuszczalników organicznych oraz olejów roślinnych i tłuszczy zwierzęcych.
Zanieczyszczenia te obecne są nie tylko w wodach powierzchniowych, ale również w wodach
podziemnych, co przy toksycznych ich właściwościach oraz trudnościach w ich usunięciu z wody zmusza
technologów do poszukiwań nowych metod oczyszczania.
Dobre właściwości sorpcyjne zeolitu, w stosunku do substancji ropopochodnych wykazały badania na
słowackim i rzeszowskim klinoptylolicie. Utrzymując złoże w stanie fluidyzacji (lekkiego uniesienia)
poprzez ukierunkowanie przepływu w kierunku z dołu do góry uzyskano skuteczność oczyszczania nawet
do 90%. Jednakże obok głównego procesu sorpcji, istnieje niebezpieczeństwo pojawienia się efektu
niepożądanego - koalescencji, która to wprawdzie może być przyczyną usunięcia około 30%
zanieczyszczeń olejowych, jednakże pojawia się możliwość skokowego pogorszenia efektów w wyniku
odrywania się warstewek oleju. Przeciwdziałaniem zaistnieniu tego zjawiska byłoby zastosowanie
przepływu w kierunku z góry na dół, jednakże taki układ z kolei spowodowałby zasklepianie oraz
zbrylenie wypełnienia, utrudniające głównie filtracyjną pracę złoża.
http://www.erem.com.pl
Kreator PDF
Utworzono 2-03-2017, 12:46
Uzdatnianie wody
Dużą efektywność usuwania zanieczyszczeń ropopochodnych uzyskano stosując łączenie procesów
adsorpcji z biodegradacją. Zastosowany w układzie przeciwprądowym fluidyzujący słowacki klinoptylolit
wykazywał powstanie błony biologicznej już po 60 [h] pracy złoża. Jego wydajność adsorpcyjna wyniosła
83 mg oleju na l lg zeolitu. Teoretyczną pojemność adsorpcyjną złoża przekroczono 8 razy, co świadczyło
o sprawnym działaniu biosorpcji. Układ łączący adsorpcję i biosorpcję nie tylko wydłużał czas pracy
kolumny, ale także złoże zeolitowe wykazało pozytywne właściwości jako podłoże dla rozwoju
mikroorganizmów rozkładających substancje ropopochodne. Najefektywniej usuwane były
zanieczyszczenia przy średnicy ziaren około 0,72 mm. Występują jednak ograniczenia stosowania tych
procesów związane z pH. Proces eliminacji zanieczyszczeń przebiega z największą efektywnością (88%)
przy pH=7, natomiast w przypadku alkalicznego odczynu (pH=9) wydajność adsorpcji i biosorpcji może
spaść nawet do 55%. Związane jest to ze zwiększoną zwilżalnością ziaren sorbenta przez fazę wodną,
wskutek czego następuje cofanie się filmu olejowego i odrywanie kropel oleju od ziaren klinoptylolitu.
Otwarta sprawa pozostaje w przypadku ewentualnej regeneracji zużytego złoża lub jego bezpiecznej
ekologicznie utylizacji.
5.4. Oczyszczanie ścieków
W ostatnich latach zeolity naturalne zaczęto stosować w procesie oczyszczania ścieków. Przeprowadzone
testy na oczyszczalniach w Niemczech i na Węgrzech wykazują pozytywne rezultaty, choć ciągle są
prowadzone intensywne badania nad optymalizacją stosowania zeolitów. Zaleca się stosować czysty zeolit
(Zeotrade - Węgry), odpowiednio przygotowany technologicznie w trakcie obróbki pod kątem jego
przeznaczenia (np. aktywowanie siarczanem żelaza - do efektywnego usuwania fosforanów) i
przemielony do postaci sypkiego proszku o średnicy ziaren około 125 µm. Badania wykonane przez
Centralny Instytut Badawczy w Budapeszcie potwierdziły duże możliwości zastosowania zeolitu zeoflocc
(55% klinoptylolitu) do biologicznego oczyszczana ścieków. Zastosowanie sypkiego zeolitu eliminuje
zanieczyszczenia koloidalne oraz organiczne, usuwa związki amonowe, sprzyja zmniejszeniu parametrów
BZT5 oraz ChZT nawet do ok. 30%, zanieczyszczeń koloidalnych i lepszemu osadzaniu zawiesiny oraz
stymulacji ich biologicznej aktywności. Rysunek 7 wskazuje możliwe miejsca dozowania zeolitu w
układzie oczyszczania ścieków. Najczęściej realizuje się je w punkcie 1 i 2 (Rysunek 7) na dopływie do
reaktora biologicznego. Badania prowadzone na Politechnice Koszalińskiej wykazały skuteczność
dozowania zeolitów do komory osadu czynnego w procesie oczyszczania ścieków komunalnych. Jednak
problem ten wymaga jeszcze wielu badań laboratoryjnych i przemysłowych, które ustalą optymalne
zastosowanie tego minerału.
{mosimage|m:m|a:42|t:1|ti:3;3|x:9|y:9|} Rys. 7. Typowe punkty dozowania zawiesiny zeolitu.
Zastosowanie zeolitu w oczyszczaniu ścieków pozwala również na racjonalne i ekologiczne
zagospodarowanie osadu, o czym świadczy opracowana przez Instytut Nawozów Sztucznych w Puławach
technologia produkcji granulowanego nawozu mineralno-organicznego na bazie osadów komunalnych
oczyszczalni ścieków.
Oczyszczone biologicznie ścieki można również kierować na filtr z wypełnieniem klinoptylolitowym, jako
końcowy etap procesu, uzyskując parametry odcieku odpowiadające wymaganiom odbiorników wodnych
naturalnych, a także wód przemysłowych. Badania prowadzone na instalacji filtracyjnej ze złożem zeolitu
naturalnego z Buriacji, o zawartości 50-60 klinoptylolitu, wykazały zmniejszenie stężenia; jonów
amonowych od kilkunastu do 0.5Mg/L, natomiast jonów potasu od 110 do 1-2 mg/L. Wysokie efekty
usunięcia tych kationów mogą być wykorzystane podczas oczyszczania ścieków pochodzących z fabryk
http://www.erem.com.pl
Kreator PDF
Utworzono 2-03-2017, 12:46
Uzdatnianie wody
nawozów sztucznych, czy hodowli trzody chlewnej, z równoczesną utylizacją powstałych odpadów. Po
oczyszczeniu biologicznym ścieki skierowane na filtr klinoptylolitowy o zawartości 50-90% zeolitu
uzyskały obniżenie stężenia jonów K i NH4 do 6-10 mg/L. W pracach nad oczyszczaniem ścieków zawierających metale alkaliczne i ziem alkalicznych, z
wykorzystaniem klinoptylolitu szywyrtujskiego (Syberia wschodnia) wykazano, że kationy K+, Na+ i
Mg2+ usuwane są w procesie sorpcji, natomiast Ca2+ - podczas wymiany jonowej. Jordańskie tufy
zeolitowe zawierające głównie filipsyt, fojazyt i chabazyt nadają się do usuwania jonów amonowych oraz
fosforanowych ze ścieków znajdujących się w stawach osadowych.
Na podkreślenie zasługuje fakt, że zastosowanie zeolitów przyczyniać się może do ochrony środowiska
naturalnego poprzez użycie minerału naturalnego, będącego alternatywą dla aktualnie stosowanych
środków chemicznych. Zeolit pozwala na zmniejszenie ładunku azotu i fosforu w oczyszczonych ściekach
oraz zagospodarowanie osadu ściekowego jako nawozu dla rolnictwa.
5. 5. Usuwanie metali ciężkich w technologii oczyszczania
ścieków przemysłowych
Do usuwania jonów metali ciężkich ze ścieków najczęściej wykorzystuje się metody adsorpcyjne i
wymianę jonową. Ze względu na właściwości fizycznochemiczne, mechaniczne, hydrodynamiczne oraz
wyraźną selektywność w stosunku do jonów metali ciężkich, materiałami używanymi do realizacji tych
procesów są naturalne zeolity, szczególnie klinoptylolit i mordenit. Badania wykazały, że proces usuwania
metali na zeolitach ma charakter wymienno-sorpcyjny, w którym dominującym procesem jest jednak
wymiana jonowa.
Jonowymienne właściwości zeolitów naturalnych predysponują do usuwania metali ciężkich ze ścieków
kopalnianych i metalurgicznych. Można je więc wykorzystać nie tylko do oczyszczania wody i ścieków z
tych metali, ale również do ich odzyskiwania. Klinoptylolit, zwłaszcza w formie sodowej, nadaje się do
skutecznego usuwania dwuwartościowych kationów metali: Cu, Cd, Zn, Pb, Co, Mn, Ni i in., szczególnie w
końcowym etapie trójstopniowej oczyszczalni ścieków przemysłowych. W badaniach nad usuwaniem
metali ciężkich za pomocą, klinoptylolitu stwierdzono, że pojemność jonowymienna zeolitu może się
zmieniać od 1,6 mval/g dla ołowiu do 0 mval/g dla rtęci. Oznaczona doświadczalnie kolejność
selektywności układa się następujące:
Pb2+ > Cd2+ > Cu2+ > Co2+ > Cr3+ > Zn2+ > Ni2+ > Hg2+. Klinoptylolity, słowacki i ukraiński, użyte do usuwania miedzi i kadmu z roztworów wodnych wykazywały
większą selektywność w stosunku do jonów kadmu niż do jonów miedzi, potwierdzając przedstawiony
szereg. Wykorzystanie klinoptylolitu do usuwania cynku z kwaśnych wód kopalnianych w Montanie
dowiodło, iż mimo zajmowania przez metal dalekiego miejsca w szeregu selektywności, zeolit pozwolił
obniżyć zawartość Zn prawie o 100%.
W przypadku oczyszczania ścieków galwanicznych, zawierających Cr(III) skutecznym sorbentem okazał
się naturalny zakarpacki klinoptylolit modyfikowany roztworem NH4CI. Procesowi adsorpcji ulegał tylko
Cr(III). W przypadku jonu Cr(VI) nie wykazano efektów usunięcia. Oszacowano, że 1 kg naturalnego
klinoptylolitu może w ciągu 2 godzin kontaktu usunąć jony Hg(II), Ni(II) i Cr(III) ze ścieków o objętości
100-200 litrów i stężeniu kationów metali 0,5-10 g/m3. W przypadku wyższych stężeń należy
przeprowadzać wstępne chemiczne podczyszczanie ścieków (np. poprzez wytrącanie osadów metali)
obniżające zawartość jonów metali, natomiast zeolity wykorzystać do głębszego doczyszczenia ścieków.
Istotnym elementem w skuteczności usuwania metali z roztworów za pomocą zeolitu jest czas kontaktu z
roztworem regenerującym w celu uzyskania formy jednojonowej. Korzystnie jest zeolit poddawać kilka
krotnemu procesowi wymiany i regeneracji, aby uniknąć sytuacji, kiedy nie wszystkie jony ruchliwe
http://www.erem.com.pl
Kreator PDF
Utworzono 2-03-2017, 12:46
Uzdatnianie wody
zostają wymienione na jon sodowy. Selektywność minerału jest w części determinowana przez obecne w
matrycy zeolitu jony wapnia i potasu, stąd należy je maksymalnie usunąć. Jednym z czynników
limitujących wiązanie metali jest pH, ponieważ klinoptylolit w trakcie wymiany jonowej usuwa formy
dwuwartościowe np. Cd i Cu, niepożądane jest aby w roztworze były obecne konkurencyjne jony
wodorowe.
Po zakończonym procesie sorpcji zeolity można poddać procesowi cementacji albo zeszklenia i
ostatecznie zamknięcia w betonie. Badania wykazały dużą stabilność metali w matrycy zeolitu w
połączeniu z wapnem i gipsem, co wskazuje, że odpad ten potencjalnie możliwy jest do wykorzystania
jako materiał budowlany. Istnieje także możliwość odzyskiwania metali ciężkich metodami
hydrometalurgicznymi, przez elucję złoża roztworem NaCl o wysokim pH, z elektrolitycznym
wydzielaniem metalu.
5.6. Usuwanie metali ciężkich z osadów ściekowych
Oczyszczalnie ścieków komunalnych i przemysłowych dostarczają dużych ilości osadów ściekowych o
zróżnicowanym składzie chemicznym. Mogą one zawierać stosunkowo dużo składników biogennych:
N,P,K,Ca,Mg, które mogłyby być wykorzystane w rolnictwie, ogrodnictwie czy leśnictwie. Podstawowym
jednak ograniczeniem ich wykorzystania jest obecność w nich metali ciężkich (m.in. Pb, Cu, Ni, Cr, Cd,
Hg). Problem ten może zostać wyeliminowany poprzez zastosowanie zeolitów jako selektywnych
sorbentów metali ciężkich z osadów.
Przeprowadzone przez SGGW w Warszawie badania modelowe na złożach kaukaskich, zawierających
około 20% zeolitów z grupy klinoptylolitu wykazały, że w stosunkowo krótkim czasie można oczyścić
osady ściekowe z metali ciężkich poprzez wiązanie i unieruchomianie ich w strukturze minerału. Zeolity
złóż naturalnych wiążą metale ciężkie (ilościowo) z osadów ściekowych według następującej kolejności:
Cu > Pb > Ni. W przypadku form łatworozpuszczalnych, dla stosunku wagowego osadu do zeolitu 1:1
uzyskano usunięcie od 40% dla Cu i Ni do 100% dla Pb. Nie zostało jednak zbadane, jak długo zeolity
mogą utrzymywać wbudowane w swoją strukturę metale ciężkie. W warunkach silnego zakwaszenia gleb
zeolity mogą stać się jednak mało stabilne i ulegać rozpadowi, a w związku z tym metale ciężkie z
powrotem przejdą w formę rozpuszczalną.
5. 7. Dezaktywacja ścieków promieniotwórczych
Jedną z podstawowych metod oczyszczania ścieków promieniotwórczych jest metoda dezaktywacji
adsorpcyjnej. W ostatnich latach pojawiło się zainteresowanie możliwością zastosowania minerałów
zeolityzowanych, w szczególności tufów zawierających klinoptylolit, które wykazują dobrą selektywność
jonowymienną do 137Cs oraz 90Sr i innych pierwiastków promieniotwórczych, w usuwaniu ich ze
ścieków. Pojemność klinoptylolitu względem cezu jest 30-krotnie większa niż w przypadku żywic
jonowymiennych, a ponadto naturalny zeolit jest również bardziej odporny na degradację radiacyjną.
Przy oczyszczaniu ścieków nuklearnych izotopy promieniotwórcze cezu, strontu czy plutonu są sorbowane
w kolumnach wypełnionych zeolitem z wydajnością dochodzącą do 100%. W elektrowni atomowej w
Hanford (stan Waszyngton) za pomocą układu z 8,4 m3 klinoptylolitowego sorbentu usuwano izotop
137Cs z ponad 100 mln litrów ścieków radioaktywnych dziennie. Proces sorpcji przebiegać musi w
środowisku obojętnym lub zasadowym, aby wyeliminować konkurencję kationów wodoru w stosunku do
jonów cezu (strontu).
http://www.erem.com.pl
Kreator PDF
Utworzono 2-03-2017, 12:46
Uzdatnianie wody
Ponieważ krzemiany reagują szybko w układach cementowych i szklanych immobilizując radioaktywne
składniki, zużyte zeolity poddaje się cementacji lub zeszkleniu w piecu indukcyjnym i po zamknięciu w
obudowie z betonu umieszcza się w bezpiecznych składowiskach.
6. Podsumowanie
Przedstawiony szeroki wachlarz zastosowań naturalnego minerału - zeolitu, skłania nas do określenia
go mianem surowca XXI wieku. Unikalna struktura szkieletowa, charakterystyczna dla skaleni nadała mu
właściwości, których wykorzystanie w praktyce lawinowo rośnie w ostatnich latach. Największe
zainteresowanie i zastosowanie przejawia . klinoptylolit, który obok szerokiego występowania w
przyrodzie duże spektrum specyficznych cech fizykochemicznych: adsorpcyjne, jonowymienne, sitowomolekularne. W praktycznym użyciu są one wzmacniane dodatkowo przez wstępną obróbkę pod kątem
indywidualnego zastosowania. Obok przemysłu, rolnictwa, szeroko pojętej ochrony środowiska, zeolity
odnalazły istotne zastosowanie w oczyszczaniu wody oraz ścieków. Klinoptylolit okazał się skutecznym
materiałem usuwającym z roztworów wodnych m.in.:
-
azot amonowy, -
metale ciężkie i alkaliczne, -
pierwiastki promieniotwórcze, -
twardość wody, -
związki chloroorganiczne (THM), -
zanieczyszczenia olejowe i ropopochodne, oraz pełniącym rolę efektywnych filtrów mechanicznych lub biologicznie aktywnych, gdyż stanowi on
doskonałe podłoże dla rozwoju mikroorganizmów.
Zużyty zeolit podczas usuwania NH4-N lub oczyszczania ścieków może zostać wykorzystany w
rolnictwie jako materiał o wartościowych właściwościach nawozotwórczych lub też jako element
budowlany po związaniu w matrycy z cementem lub gipsem, gwarantując immobilizację zawartych w nim
metali ciężkich.
Własności zeolitów do dziś nie zostały jeszcze w pełni wykorzystane, a ze względu na dostępność i cenę
stanowią one tani substrat do wykorzystania w różnych etapach oczyszczania wody i ścieków.
Streszczenie
http://www.erem.com.pl
Kreator PDF
Utworzono 2-03-2017, 12:46
Uzdatnianie wody
Rosnące wymagania w zakresie uzdatniania i ochrony wód przed zanieczyszczeniami wymuszają
poszukiwanie coraz bardziej efektywnych, ale jednocześnie tanich i bezpiecznych ekologicznie rozwiązań.
W związku z tym, w ostatnich latach coraz większe zainteresowanie budzą naturalne minerały o
właściwościach molekularno-sitowych, sorpcyjnych i jonowymiennych - jednym słowem zeolity. Dzięki
dostępności, niskiej cenie oraz właściwościom, wynikającym ze szkieletowej struktury, ich możliwości
zastosowania pozwalają nazwać go minerałem XXI wieku. Zeolity wykorzystywane są w technologiach
szeroko pojętej ochrony środowiska: od oczyszczania wody i ścieków (usuwanie jonów amonowych,
pierwiastków promieniotwórczych, metali ciężkich, zanieczyszczeń ropopochodnych) do adsorpcji wody i
gazów, w rolnictwie oraz różnych gałęziach przemysłu. Na podstawie przeglądu literatury przedstawiono
wielostronne przeznaczenie zeolitów we współczesnej inżynierii środowiska, a szczególnie w technologii
oczyszczania wody i ścieków. Składnik
Zawartość
% wagowy
Zawartość
ilosć moli
izowany stosunek molowy
SiO2
66,470
1,1280
10,349
AloOo
10,93
0,1090
1,000
Fe2O3
1,463
0,0093
0,085
MnO
0,0245
0,0004
0,004
MgO
0,486
0,0123
0,113
CaO
1,949
0,0354
0,325
http://www.erem.com.pl
Kreator PDF
Utworzono 2-03-2017, 12:46
Uzdatnianie wody
N2O
0,692
0,0114
0,105
K2O
4,635
0,0501
0,459
TiO2
0,136
0,0017
0,016
P2O5
0,0245
0,0002
0,002
Straty prażenia (H2O)
12,66
0,614
5,633
Na podstawie przeprowadzonej analizy chemicznej wyznaczono skład komórki elementarnej badanego
klinoptylolitu oraz jego moduł krzemowy:
(Na0 42KX 86Mg0 46Cai 34) [Si30 16Al5 83O72] * 16,42 H2O Si/Al = 5,17
Czas [min]
Masa zadsorbowanej wody [g wody/g zeolitu]
0
30
0,109
60
0,111
http://www.erem.com.pl
Kreator PDF
Utworzono 2-03-2017, 12:46
Uzdatnianie wody
90
0,111
120
0,111
Analiza rentgenograficzna
Analiza rentgenograficzna preparatu ze złóż meksykańskich nr 045 wykazała obecność sygnałów
odpowiadających strukturze klinoptylolitu (HEU).
W dyfraktogramie widoczne są ponadto bardzo niewielkie ilości innych faz (2 theta ok. 8°; 19,5° i 22°).
Zanieczyszczenia te zostaną zidentyfikowane po ich wydzieleniu z próbki minerału.
Sorpcja pary wodnej w warunkach dynamicznych
Granulowany klinoptylolit (ziarna 1-2 mm) prażono w temp. 350°C przez 3 godziny.
Badaną próbkę zeolitu (0.503 g) umieszczono w naczyńku pomiarowym przez które przepuszczano
powietrze o temp. 12°C z natężeniem przepływu 2.5 dm3/min/ w którym prężność pary wodnej wynosiła
1402 Pa.
Masę zaadsorbowanej wody określano ważąc naczyńko wraz z próbką.
http://www.erem.com.pl
Kreator PDF
Utworzono 2-03-2017, 12:46