Użyteczność diagnostyczna zautomatyzowanego analizatora osadu
Transkrypt
Użyteczność diagnostyczna zautomatyzowanego analizatora osadu
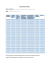
diagnostyka laboratoryjna Journal of Laboratory Diagnostics 2009 • Volume 45 • Number 4 • 301-307 Praca oryginalna • Original Article Użyteczność diagnostyczna zautomatyzowanego analizatora osadu moczu iQ200 Select Anna Rodziewicz-Lurzyńska, Małgorzata Brzozowska, Dagna Bobilewicz Zakład Diagnostyki Laboratoryjnej Wydziału Nauki o Zdrowiu Warszawskiego Uniwersytetu Medycznego Streszczenie Obecnie prawie we wszystkich obszarach diagnostyki laboratoryjnej obserwuje się ogromny postęp technologiczny, który tylko w niewielkim stopniu dotyczy badania ogólnego moczu. Jednym z powodów jest skomplikowana matryca moczu, w której cząstki różnią się od siebie wielkością nawet 100-krotnie oraz małe stężenie tych elementów. Mimo tego od kilku lat próbuje się wprowadzić analizatory moczu, które miałyby poprawić jakość otrzymywanych wyników, jak również skrócić czas oczekiwania na nie. Celem badania było porównanie metody mikroskopowej stosowanej rutynowo w laboratoriach medycznych do oceny osadu moczu z metodą automatyczną (iQ200). Uzyskano zadawalające wyniki zarówno dla erytrocytów, jak i leukocytów oraz pozostałych składników upostaciowanych moczu. Diagnostic usefulness of the iQ200 Select automated urine sediment microscopy analyser Summary Recently we observe a huge technological progression in laboratory diagnostics, but it’s less effective to urine analysis. One of the problem is a matrix, a various sizes of the particles and their low concentration in urine. There are several automated urine analyzers on the market, which can change the quality of the urine results for better and reduce the time of examination. We compared the performance of the iQ200 with traditional light microscopy and obtain satisfactory results for erythrocytes, leukocytes and others particles of urine. Słowa kluczowe:osad moczu, zautomatyzowany analizator moczu, iQ200 Key words:urine sediment, automated urine microscopy analyzer, iQ200 Badanie ogólne moczu jest jednym z najstarszych i podstawowych badań wykonywanych w laboratorium medycznym. Badanie przesiewowe, wykonywane głównie w oparciu o testy paskowe, zostało częściowo zautomatyzowane. Natomiast badanie osadu moczu, dostarczające istotnych informacji, wciąż wykonywane jest manualnie i interpretowane mikroskopowo. Jest ono zarówno praco-, jak i czasochłonne oraz pozostaje wciąż badaniem subiektywnym „autorskim”, gdyż zależy nie tylko od staranności przygotowania preparatu, ale również od doświadczenia analityka [1, 3, 6]. Niestety w wielu laboratoriach w próbkach moczu, niewykazujących zmian w badaniu „paskowym”, osady w ogóle nie są oglądane. Z tych powodów nadal poszukiwane są metody pozwalające na automatyzację wszystkich etapów badania w moczu, w tym również i osadu. Na światowym rynku i od kilku lat w Polsce wprowadzane są analizatory osadu moczu wykorzystujące technikę cytometrii przepływowej. Wykazując bardzo dobrą korelację z wynikami mikroskopowymi mają one jednak odmienną od dotychczasowej formę przed- stawienia wyników, co nastręcza lekarzom problemów z interpretacją. Drugą grupę, której przedstawicielem jest iQ200 firmy Iris Diagnostics, stanowią aparaty oparte na cyfrowej analizie zdjęć mikroskopowych, a forma wyniku nie różni się od obecnie stosowanej, gdzie elementy osadu moczu wyrażane są jako liczba cząstek w polu widzenia lub w mikrolitrze. Dodatkowo każdy wynik można sprawdzić wizualnie poprzez ocenę zdjęć na ekranie, co nie jest możliwe w technice cytometrii, gdzie do końca nie wiadomo, jakie komórki zostały przyporządkowane do danej grupy. Celem pracy było porównanie metody mikroskopowej stosowanej rutynowo w laboratorium medycznym do oceny osadu moczu z metodą automatyczną (iQ200 firmy Iris Diagnostics). Materiał i metody Materiałem do badań były 602 niewyselekcjonowane próbki moczu kierowane na badanie ogóle do Pracowni Analityki Ogólnej Centralnego Laboratorium SP CSK w Warszawie. 301 Użyteczność diagnostyczna zautomatyzowanego analizatora osadu moczu iQ200 Select Próbki moczu pochodziły bądź od pacjentów szpitalnych, bądź ambulatoryjnych i badano je w okresie czasu nie dłuższym niż 2-3 godziny od dostarczenia do laboratorium. W tym czasie przechowywane były w temperaturze pokojowej. Każdą próbkę moczu badano dwukrotnie — metodą mikroskopową zgodnie z rutynową procedurą stosowaną w laboratorium i metodą automatyczną przy pomocy analizatora iQ 200 firmy Iris Diagnostics. klatki. Z kolei program do automatycznego rozpoznawania cząstek, wykorzystując ich wielkość, kontrast i strukturę, kwalifikuje je do jednej z 12 kategorii: erytrocyty, leukocyty, skupiska leukocytów, bakterie, nabłonki płaskie, nabłonki „okrągłe”, kryształy, wałeczki szkliste, wałeczki niesklasyfikowane, drożdże, plemniki i śluz (ryc. 1) [2, 3, 4, 5, 7]. Wyniki przedstawiane są na ekranie przeglądowym operatora lub bezpośrednio przesyłane do systemu i mogą być wyrażone jako liczba cząstek w mikrolitrze lub liczba cząstek w polu widzenia. Otrzymane wyniki można przechowywać i edytować. Metoda automatyczna iQ200 Select firmy Iris Diagnostics jest w pełni zautomatyzowanym analizatorem osadu moczu. W skład systemu iQ200 wchodzi moduł mikroskopowy połączony z kamerą cyfrową i program do automatycznego rozpoznawania cząstek (APR™ – wysoko wyszkolona sieć neuronalna). Materiałem do badań jest nieodwirowany mocz w ilości 2-3 ml. Analizator automatycznie miesza i pobiera około 1 ml próbki, równocześnie aspirując izotoniczny roztwór iQ Lamina, dzięki któremu próbka może zostać zaprezentowana mikroskopowi połączonemu z kamerą cyfrową CCD. Przymocowana do mikroskopu lampa stroboskopowa jest zsynchronizowana z kamerą CCD. Błysk lampy podświetla pole widzenia mikroskopu, którego obraz zostaje utrwalony przez kamerę CCD. Kamera CCD wykonuje pięćset zdjęć w każdej próbce pod powiększeniem 400-krotnym. Następnie uzyskane obrazy są zapisywane cyfrowo i wysyłane do komputera, gdzie poszczególne zdjęcia cząstek są izolowane w obrębie jednej a) b) e) f) h) i) Metoda mikroskopowa Jako metodę odniesienia wykorzystano metodę mikroskopową stosowaną rutynowo w laboratoriach medycznych. W porównaniu do metody automatycznej badania wykonywano w próbce moczu odwirowanego (10 ml, 2000 obr./min /10 min., temperatura pokojowa). Po odwirowaniu zlewano płyn znad osadu, pozostawiając ok. 0,5 ml osadu. Preparat moczu oglądano pod mikroskopem świetlnym. Pod powiększeniem 100-krotnym liczono – nabłonki, wałeczki, a pod powiększeniem 400-krotnym erytrocyty i leukocyty oraz pozostałe elementy upostaciowane moczu. W każdym preparacie osadu liczono cząstki w 10 polach widzenia, a następnie ustalano średni przedział wartości, jako liczba cząstek w polu widzenia, przy czym liczono komórki tylko do 30 w jednym polu widzenia. Jeśli ich liczba przekraczała 30, c) d) j) k) g) Rycina 1. Kategorie samodzielnej klasyfikacji APR; a) erytrocyty, b) leukocyty, c) skupiska leukocytów, d) nabłonki płaskie, e) nabłonki „okrągłe”, f) bakterie, g) kryształy: szczawian wapnia, szczawian wapnia przypominający erytrocyt, kwas moczowy, fosforan wapnia, fosforan amonowo-magnezowy, h) wałeczki szkliste, i) drożdże, j) plemniki, k) śluz. Zdjęcia wykonane podczas pracy na iQ200 Select. 302 A. Rodziewicz-Lurzyńska, M. Brzozowska i D. Bobilewicz Rycina 2. Schemat przedstawiający ilość badanych próbek oraz sposoby wyrażania wyników: jako liczba cząstek w polu widzenia i liczba cząstek w mikrolitrze. ppw – pokrywające pole widzenia, wpw- w polu widzenia. Tabela I. Przedziały wyników dla elementów upostaciowionych przed i po wprowadzeniu zmian. Oznaczenie Powiększenie Przedziały wyników proponowane przez firmę Iris Diagnostics Zmienione przedziały wyników Erytrocyty HPF >0 – 0-3 wpw >4 – 4-10 wpw >11 – 11-15 wpw >16 – 16-25 wpw >26 – ppw >0 – 0-3 wpw >4 – 4-6 wpw >7 – 7-10 wpw >11 – 11-14 wpw >15 – 15-18 wpw >19 – 19-25 wpw >26 – 26-30 wpw >30 – ppw Leukocyty HPF >0 – 1-5 wpw >6 – 6-10 wpw >11 – 11-18 wpw >19 – 19-25 wpw >26 – ppw >0 – 0-3 wpw >4 – 4-7 wpw >8 – 8-12 wpw >13 – 13-16 wpw >17 – 17-20 wpw >21 – 21-25 wpw >26 – 26-30 wpw >30 – ppw Nabłonki okrągłe LPF 0-brak 2- pojedyncze 5- dość liczne 10- liczne 0-brak >2 – 1-2 wpw >3 – 3-5 wpw >6 – 6-8 wpw >9 – 9-14 wpw >15 – > 14 wpw HPF (High Power Field) – duże powiększenie, LPF (Low Power Field) – małe powiększenie, wpw – w polu widzenia, ppw – pokrywają pole widzenia 303 Użyteczność diagnostyczna zautomatyzowanego analizatora osadu moczu iQ200 Select to ilość cząstek upostaciowanych określano jako „pokrywające pole widzenia”. Takie próbki moczu porównano bez wyliczeń statystycznych z wynikami uzyskanymi metodą automatyczną. Ocenę analizatora iQ200 Select przeprowadzono na podstawie badań 602 próbek (ryc. 2). Wyniki badań podawano jako liczbę cząstek w polu widzenia (N=482) oraz liczbę cząstek w mikrolitrze (N=120). W przypadku 353 próbek stosowano przedziały wyników zaproponowanych przez producenta, następnie w celu przybliżenia warunków dla metody manualnej zawężono przedziały wyników dla erytrocytów i leukocytów (N=129). Dla nabłonków okrągłych zmieniono przedziały z określeń jakościowych na ilościowe (liczbę cząstek w polu widzenia) (tab. I). Każdy wynik sprawdzano poprzez ekran przeglądowy operatora i w razie potrzeby edytowano. Dla erytrocytów i leukocytów wyrażonych jako liczba cząstek w mikrolitrze wykonywano w analizatorze 21- krotne powtórzenia. Obliczenia statystyczne wykonywano przy użyciu programu STATISTICA 8.0 i Excel (Microsoft Office 2007). Wyniki Wykazano dobrą korelację wartości dla erytrocytów (r=0,75), leukocytów (r=0,72) i wałeczków szklistych (r=0,71) (tab. II, IV), która tylko nieznacznie zmieniła się po zmianie przedziałów wyników dla erytrocytów (r=0,76) i leukocytów (r=0,78) (tab. III). Przy pomocy metody automatycznej wykrywano istotnie większą liczbę erytrocytów i leukocytów (p<0,001). W grupie próbek moczu z erytrocytami i leukocytami pokrywającymi pole widzenia (>30 w polu widzenia) uzyskano porównywalne wyniki. Prawie we wszystkich przypadkach, w których tylko w jednej z metod komórki pokrywały pole widzenia w drugiej metodzie liczba erytrocytów lub leukocytów przekraczała wartości przyjęte za prawidłowe. Duże różnice odnotowane w kilku przypadkach (N=5). Najprawdopodobniej są one skutkiem wieloetapowości metody manualnej, składającej się z wielu etapów w tym wirowania, w których może dojść do utraty komórek, ponadto źle zdekantowany osad – zbyt zagęszczony lub rozcieńczony — może zafałszowywać wynik. Wykazano również, że przy pomocy metody automatycznej można wykryć większą liczbę wałeczków szklistych (p<0,001). Z uwagi na małą liczbę próbek z wałeczkami szklistymi (N=35), wyliczono również korelację dla grupy próbek moczu zawierających wałeczki szkliste powyżej 2 w polu widzenia (N=22), przy czym nie stwierdzono, iż analizator wykrywa istotnie więcej tych elementów (p>0,05) (tab. IV). Tabela II. Porównanie wyników oznaczeń erytrocytów i leukocytów w moczu metodą mikroskopową i metodą automatyczną (iQ200). Ustawienia firmowe. [Wynik wyrażony jako liczba elementów w polu widzenia]. Oznaczenie N Metoda mikroskopowa x iQ 200 Iris x Równanie regresji Współczynnik korelacji Erytrocyty 305* 2,2 2,9 y=1,34+0,73x 0,75 Leukocyty 303* 3,3 4,5 y=2,29+0,67x 0,72 * próbki moczu, w których erytrocyty lub leukocyty nie przekraczały liczby 30 w polu widzenia Tabela III. Porównanie wyników oznaczeń erytrocytów i leukocytów w moczu metodą mikroskopową i metodą automatyczną (iQ200) po zawężeniu przedziałów wyników. [Wynik wyrażony jako liczba elementów w polu widzenia]. Oznaczenie N Metoda mikroskopowa x iQ 200 Iris x Równanie regresji Współczynnik korelacji Erytrocyty 102* 3,7 4,2 y=1,25+0,80x 0,76 Leukocyty 101* 5,1 4,4 y=1,52+0,58x 0,78 * próbki moczu, w których erytrocyty lub leukocyty nie przekraczały liczby 30 w polu widzenia Tabela IV. Porównanie wyników oznaczeń liczby wałeczków szklistych w moczu metodą mikroskopową i automatyczną (iQ200) [Wynik wyrażony jako liczba elementów w polu widzenia]. Oznaczenie N Metoda mikroskopowa x iQ 200 Iris x Równanie regresji Współczynnik korelacji Wałeczki szkliste 482 0,32 0,58 y=0,28+0,95x 0,71 Wałeczki szkliste >2 wpw 22 5,8 5,9 y=1,68+0,73x 0,62 304 A. Rodziewicz-Lurzyńska, M. Brzozowska i D. Bobilewicz Uzyskano gorsze wyniki dla nabłonków „okrągłych” w porównaniu do erytrocytów, leukocytów i wałeczków szklistych (tab. V). Pomimo że w metodzie mikroskopowej wykryto więcej nabłonków okrągłych, na co wskazują średnie arytmetyczne nie wykazano statystycznie istotnych różnic. Współczynniki zmienności wyliczone w oparciu o dane z analizatora dla liczby elementów w mikrolitrze były lepsze dla erytrocytów (11,2-39,3%) i leukocytów (4,6-23,4%) niż wyrażone jako ilość elementów w polu widzenia dla meto- dy mikroskopowej, w której zarówno dla erytrocytów (26,733,3%) i leukocytów (22,2-29,1%) wartość współczynnika zmienności pozostawała stale wysoka bez względu na liczbę zliczanych cząstek (tab. VI, VII). iQ200 dawał porównywalne wyniki dla kryształów szczawianu wapnia (N=34) i kwasu moczowego (N=14), aczkolwiek małe szczawiany w niektórych przypadkach kwalifikowane były przez analizator jako erytrocyty, aczkolwiek bezpośrednia ich obserwacja nie budziła wątpliwości, do jakiej grupy Tabela V. Porównanie wyników oznaczeń liczby nabłonków „okrągłych” w moczu metodą mikroskopową i automatyczną (iQ200). [Wynik wyrażony jako liczba elementów w polu widzenia]. Oznaczenie N Metoda mikroskopowa x iQ 200 Iris x Równanie regresji Współczynnik korelacji Nabłonki okrągłe 248 1,3 1,2 y=0,37+0,66x 0,68 Nabłonki okrągłe > 2 wpw 35 7,3 6,2 y=3,77+0,33x 0,31 Tabela VI. Ocena nieprecyzyjności oznaczeń liczby erytrocytów i leukocytów w moczu przy użyciu analizatora iQ 200. [Wyniki wyrażone jako liczba elementów w μl] (N=21). Oznaczenie Średnia Odchylenie standardowe Współczynnik zmienności Erytrocyty 2,8 1,1 39,3% 4,8 1,8 37,5% 24,4 4,3 17,6% 51,4 9,0 17,5% 67,6 7,6 11,2% 430,0 60,1 14,0% 12,8 3,0 23,4% 19,2 3,8 19,8% 25,8 4,0 15,5% 34,0 7,2 21,2% 45,8 6,8 14,8% 54,7 5,6 10,2% 75,8 7,1 9,4% 969,6 44,3 4,6% Leukocyty Tabela VII. Ocena nieprecyzyjności oznaczeń liczby erytrocytów i leukocytów moczu metodą mikroskopową. [Wynik wyrażony jako liczba elementów w polu widzenia] (N=21). Oznaczenie Średnia Odchylenie standardowe Współczynnik zmienności Erytrocyty 3,0 1,0 33,3% 4,0 1,1 31,8% 31,8 8,5 26,7% 0,9 0,2 22,2% 7,9 2,3 29,1% 26,1 6,5 24,9% Leukocyty 305 Użyteczność diagnostyczna zautomatyzowanego analizatora osadu moczu iQ200 Select powinny być zakwalifikowane. Dla drożdży (N=24) wyniki otrzymywane przy pomocy analizatora były bardzo dobre, porównywalne z metodą mikroskopową, pod warunkiem dokonania przez operatora przeglądu zdjęć, w przeciwnym razie istnieje niebezpieczeństwo wyników fałszywie dodatnich. Przy pomocy analizatora wykryto znacznie mniej bakterii niż w metodzie mikroskopowej (33% wyników fałszywie ujemnych), dotyczy to szczególnie bakterii małych – ziarniaków, co z diagnostycznego punktu widzenia nie jest istotne. W przypadku tzw. „trudnych obrazów osadu moczu”, gdy w metodzie mikroskopowej nie można określić liczby erytrocytów, leukocytów i wałeczków z powodu grubej warstwy elementów komórkowych bądź mineralnych, pokrywających pole widzenia, analizator iQ200 dawał możliwość podania wyniku ilościowego (tab. VIII). Dyskusja Na jakość wyniku badania osadu ma wpływ szereg czynników, związanych z etapami przygotowywania próbki moczu jak mieszanie, wirowanie, zlewanie supernatantu i ponowne wymieszanie uzyskanego osadu. Pomimo propozycji standaryzacji etapu wirowania i przygotowywania osadu do mikroskopowania (zalecenia ECLM) nadal istnieje pewna dowolność odnośnie czasu wirowania. W popularnych w Polsce pozycjach piśmiennictwa [1] mówi się o 10 minutach, również w takim czasie uzyskiwali próbki van den Broek i wsp [2]. Również w przedstawianej pracy przyjęto ten czas, który jest stosowany do przygotowania osadu w warunkach rutynowych. Niekorzystne działanie ma również czas, jaki upływa od momentu pozyskania moczu do chwili oceny osadu. Im jest dłuższy, tym bardziej należy się liczyć z namnożeniem bakterii, a także z rozpadem komórek pod wpływem zmian pH i temperatury. Nawet prawidłowo przygotowany preparat osadu moczu nie gwarantuje wiarygodnego wyniku, gdyż oko ludzkie już po obejrzeniu kilkudziesięciu próbek ulega zmęczeniu. Wyniki uzyskane w badaniach własnych wskazują na dobrą korelację dla erytrocytów, leukocytów i wałeczków szklistych nieco gorszą dla nabłonków „okrągłych”, które są ogólnym i niesprecyzo- Bardzo dobrą zgodność wyników pomiędzy iQ200 i metodą mikroskopową (komora Fuchsa-Rosenthala) otrzymali Wah i wsp. dla erytrocytów (r=0,96) i leukocytów(r=0,94) wyrażonych jako liczba elementów w mikrolitrze [8]. Natomiast Linko i wsp. porównali wyniki iQ200 z metodą referencyjną, wykorzystującą mikroskop fazowo-kontrastowy i komorę Bűrker’a, uzyskując jeszcze lepszą korelację dla leukocytów (r=0,98) i erytrocytów (r=0,95) [5]. Shayanfar i wsp. wykazali że iQ200 ma mniejszą czułość w stosunku do leukocytów niż analizator UF-100 (cytometria przepływowa) ze względu na to, że nie zlicza on uszkodzonych leukocytów, tylko kwalifikuje je jako artefakty. Ponadto autorzy ci uzyskali niższe wyniki dla erytrocytów wyługowanych i zmienionych, które klasyfikowane były jako artefakty, przy czym w przypadku UF-100 analizator jedynie „oflagowywał” taką próbkę [7]. Natomiast według Linko i wsp. erytrocyty zmienione nawet pod mikroskopem świetlnym są trudne do rozróżnienia, dlatego dobrym rozwiązaniem wydaje się być podłączenie do analizatora sekcji czytnika pasków, co daje ogólną, dodatkową orientację odnośnie obecności erytrocytów (hemoglobiny) [5]. Z przeprowadzonych badań wynika, że metodą mikroskopową wykrywana jest mniejsza ilość wałeczków szklistych, można to wytłumaczyć rozpadem ich w trakcie wirowania, jak i ich półprzezroczystą strukturą, z powodu której łatwo je przeoczyć oglądając preparat pod mikroskopem [8]. Przez wielu autorów poruszany jest problem wykrywania obecności bakterii przez analizator iQ200 [2, 3, 4, 7]. Jednym z ograniczeń jest brak możliwości poprawienia ostrości uzyskanego zdjęcia, jak jest to w przypadku mikroskopii świetlnej [4]. Trzeba mieć jednak na uwadze, że standardem bakteriurii nadal pozostaje posiew moczu. W trakcie badań własnych uzyskiwano fałszywie dodatnie wyniki dla drożdży i kryształów. Podobne spostrzeżenia mieli także inni autorzy [2, 3, 4, 5 ]. Jednakże w trakcie przeglądu raportu wstępnego w oparciu o wykonane przez analizator zdjęcia można było taki wynik skorygować. Obserwowane kryształy również można było przyporządkować do określonej klasy, co nie jest możliwe w przypadku pomiarów cytometrycznych wanym określeniem dla nabłonków innych niż typowe, pochodzące z górnych warstw dróg wyprowadzających mocz. [7]. W trakcie badań zaobserwowano kilka przypadków, w których małe kryształy szczawianu wapnia były klasyfiko- Tabela VIII. Przykładowy wynik badania osadu moczu, w którym nie można było ustalić dokładnej liczby erytrocytów i leukocytów w metodzie mikroskopowej ze względu na obecność moczanów bezpostaciowych zestawiony z wynikiem badania metodą automatyczną. 306 Badanie osadu moczu Mikroskopowe Automatyczne (iQ200) nabłonki płaskie pojedyńcze nieliczne nabłonki okrągłe 3-5 wpw 8-12 wpw śluz skąpy bakterie bardzo liczne pojedyńcze leukocyty obecne 11-18 wpw erytrocyty obecne 16-25 wpw kryształy moczany bezpostaciowe bardzo liczne moczany bezpostaciowe obecne A. Rodziewicz-Lurzyńska, M. Brzozowska i D. Bobilewicz wane jako erytrocyty, jednakże doświadczony analityk jest w stanie je odróżnić. Z obserwacji Lamchiagdhase i wsp. Trichomonas vaginalis był kwalifikowany do kategorii nabłonków, przy czym uważają oni, że zdjęcia nie są wystarczająco wyraźne, żeby potwierdzić jego obecność ze względu na brak możliwości obserwacji charakterystycznego ruchu tego pierwotniaka [4]. Cytometr przepływowy przypisywał rzęsistka do wałeczków szklistych [3]. Celem badań własnych była nie walidacja analizatora i ocena możliwości wykorzystania go do „trudnych” osadów, które wymagają dodatkowych etapów postępowania (barwienie) lub technik (mikroskop fazowo-kontrastowy), ale wykazanie jego przydatności dla laboratoriów rutynowych, wykonujących dużą liczbę analiz. Pomimo kilku ograniczeń analizator iQ200 jest użytecznym narzędziem do pracy w laboratorium. Niewątpliwą jego zaletą jest badanie próbki moczu nieodwirowanego, co narzuca standaryzację warunków badania, znacznie skraca czas oczekiwania na wynik i zapobiega wpływom wirowania i czasu przechowywania na elementy morfotyczne, a także umożliwia ilościową ocenę elementów morfotycznych w przypadkach, kiedy inne składniki osadu pokrywają całe pole widzenia, uniemożliwiając podanie wartości liczbowych. Analizator iQ200 wykonuje 50 osadów moczu na godzinę, co znacznie przyśpiesza i ułatwia pracę szczególnie w dużych laboratoriach. Posiada przyjazne oprogramowanie pozwalające m.in. na przedstawianie wyniku jako liczby elementów w polu widzenia i liczby w mikrolitrze. Edytowanie wyniku, tzn. przegląd zdjęć zakwalifikowanych do poszczególnych kategorii i ewentualne przeniesienie do innych, jest dodatkowym atutem. Zaletą jest także możliwość połączenia analizatora ze stacją biochemiczną (czytnik pasków), co stanowi już pełną jednostkę automatyczną. Wnioski Zastosowanie w pracy rutynowej analizatora iQ200 Select eliminuje etapy przygotowywania preparatu osadu moczu, skraca czas uzyskania wyniku, a także umożliwia uzyskanie szczegółowych danych odnośnie liczby elementów morfotycznych w przypadkach dużej ilości kryształów bezpostaciowych czy innych elementów pokrywających grubą warstwą pole widzenia. Cechy te wpływają pozytywnie na jakość wyniku. Analizator osadu moczu iQ200 Select firmy Iris Diagnostics może być wykorzystywany w codziennej praktyce laboratoryjnej, przy czym w przypadkach trudnych i niejednoznacznych do interpretacji osadów konieczna jest indywidualna korekta poprzez ocenę zdjęć lub dodatkowa ocena mikroskopowa. Piśmiennictwo: 1. Węgrowicz-Rebandel I, Rebandel H. Atlas osadu moczu PZWL, Warszawa 2006. 2. Broek D, Keularts I, Wielders J. Benefits of the iQ200 automated urine microscopy analyser in routine urinalysis. Clin Chem Lab Med 2008; 46: 1635-1640. 3. Chien TI, Kao JT, Liu HL. Urine sediment examination: A comparison of automated urinalysis systems and manual microscopy. Clin Chim Acta 2007; 384: 28-34. 4. Lamchiagdhase P, Preechaborisutkul K, Lomsomboon P. Urine sediment examination: A comparison between the manual method and iQ200 automated urine microscopy analyzer. Clin Chim Acta 2005; 358: 167-174. 5. Linko S, Kouri TT, Toivonen E. Analytical performance of the Iris iQ200 automated urine microscopy analyzer. Clin Chim Acta 2006; 372: 54-64. 6. Mayo S, Acevedo D, Quinones-Torrelo C. Clinical Laboratory Automated Urinalysis: Comparison among automated microscopy, flow cytometry, two test strip analyzers, and manual microscopic examination of urine sediments. J Clin Lab Anal 2008; 22: 262-270. 7. Shayanfar N, Tobler U, von Eckardstein A. Automated urinalysis: first experiences and comparison between the Iris iQ200 urine microscopy system, the Sysmex UF-100 flow cytometer and manual microscopic particle counting. Clin Chem Lab Med 2007; 49(9): 1251-1256. 8. Wah DT, Wises PK, Buth AW. Analytic performance of iQ200 automated urine microscopy analyzer and comparison with manual counts using Fuchs-Rosenthal cell chambers. Am J Clin Pathol 2005; 123: 290-296. Adres Autorów: Zakład Diagnostyki Laboratoryjnej WUM ul.Banacha 1a 02-097 Warszawa (Praca wpłynęła do Redakcji: 2010-01-01) (Praca przekazana do opublikowania: 2010-02-12) 307