Wpływ wodnego ekstraktu z kłączy )RIS DICHOTOMA 0ALL na
Transkrypt
Wpływ wodnego ekstraktu z kłączy )RIS DICHOTOMA 0ALL na
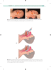
&ARM0RZEGL.AUK COPYRIGHT'RUPADR!2+WIECIÊSKIEGO)33. 7PYWWODNEGOEKSTRAKTUZKCZY)RISDICHOTOMA0ALL NAAKTYWNOu¿MITOTYCZNOCENIANTESTEMALLIUM )NFLUENCEOFTHEWATEREXTRACTFROMRHIZOMEOF)RISDICHOTOMA0ALL ONTHEMITOTICACTIVITYOFALLIUMTESTCELLS /TGONBAATAR50UREVSUREN'/YUN:.ARANTSETSEG'+HISHGEE$ 5RJIN".OWAKOWSKA*-ACHALSKA!:OBEL!+URAu-'OWNIAK+ )NSTITUTEOF4RADITIONAL-EDICINE5LAANBAATAR-ONGOLIA 5NIWERSYTET7ARSZAWSKI0RACOWNIA-IKROSKOPII%LEKTRONOWEJ !KADEMIA-EDYCZNAW,UBLINIE+ATEDRAI:AKAD&ARMAKOGNOZJI Z0RACOWNI2OuLIN,ECZNICZYCH 4RENT5NIVERSITY0ETERBOROUGH/NTARIO+*"#ANADA 5NIWERSYTET7ARSZAWSKI:AKAD%KOTOKSYKOLOGII Streszczenie Summary W pracy przebadano wpływ wodnego ekstraktu z kłączy Iris doichotoma Pall. na merystemy wierzchołkowe korzeni, strukturę euchromatyny jąder interfazowych i chromosomów mitotycznych oraz aktywność podziałową komórek Testu Allium. Stwierdzono, że pod wpływem inkubacji w wysokich stężeniach ekstraktu, zarówno chromatyna jąder interfazowych jak i chromosomy podziałowe ulegały kondensacji, pogrubieniu i skróceniu. Procent dzielących się komórek ulegał początkowo redukcji a później całkowitemu zahamowaniu. Małe stężenia ekstraktów powodowały despiralizację chromatyny. Wzrastał procent dzielących się komórek. Mamy tu, zatem dwojakie działanie ekstraktów z kłączy Iris i można przypuszczać, że badany ekstrakt może mieć istotne znaczenie zarówno w zapobieganiu jak i leczeniu chorób nowotworowych związanych z modyfikacją indeksu mitotycznego i fazowego. A water extract from rootstock of Iris dichotoma Pall. was used to investigate its effect on meristem cells of the root tips of the Allium Test. The structure of chromatin of the interphase nuclei was changed as compared to the control. The highest concentrations (16 and 8 mg/mL) caused condensation of chromatin. Dividing cells contained chromosomes shortened and thickened, but no chromosomal aberrations were visible. There was a decrease in the number of mitoses, and already after 24 hours total inhibition. The lowest concentrations caused despiralisation of chromatin, and the percentage of mitoses increased; thus a dual mechanism of reaction was found, which could be used for both stimulation and inhibition of mitoses, dependent on concentration. Key words: Iris dichotoma, extract from rhizome, change structure of chromatin, condensed and contracted chromosomes, modification of mitotic and phase index. Słowa kluczowe: Iris dichotoma, ekstrakty z kłączy, zmiana struktury chromatyny, kondensacja i kontrakcja chromosomów, modyfikacja indeksu mitotycznego i fazowego. ' Ö Żyjemy w dobie niezwykłego progresu chorób cywilizacyjnych (otyłość, cukrzyca, choroby nowotworowe, choroby serca i układu krążenia), wobec których w większości bezradna jest medycyna akademicka (konwencjonalna). W związku z tym obserwujemy bardzo dynamiczny rozwój fitochemii, pociągający za sobą, duże zainteresowanie lekami pochodzenia roślinnego i duże zapotrzebowanie na surowce roślinne o dużej zawartości poszukiwanych substancji. Szczególnie cennymi są tu rośliny odznaczające się właściwościami przeciwnowotworowymi. W większości są to rośliny egzotyczne pochodzące ze strefy klimatu tropi- kalnego, gdzie nadzwyczajnych właściwości leczniczych nabywają dzięki specyficznym warunkom glebowym i klimatycznym. Szczególne właściwości przypisuje się roślinom południowo-amerykańskim i śródziemnomorskim. Nie stanowi to jednak bezwzględnej reguły, bowiem na każdym kontynencie i nieomal w każdym zakątku naszego globu, znane są różnorodne leki roślinne używane powszechnie w ludowym lecznictwie. Do takich należy również, rosnący w ostrym klimacie pustynnym Mongolii Iris dichotoma Pall. Należy on do rodzaju Iridaceae i zawiera różne biologicznie czynne substancje, takie jak: kumaryny, saponiny, chinony [1], iridoidy [2], flawony i izoflawony [3] i inne, dzięki którym od lat używany jest w medycynie ludowej tego kraju (Ryc. 1). &ARM0RZEGL.AUK z 1938 r.) [4]. Stanowiły je komórki merystematyczne korzeni przybyszowych Allium cepa. Hodowano je w wodzie destylowanej w 300 ml naczyniach Erlenmayera w warunkach laboratoryjnych Zakładu Ekotoksykologii UW. Kiedy korzenie osiągnęły długość 3 cm (± 0,5 cm) wraz z cebulami przenoszono je do w/w roztworów w 50 ml zlewkach. Inkubację w nich prowadzono przez 12, 36, 60 i 84 godz. W celu zbadania wpływu ekstraktu na aktywność mitotyczną (indeks mitotyczny i fazowy) komórek Testu Allium w czasie eksperymentu odcinano wierzchołki korzeni (o długości ok. 2-3 mm), barwiono je i macerowano w 2% roztworze acetoorceiny z dodatkiem 1N HCl (w stosunku 9:1) i wykonywano preparaty gniecione na szkiełkach podstawowych. Indeks mitotyczny i fazowy obliczano według metody opisanej przez Lopez-Saez and Fernandez-Gomez i innych [5 – 9]. Dla każdego wariantu doświadczenia pobierano po sześć korzeni z trzech analogicznych cebul. Średnie wyniki indeksu mitotycznego i fazowego wraz z odchyleniami standardowymi przedstawiono na wykresach a zmiany morfologii chromosomów fotografowano przy użyciu mikroskopu świetlnego (NU Zeiss) i standardowej kamery fotograficznej (Nikon) oraz przedstawiono na tablicach. Ryc. 1. Kwiat Iris dichotoma Pall Do wstępnych badań ekstraktów tej rośliny zastosowaliśmy niezwykle dogodny test Allium [4]. Stanowią go merystematyczne komórki wierzchołków korzeni przybyszowych Allium cepa L. Cechują się one dużą jednorodnością genetyczną, łatwe są do hodowli i wykonania preparatów mikroskopowych, a co najważniejsze są niezwykle dogodnym materiałem kariologicznym: posiadają duże jądra komórkowe z niewielką liczbą (16) dużych chromosomów, na których bardzo łatwo w mikroskopie świetlnym można obserwować i liczyć wszelkie mutageniczne aberracje chromosomowe w poszczególnych fazach mitozy. Celem naszych badań było ustalenie, w oparciu o ten dogodny test, wpływu wodnego ekstraktu z kłączy irysa, na biologiczną jego aktywność a w tym: na strukturę interfazowej chromatyny i chromosomów podziałowych oraz na frekwencję podziałową komórek a więc cechy określające cytostatyczne/cytotoksyczne własności badanego ekstraktu jako potencjalnego preparatu przeciwnowotworowego. - Rl-tluR |J¬ Materiałem badanym były wysuszone i sproszkowane kłącza Iris dichotoma Pall. zbierane ze stanowisk naturalnych na stepach w okolicach Ułanbator i otrzymane z Instytutu Medycyny Naturalnej z Mongolii. Wodny ekstrakt z kłączy przygotowano zalewając 1 g wysuszonego i sproszkowanego materiału 40 ml wrzącej wody destylowanej a następnie pozostawiano mieszaninę na 24 godz. w temperaturze pokojowej. Po tym czasie ekstrakt przesączano i wyjściowo obliczano stężenie substancji rozpuszczonych na 6 mg/ml. Ekstrakt wyjściowy do eksperymentu był odpowiednio rozcieńczany w celu otrzymania szeregu następujących stężeń: 0,1; 0,2; 0,4; 0,75; 1,5; 3,0 i 6 mg/ml. Równoległa kontrola prowadzona była w wodzie destylowanej. Badania wykonano na komórkach Testu Allium (Test Levana '¬ylpl Podczas inkubacji korzeni Allium w ekstraktach z kłączy irysa o różnym stężeniu przez 60 godz. zaobserwowano wyraźne zmiany w ich morfologii. Korzenie inkubowane w ekstrakcie o najniższym stężeniu (0,1 mg/ml) były dłuższe od korzeni kontrolnych i nie posiadały widocznych cech jakiejkolwiek deformacji (Ryc. 2b). Podczas inkubacji w wyższych stężeniach ekstraktu (0,4 i 1,5 mg/ml) na pograniczu elongacyjnej i merystematycznej strefy wierzchołka korzeni, pojawiały się charakterystyczne zgrubienia oznaczone na fotografii klamrą (Ryc. 2c i 2d). Inkubacja korzeni w ekstrakcie o stężeniach najwyższych (3 i 6 mg/ml) spowodowała zahamowanie ich wzrostu i były one krótkie i dodatkowo ciemno zabarwione (Ryc. 2e). Analiza preparatów mikroskopowych wykazała wpływ inkubacji w ekstrakcie na intensywność podziałów komórkowych i morfologię jąder interfazowych i chromosomów mitotycznych. Na preparatach kontrolnych obserwowano regularne podziały mitotyczne o natężeniu charakterystycznym dla komórek Testu Allium wynoszącym ok. 10%. Jądra komórek interfazowych miały zróżnicowanie skondensowaną chromatynę w zależności od fazy cyklu komórkowego, w której się znajdowały (Ryc. 3a). W komórkach kontrol- Ryc. 2. Morfologia korzeni Allium cepa L. poddanych działaniu różnych stężeń wodnego ekstraktu z kłącza Iris dichotoma Pall. przez 36 godz. a) kontrola; b) 0,1 mg/ml; c) 0,4 mg/ml; d) 1,5 mg/ml, e) 3,0 mg/ml COPYRIGHT'RUPADR!2+WIECIÊSKIEGO)33. sowaną euchromatynę i były one wyraźnie mniejsze i silniej wybarwione w porównaniu od jąder kontrolnych (Ryc. 4b). Analiza indeksu mitotycznego, czyli procentu dzielących się komórek wykazała, że w czasie ciągłej inkubacji od 0 do 84 godz. następowały zmiany procentu dzielących się komórek zależne od użytego stężenia ekstraktu i czasu trwania inkubacji (Ryc. 5). Dwa najniższe stężenia (0,1 i 0,2 mg/ml) były stymulujące dla podziałów komórkowych juz od 12 godz. i pozostawały stymulującymi do 84 godzin. Najwyższą wartość indeksu mitotycznego odnotowano pod wpływem stężenia 0,1 mg/ml po 36 godz. inkubacji i wynosiła ona ok. 150% kontroli (Ryc. 3c). Inkubacja w ekstrakcie o stężeniu 0,4 mg/ml spowodowała obniżenie indeksu mitotycznego po 12 godz. inkubacji do ok. 60% a następnie jego powolny wzrost aż po 84 godz., kiedy osiągnął on wartość zbliżoną do kontroli wyjściowej (100%). Pod wpływem działania ekstraktu o stężeniu wyższym (1,5 mg/ml) również po 12 godz. doszło do znacznego obniżenia wartości indeksu mitotycznego (Ryc. 3b) a następnie wraz z upływem czasu inkubacji do jego ponownego wzrostu. Z tym, że po 84 godz. wartość indeksu spadła bardziej niż w poprzednim stężeniu do ok. 70% indeksu kontrolnego. Inkubacja korzeni w najwyższym ze stosowanych w eksperymencie stężeniu Ryc. 3. Obraz aktywności podziałowej komórek Testu Allium korzeni kontrolnych oraz po inkubacji w ekstraktach z kłącza Iris dichotoma a) podziały kontrolne; b) po 12 godzinnej inkubacji w ekstrakcie o stężeniu 1,5 mg/ml; c) po 36 godzinnej inkubacji w ekstrakcie o stężeniu 0,1 mg/ml; d) po 60 godzinnej inkubacji w ekstrakcie o stężeniu 6 mg/ml. (Pow. 400x) nych Testu Allium chromosomy profazowe miały w różnym stopniu skondensowaną chromatynę tworzącą różnej grubości splątane nici chromosomów (Ryc. 4a), które w metafazie układały się w płytce metafazowej a podczas anafazy, ich siostrzane połówki (chromatydy) w sposób uporządkowany rozchodziły się do biegunów komórki. Na etapie telofazy nowo powstające jądra po wytworzeniu błony jądrowej i jąderka, stopniowo przybierały regularne kształty a chromatyna ulegała dekondensacji. Inkubacja korzeni Allium cepa w ekstrakcie z kłączy irysa (0,75 - 6 mg/ml) spowodowała zmiany w morfologii chromosomów polegające na silnej ich kondensacji i kontrakcji nie doprowadzającej jednak do powstawania aberracji chromosomowych. Jądra te w dalszej części pracy będą określane jako zmienione - cc (z ang. condensed and contraction). Były to liczne cc-profazy (Ryc. 4c), w których chromosomy były silnie skondensowane a pomiędzy nimi uwidaczniały się wyraźne przejaśnienia kariolimfy. Zmienione metafazy posiadały silnie skondensowane, skrócone chromosomy zwykle ułożone w rozproszeniu typowym dla C-metafaz (typowych dla komórek po działaniu kolhicyną) (Ryc. 4d) lub ściśle ułożone w płytkę metafazalną (Ryc. 4e). Wśród anafaz i telofaz występowały również zmiany cc (Ryc. 4f i 4g). Po całkowitym wyhamowaniu aktywności mitotycznej (po 36 godz. inkubacji) w najwyższym stężeniu ekstraktu, również jądra komórek interfazowych miały silnie skonden- Ryc. 4. Morfologia chromosomów kontrolnych komórek Testu Allium oraz pod wpływem inkubacji w wodnym ekstrakcie z I. dichotoma. a) Kontrolny obraz komórek w poszczególnych fazach mitozy (P-profaza; M-metafaza; A-anafaza; T-telofaza); b) zmieniona morfologia interfazowych jąder komórek traktowanych przez 36 godzin ekstraktem o stężeniu 6 mg/ ml; c) zmieniona profaza z wyraźnie zgrubiałymi chromosomami; d) zmieniona metafaza, chromosomy krótkie i zgrubiałe rozrzucone na terenie cytoplazmy; e) zmieniona metafaza gdzie chromosomy są ułożone skośnie w płytce metafazowej, tez są skrócone i zgrubiałe; f) zmieniona anafaza; g) zmieniona telofaza. (Pow. 800x) &ARM0RZEGL.AUK wała wyraźny wzrost procentu profaz i metafaz po 12 godz. inkubacji, kiedy to dochodziło do wyraźnej redukcji podziałów a jednocześnie pojawiały się mitozy zmienione, które stanowiły znaczny odsetek wszystkich komórek dzielących się (Ryc. 6b). Może to wskazywać na mechanizm blokowania cyklu komórkowego w punkcie metafaza/anafaza, który może być związany z uszkodzeniami cytoszkieletu tubulinowego w komórkach. Najwyższa z użytych koncentracji ekstraktu, również po 12 godz. inkubacji spowodowała wyraźny wzrost indeksu profaz a tym samym spadek udziału pozostałych trzech faz mitozy. Po 36 godz. inkubacji doszło już do całkowitego zahamowania podziałów komórkowych (Ryc. 6d). ¬p¥o-lªyl|pl Ryc. 5. Indeksu mitotyczny kontrolnych komórek Testu Allium i po inkubacji w różnych stężeniach ekstraktu (0,1; 0,2; 0,4; 0,75; 1,5 i 6,0 mg/ml) z I. dichotoma W oparciu o powyższe badania działania wodnego ekstraktu z I. dichotoma na komórki Testu Allium wyodrębniono trzy zasadnicze typy reakcji w zależności od jego koncentracji. ekstraktu (6 mg/ml) juz po 12 godz. spowodowała obniżenie inDziałanie stężeń najniższych uwidaczniało się w przyspieszaniu deksu mitotycznego do 25% i całkowitą jego inhibicję po 36 godz. (stymulacji) wzrostu merystemów korzeniowych w stosunku i na tym poziomie pozostawał on do 84 godz. inkubacji (Ryc. 3d). do kontrolnych. Skorelowane to było z obserwowaną, wyraźną Wyniki tych zmian przedstawiono na wykresie (Ryc. 5). despiralizacją chromatyny interfazowej prowadzącej najprawdoJednocześnie ze zmianami indeksu mitotycznego w czapodobniej do zwiększenia jej transkrypcyjnego potencjału przesie trwania inkubacji w ekstraktach wystąpiły zmiany indekjawiającego się w dalszej konsekwencji w skróceniu faz cyklu su fazowego (procent komórek w poszczególnych fazach komórkowego oraz wzmożonej aktywności mitotycznej [10]. mitozy) (Ryc. 6). W początkowych godzinach inkubacji Działanie średnich z badanych koncentracji ekstraktu w niższych stężeniach ekstraktu (0,1 – 0,4 mg/ml) indeks przejawiało się z kolei w tworzeniu charakterystycznych profaz był niższy w porównaniu do kontroli a indeks mezgrubień dystalnej części strefy przejściowej pomiędzy stretafaz lekko wzrastał ponad poziom kontroli. Generalnie nie fą mitoz a elongacji komórek, podobnych do tych, jakie pobyły to zmiany istotne i nie zaobserwowano występowania wstają np.: po działaniu kolchicyny lub soli metali ciężkich podziałów zmienionych (cc) (Ryc. 6a i 6c). Natomiast inku(ołowiu, kobaltu i manganu). Jak wynika z naszych wczebacja w roztworach o stężeniach 0,75 i 1,5 mg/ml spowodośniejszych badań, zgrubienie to jest efektem częściowego lub całkowitego zahamowania podziałów komórkowych w strefie mitotycznej, przy jednoczesnej zmianie kierunku wzrostu komórek strefy elongacyjnej [11], co związane jest ze zmianą reorientacji mikrotubul cytoszkieletu tubulinowego. Natomiast redukcja/zahamowanie podziałów w części mitotycznej następiło najprawdopodobniej na skutek drastycznego zablokowania syntezy białek tubulinowych, co przejawia się w zakłóceniu reorientacji chromosomów w okresie ich przejścia z fazy G2 do M i w samej Ryc. 6. Indeks fazowy pod wpływem inkubacji w różnych stężeniach ekstraktu z I. dichotoma, w różnym czasie trwania inkubacji a) Indeks fazowy w komórkach Testu Allium w trakcie inkubacji w ekstrakcie o stężeniu mitozie przy przejściu 0,1 mg/ml; b) Indeks fazowy w komórkach Testu Allium w trakcie inkubacji w ekstrakcie o stężeniu 0,75 mg/ml; z profazy do metafazy c) Indeks fazowy w komórkach Testu Allium w trakcie inkubacji w ekstrakcie o stężeniu 0,4 mg/ml; d) Indeks i z metafazy do anafazy fazowy w komórkach Testu Allium w trakcie inkubacji w ekstrakcie o stężeniu 6 mg/ml COPYRIGHT'RUPADR!2+WIECIÊSKIEGO)33. [10]. Podobne sytuacje, aczkolwiek związane z inhibicją polimeryzacji bądź depolimeryzacji mikrotubul tubulinowych mamy do czynienia w przypadku wielu cytostatyków jak np.: winblastyna, winkrystyna, Taxol i Taxoter oraz kofeina [8, 12]. Istnienie tej bariery pomiędzy poszczególnymi fazami mitozy uniemożliwia jej zakończenie, ale poprzez ich restytucję, ponowne cofanie się do interfazy. Doprowadza to z kolei do stopniowej redukcji poziomu aktywności mitotycznej albo do całkowitego jej wygaśnięcia. Komórki te jednak nadal zachowują żywotność, której poziom może nawet nagle i falowo wzrastać w momencie ponownego przeniesienia komórek do środowiska kontrolnego. Ekstrakty o tych stężeniach zmieniają więc metabolizm komórek nie powodując jednak ich aberracyjnej – mutagennej dezorganizacji ani zwiększenia ich śmiertelności. Stężenia te określane są one jako cytostatyczne lub subletalne. Z kolei najwyższe ze stosowanych stężeń prowadziły do nieodwracalnych zmian morfologicznych całych merystemów oraz daleko posuniętych morfologicznych zmian chromatyny interfazowej i chromosomów podziałowych polegającej na ich kondensacji i kontrakcji. Taka kondensacja określana często jako „heterochromatynizacja” a prawidłowiej jako kondensacja euchromatyny [13] prowadzi do całkowitej inhibicji transkrypcji a w konsekwencji zablokowania translacji i aktywności podziałowej oraz do totalnej inaktywacji całej tkanki aktywnej podziałowo. Takie działanie czynnika zmieniajacego poziom aktywności podziałowej, określane jest jako cytotoksyczne – letalne. Powyższe wyniki badań wskazują, zatem na pewną dwoistość działania wodnego ekstraktu z kłącza Iris dichotoma. Z jednej strony na działanie cytoprotekcyjne i stymulujące a z drugiej na ich działanie inhibujące. W związku z takim działaniem na komórki Testu Allium mamy tu analogię do immunomodulacyjnego działania innych cytostatyków na komórki ludzkie i zwierzęce a wyrażające się (zależnie od stężenia) w immunostymulacyjnym lub immunosupresyjnym działaniu [14]. Być, zatem może, że przejawiające się dwojakie działanie ekstraktu z I. dichotomia na komórki Testu Allium może w odniesieniu do komórek ludzkich i zwierzęcych okazać się właśnie działaniem „immunomodulacyjnym”. Gdyby tak było to ekstrakty z kłączy irysa mogłyby mieć zastosowanie jako typowe roślinne preparaty wspomagające terapię nowotworową. Właśnie ze względu na to dwojakie działanie wodnego ekstraktu z kłączy I. dichotoma bardzo ważnym staje się dokładne przebadanie mechanizmu jego działania na komórki ludzkiego organizmu, oraz ustalenie odpowiednich dawek preparatu w zależności od potrzeb tak aby wykluczyć np.: możliwość stymulacji rozwoju choroby nowotworowej podczas jego stosowania. Dalsze badania w tym kierunku wydają się być bardzo celowe i powinny prowadzić do ustalenia przeciwnowotworowych aspektów ich działania. Reasumując dotychczasowe nasze wyniki badań możemy stwierdzić, że: 1. Wodny wyciąg z kłączy I. dichotoma wykazuje podwójne działanie („immunomodulujące”) na badane komórki Testu Allium w zależności od stężenia: A) Niższe stężenia 0,1-0,4 mg/ml działały stymulująco na aktywność podziałową B) Najwyższe stężenie 6,0 mg/ml działało inhibujaco na tą aktywność. 2. Głównym czynnikiem powodującym zmianę aktywności podziałowej był stopień kondensacji chromatyny. 3. Zmianom struktury i kondensacji chromatyny nie towarzyszyły aberracje – wywołujące skutki mutagenne. 4. Mechanizm kondensacji chromatyny należy opracować szerzej używając metod cytofotometrychnych, w tym należy ustalić mechanizm zmian struktury chromatyny przy różnych koncentracjach ekstraktu i w różnych fazach cyklu komórkowego. 5. Oba powyższe efekty działania ekstraktu z I. dichotoma (stymulacji i inhibicji) należy rozpatrywać z punktu widzenia ich użyteczności w działaniach prewencyjnych i/ lub terapeutycznych walki z rakiem Piśmiennictwo 1. Rahman A. et al. Two New Quinones from Iris bungei. Chem Pharm Bull 2000; 48: 738-739. 2. Choudhary M.I. et al. Five New Peltogynoids from Underground Parts of Iris bungei: A Mongolian Medicinal Plant. Chem Pharm Bull 2001; 49: 1295-1298. 3. Choudhary M.I. et al. Four New Flavones and a New Isoflavone from Iris bungei. J Nat Prod 2001; 64: 857-860. 4. Levan A. The effect of colchicine on root mitosis in Allium. Hereditas 1938; 24: 471-486. 5. Lopez-Saez, J.F., Fernandez-Gomez E. Partial mitotic index and phase indices. Experientia 1965; 21: 591-592. 6. Kuraś M., Malinowska A. Influence of 1-b-D arabinofuranosylcystoine on mitotic activity of apical meristem of onion (Allium cepa L.) roots. Acta Soc Bot Polon 1978; 47: 173-187. 7. Keithtey A.M. et al. Coumarin and its 4- and 7- substituted derivates as retardants of mitoses in Allium root promeristem. Int J Pharmacogn 1996; 34: 105-113. 8. Majewska, A. i wsp. Influence of extracts from schoots of Taxus baccata var. Elegantissima on mitotic activity of meristematic cells of Allium cepa L. roots. Acta Soc Bot Polon 2001; 63: 185-192. 9. Kuraś M. i wsp. Changes in chromosome structure, mitotic activity and nuclear DNA content from cells Allium Test induced by bark water extract of Uncaria tomentosa (Willd.) DC. J Ethnopharmacol 2006; 107: 211-221. 10. Woźny A., Michleda J., Ratajczak L. Podstawy biologii komórki roślinnej. Wyd. Naukowe UAM, Poznań 2000. 11. Wierzbicka M. The effect of leads on the ultrastructural changes in the root tip onion – Allium cepa L. Folia Histochem Cytobiol 1986; 24: 340-341. 12. Podbielkowska M. i wsp. Effect of coumarin and its derivatives no mitosis and ultrastructure of meristematic cells. Int J Pharmacogn 1995; 33: 7-15. 13. Olszewska M.J. Heterochromatyna i “heterochromatynizacja”. Post Biol Kom 2007; 34: 391-407. 14. Skopińska-Różewska E. Wpływ substancji naturalnych na układ odpornościowy. Wyd. Fundacja Pomocy Zdrowiu – Medycyna Naturalna, Warszawa 2002. Adres do korespondencji: Prof. dr hab. Mieczysław Kuraś, ul. Miecznikowa 1, 02-096 Warszawa, tel. 22 554-20-07, e-mail: [email protected]