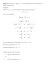wyznaczanie współczynnika podziału oktanol/woda
Transkrypt
wyznaczanie współczynnika podziału oktanol/woda
WYZNACZANIE WSPÓŁCZYNNIKA PODZIAŁU OKTANOL/WODA SUBSTANCJI TOKSYCZNYCH TECHNIKĄ HPLC WPROWADZENIE Aktywność biologiczna związku chemicznego wiąże się w sposób bezpośredni z jego cechami fizykochemicznymi. Najbardziej użytecznym parametrem w przewidywaniu aktywności biologicznej danej substancji, a także prognozowania jej aktywności toksycznej jest lipofilowość - parametr będący wypadkową kilku cech. Lipofilowość charakteryzuje powinowactwo związku chemicznego do fazy lipidowej i wodnej, a jej miarą jest stosunek równowagowych stężeń rozpuszczonej substancji w układzie dwufazowym, składającym się z dwóch niemieszających się rozpuszczalników. Zgodnie z prawem Nernsta, w warunkach równowagi termodynamicznej, w stałej temperaturze i przy stałym ciśnieniu, stosunek stężeń (a dokładniej aktywności) rozpuszczonej substancji w obu takich rozpuszczalnikach jest wielkością stałą, zwaną współczynnikiem podziału. Należy zaznaczyć, iż wartość współczynnika podziału nie zależy od aktywności substancji rozpuszczonej, jest natomiast cechą charakterystyczną dla danego układu dwóch rozpuszczalników i jednej substancji rozpuszczonej, zależną od temperatury i ciśnienia. Lipofilowość jest ważnym parametrem charakteryzującym substancje czynne biologicznie jakimi są leki czy środki ochrony roślin. Działanie substancji chemicznej (leku lub trucizny) na żywy organizm to szereg procesów biofizycznych i biochemicznych, które podzielić można na trzy fazy: farmaceutyczną, na którą składa się forma w jakiej przyjmowana substancja dociera do organizmu, sposób jej podania oraz uwalniania się w organizmie; farmakokinetyczną, czyli transport cząsteczek substancji w organizmie, ich metabolizm i eliminacja; farmakodynamiczną, czyli oddziaływanie cząsteczki substancji z farmakoreceptorem przynoszące pożądany efekt farmaceutyczny. 1 Choć każdy z tych etapów jest związany z charakterem lipofilowym substancji, to najistotniejszy wpływ wywiera lipofilowość na procesy dystrybucji związku chemicznego w organizmie, czyli na fazę farmakokinetyczną. Szczególną uwagę należy zwrócić na zachowanie się danej substancji podczas przenikania przez lipofilowe błony komórkowe oddzielające środowiska wodne. Lipofilowość jest opisywana przez procesy podziałowe między dwiema fazami: niepolarną (organiczną) i polarną (najczęściej wodną). Przyjęto, że rozpuszczalnikami najlepiej odwzorowującymi układ faz polarnych i niepolarnych w ustroju biologicznym oraz środowisku naturalnym są n-oktanol i woda. Rozpuszczalniki te po zmieszaniu tworzą dwie rozseparowane fazy, przy czym ze względu na wzajemną częściową rozpuszczalność jest to układ zawierający oktanol nasycony wodą (2,3 mol/L) oraz wodę nasyconą oktanolem (4,5.10-3 mol/L). Współczynnik podziału P jest wyrażany ilorazem dwóch stężeń substancji rozpuszczonej: (1) gdzie: Cokt (mol/L) stężenie molowe substancji w oktanolu, a Cw (mol/L) stężenie molowe substancji w wodzie. Współczynnik taki mierzy się w 25°C, przy stężeniu substancji badanej nie wyższym niż 0,01 mol/L. W takim układzie, jeżeli większa ilość cząsteczek badanego związku chemicznego znajdzie się w fazie oktanolowej, to mamy do czynienia ze związkiem lipofilowym (hydrofobowym). Jeżeli zaś większość pozostanie w fazie wodnej, będzie to związek lipofobowy (hydrofilowy). W fazie oktanolowej, dominującymi staną się oddziaływania dyspersyjne pomiędzy hydrofobowymi fragmentami cząsteczki rozpuszczonego związku a łańcuchem alkilowym n-oktanolu, podczas gdy nieco mniejsze znaczenie odgrywać tu będą oddziaływania dipol-dipol czy wiązania wodorowe z grupą hydroksylową alkoholu. Wynika stąd jednak, iż n-oktanol posiada zarówno właściwości lipo- jak i hydrofilowe, a cechę taką nazywa się amfifilowością. Zjawisko to przedstawiono schematycznie na rys. 1, gdzie uwidoczniono cząsteczkę rozpuszczonego benzenu w n-oktanolu (oddziaływania dyspersyjne), w którym równocześnie rozpuszczona jest woda (oddziaływania dipol-dipol i wiązania wodorowe). W fazie wodnej z kolei, występować będą niemal wyłącznie wiązania wodorowe oraz oddziaływania dipol-dipol pomiędzy polarnymi fragmentami cząsteczki związku rozpuszczonego a wodą. 2 Rys.1. Oddziaływania międzycząsteczkowe substancji rozpuszczonych w n-oktanolu Wartość współczynnika podziału zależy zarówno od budowy chemicznej cząsteczki rozpuszczonego związku (liczba i rodzaj różnych grup funkcyjnych, udział miejsc nienasyconych, fragmentów alkilowych, wartość momentu dipolowego i in.) jak i, w dużej mierze, od jej wielkości. W trakcie mieszania obu rozpuszczalników (proces spontaniczny) całkowita entropia takiego układu gwałtownie wzrasta, jednak jej uprzywilejowany wzrost będzie ograniczany spadkiem entropii w fazie wodnej, związanym ze stopniowym uporządkowywaniem cząsteczek wody w otoczce hydratacyjnej solwatowanego związku. Ponieważ większe rozmiary cząsteczki wymagać będą coraz większej wnęki w rozpuszczalniku (większej otoczki hydratacyjnej) powodować to będzie nieuprzywilejowany spadek entropii całego układu. W takiej sytuacji korzystniejsze termodynamicznie staje się obniżenie rozpuszczalności cząsteczek o dużych rozmiarach w fazie wodnej, co wpływa na zwiększenie współczynnika podziału. Stąd też nawet stosunkowo duże cząsteczki, ale zawierające w swojej strukturze układy nienasycone, rozgałęzione i in., ułatwiające zmniejszenie rozmiaru molekularnego, charakteryzują się dużo niższymi współczynnikami podziału od swoich analogów pozbawionych tych cech. Współczynnik podziału oktanol – woda zmierzony dla typowych zanieczyszczeń środowiska mieści się w bardzo szerokim zakresie od 0,01 dla związków o wysokiej polarności do 1010 dla substancji wysoce hydrofobowych. Na rysunku 2 przedstawiono zakres wartości współczynnika podziału dla wybranych toksycznych związków organicznych. 3 Rys.2. Wartości współczynnika podziału P dla wybranych toksycznych związków organicznych Tak rozpięty zakres wartości współczynnika spowodował, że wyraża się go w formie logarytmicznej: (2) Dla tak obliczonego współczynnika podziału przyjmuje się, iż związki których log P jest mniejsze od jedności, mogą być charakteryzowane jako hydrofilowe, a więc takie, które nie ulegają bioakumulacji. Związki dla których 1 < log P < 3, charakteryzują się średnią lipofilowością i mogą ulegać częściowej bioakumulacji. Natomiast związki, których log P > 3, charakteryzują się wysoką lipofilowością i wysokim potencjałem bioakumulacji. Jest to typowa wartość współczynnika podziału dla większości tzw. trwałych zanieczyszczeń organicznych (chlorowane węglowodory, PCB, WWA, polichlorowane dibenzodioksyny i furany). Tak jak przedstawiono wcześniej, oddziaływania międzycząsteczkowe zachodzące pomiędzy substancją rozpuszczoną a n-oktanolem i wodą zależą od jej budowy chemicznej i wielkości ale też od obecności ugrupowań kwaśnych bądź zasadowych. Mając do czynienia z kwasami bądź zasadami organicznymi, kolejnym bardzo ważnym czynnikiem wpływającym na podział staje się również wartość pH układu, która determinuje stopień zjonizowania substancji rozpuszczonej. W przypadku kwasów i zasad podziałowi pomiędzy fazy ulegają nie tylko związki neutralne, ale również formy zjonizowane oraz formy zasocjowane tych związków. Dodatkowo, występowanie związku w formie zjonizowanej może stać się poważnym ograniczeniem 4 technicznym w wyznaczeniu współczynnika podziału. Jeżeli związek taki w swojej strukturze zawierałby także obszerny fragment hydrofobowy (np. kilku- lub kilkunastowęglowy łańcuch alkilowy), to swoją budową przypominałby substancję powierzchniowo czynną. Na ogół, substancje takie ulegają emulsyfikacji na granicy faz dwóch niemieszających się rozpuszczalników, co utrudnia a w zasadzie uniemożliwia wyznaczenie dla nich wiarygodnego współczynnika podziału. Na rys. 3 przedstawiono przykład podziału kwasu octowego pomiędzy oktanol i wodę z uwzględnieniem wszystkich możliwych form występowania. Rys.3. Formy występowania kwasu octowego w układzie n-oktanol – woda W fazie wodnej kwas występować będzie zarówno w formie zjonizowanej jak i obojętnej. Im większy będzie udział formy zjonizowanej, tym większa ilość cząsteczek kwasu znajdzie się w tej właśnie fazie. Oczywiście, jeżeli pH układu uległoby obniżeniu, to przeważałaby forma obojętna, a poniżej wartości 4,8 (wartość pKa dla kwasu octowego) byłaby formą dominującą. W miarę protonowania grupy karboksylowej część cząsteczek kwasu przechodzić będzie do fazy oktanolowej. Oprócz formy obojętnej w fazie n-oktanolu utworzyć się mogą także dimery kwasu octowego powstałe w wyniku asocjacji. Asocjacja ma miejsce w niepolarnych rozpuszczalnikach i określą ją stałą równowagi reakcji asocjacji. Polega ona na tworzeniu cząstek zawierających dwie lub więcej cząsteczek związanych wiązaniami wodorowymi. Strukturę dimeru kwasu octowego przedstawiono na rys. 4. Rys.4. Asocjat dwóch cząsteczek kwasu octowego Jeżeli kwas asocjuje w fazie oktanolowej, to jego współczynnik podziału pomiędzy fazę oktanolową i wodną przyjmuje następującą postać: 5 (3) gdzie n to liczba asocjujących cząsteczek. Zlogarytmowana postać tego równania to: (4) Po przekształceniu uzyskujemy równanie liniowe, gdzie log P jest punktem przecięcia prostej z osią y przy x = 0, a 1/n jest współczynnikiem kierunkowym prostej: (5) Równanie to pozwala na podstawie wykresu wyznaczyć współczynnik podziału P oraz liczbę cząsteczek n tworzących asocjaty w fazie oktanolowej. Do obliczenia log P należy analitycznie określić aktywność substancji rozpuszczonej w obydwóch fazach, co w przypadku roztworów rozcieńczonych sprowadza się do wyznaczenia stężenia. W tym celu stosuje się szereg metod np. miareczkowanie, oznaczanie kolorymetrycznie, chromatografię cieczową lub gazową. Pomiędzy log P a parametrami retencji z RP HPLC można zauważyć ścisłą zależność jeżeli układ chromatograficzny przypomina układ podziałowy n-oktanol/woda. Dlatego też współczynnik podziału można wyznaczać metodami pośrednimi, z użyciem wysokosprawnej chromatografii cieczowej (HPLC) lub metodami obliczeniowymi. 1. Metoda HPLC Hydrofobowość można zdefiniować jako tendencję danego związku do “preferowania” środowiska niewodnego względem wodnego, pojęcie to może być rozumiane jako tendencja cząsteczek związku rozpuszczonego do agregacji w roztworach wodnych. fizykochemicznych: Właściwości orientacyjnych, hydrofobowe indukcyjnych, są sumą oddziaływań dyspersyjnych, wiązania wodorowego i przeniesienia ładunku. W przypadku oddziaływań hydrofobowych siły te zależą głównie od właściwości rozpuszczalników, a nie od substancji rozpuszczonych. Od czasu wprowadzenia chromatografii cieczowej z fazami odwróconymi jest ona szczególnie odpowiednia do oznaczania hydrofobowości. W przypadku metody z wykorzystaniem HPLC zakłada się, iż retencja badanej substancji w odwróconym układzie faz odpowiada jej podziałowi pomiędzy dwie nie mieszające się fazy i jako taka jest proporcjonalna do współczynnika podziału P. W takim układzie, jedną z faz (faza stacjonarna) stanowią ziarna krzemionki chemicznie zmodyfikowane warstwą hydrofobową złożoną z podstawników n-alkilowych o różnej długości łańcucha (C8 – 6 C18), natomiast drugą fazę (faza ruchoma) stanowi polarny rozpuszczalnik, na ogół mieszanina wody i metanolu. Podstawowa zaleta oznaczania hydrofobowości tą metodą to możliwość użycia modyfikatorów organicznych jako składników binarnych (dwuskładnikowych) eluentów. Jednak obecność modyfikatora organicznego powoduje podniesienie stopnia skomplikowania natury oddziaływań wpływających na rozdział chromatograficzny. Przy zastosowaniu ustalonego składu eluentu badany związek może okazywać się bardziej hydrofobowy niż inny związek, podczas gdy sytuacja taka może przedstawiać się odwrotnie przy innym składzie eluentu. Dlatego też stosuje się metodę polegającą na wykreśleniu log k względem procentowej objętościowej zawartości modyfikatora. W trakcie przemieszczania się przez kolumnę chromatograficzną badana substancja ulega podziałowi pomiędzy hydrofobową warstwą w fazie stacjonarnej a polarnym rozpuszczalnikiem w fazie ruchomej. Podobnie jak to ma miejsce w metodzie wyznaczania równowagowego współczynnika podziału pomiędzy oktanolem a wodą, im bardziej substancja będzie lipofilową tym większe będzie jej powinowactwo do stacjonarnej fazy hydrofobowej. W praktyce oznacza to, iż w układzie chromatograficznym substancja taka będzie dłużej zatrzymywana, a więc wzrastać będzie jej czas retencji. Dla dużej grupy związków chemicznych wykazano liniową zależność pomiędzy czasem retencji a współczynnikiem podziału wg następującego równania: (6) przy czym a i b są charakterystyczne dla danej grupy związków (homologów, kongenerów, izomerów itp.). Rys. 5 przedstawia tę korelację dla wybranych związków aromatycznych, których współczynnik podziału mieści się w szerokim zakresie 4 rzędów wielkości. Najprostszym, praktycznym zastosowaniem tej metody jest wyznaczenie kilkunastu współczynników retencji dla grupy związków referencyjnych, o znanych współczynnikach podziału a następnie, w oparciu o uzyskaną korelację szacowanie tych współczynników dla związków nieznanych na podstawie ich czasów retencji w tych samych warunkach chromatograficznych. 7 Rys.5. Linowa zależność pomiędzy współczynnikiem retencji log P a czasem retencji log t R Należy jednak zauważyć, iż pomiędzy współczynnikiem podziału n-oktanol/woda a współczynnikiem wyznaczonym metodą chromatograficzną występuje różnica w składzie faz. O ile można przyjąć, iż stacjonarna faza hydrofobowa oraz wolne ugrupowania silanolowe na powierzchni krzemionki przypominają do pewnego stopnia strukturę n-oktanolu (rys. 6), o tyle faza polarna zawiera nie tylko wodę lecz również modyfikator organiczny jakim jest metanol. Powoduje to, że układ chromatograficzny zawiera dodatkowy czynnik wpływający na rozpuszczalność, a tym samym na podział badanej substancji, co zwłaszcza przy wysokiej zawartości metanolu może poważnie zakłócić omawianą korelację. Rys.6. Porównanie chromatograficznej fazy odwróconej i n-oktanolu Logicznym wydałoby się więc użycie czystej wody jako fazy ruchomej. Jest to jednak niemożliwe w odwróconym układzie faz, w którym silnie uwodnione układy wywołują efekt „kładzenia” się podstawników alkilowych, co znacznie ogranicza sprawność kolumny chromatograficznej (rys. 7). 8 Rys.7. Porównanie struktury hydrofobowej fazy stacjonarnej w przypadku użycia czystej wody (A) oraz wody z metanolem (B) jako faz ruchomych Dlatego do chromatograficznego wyznaczania współczynnika podziału stosuje się metodę ekstrapolacyjną. W skrócie, polega ona na wyznaczeniu czasów (współczynników) retencji badanego związku dla kilku faz ruchomych o różnej zawartości metanolu i wykreśleniu powstałej zależności według następującego, liniowego równania: (7) nazywanego równaniem Snydera-Soczewińskiego, które jest jedną z podstawowych zależności w chromatografii w odwróconym układzie faz. W równaniu, k to współczynnik retencji (lub współczynnik objętościowy) wyznaczony z zależności: k = (tR – t0)/t0 (8) gdzie t0 to czas martwy układu; kw to wartość współczynnika retencji odpowiadająca fazie zawierającej wyłącznie wodę (0% metanolu). Z podanych powyżej ograniczeń wartość tę wyznacza się ekstrapolując wyniki uzyskane dla faz zawierających metanol do punktu przecięcia z osią y. Stąd, log kw uznaje się za chromatograficzny współczynnik podziału (odpowiadający podziałowi pomiędzy wodę a fazę hydrofobową). S to nachylenie wykreślonej prostej, charakterystyczne dla badanego związku a φ to udział metanolu w fazie ruchomej (%). Rys. 8 przedstawia opisaną zależność. Rys.8. Zależność Snydera – Soczewińskiego, z której wyznacza się chromatograficzny współczynnik podziału log kw 9 W metodzie HPLC substancje o bardzo niskiej rozpuszczalności w n-oktanolu wykazują tendencję do dawania zaniżonych wartości log P. Piki takich związków czasem towarzyszą czołu rozpuszczalnika. Dzieje się tak dlatego, iż w takiej sytuacji proces podziału jest zbyt powolny do uzyskania równowagi w czasie branym pod uwagę przy zwykłym rozdzielaniu metodą HPLC. Zmniejszenie szybkości przepływu i/lub obniżenie stosunku metanol/woda może być w tym przypadku pożądane, aby uzyskać rzeczywistą wartość. Wartość pH eluentu jest krytyczna dla związków ulegających jonizacji. Powinno być ono w obrębie zakresu roboczego pH kolumny, które zwykle wynosi między 2 i 8. Zalecane jest buforowanie. Należy zachować ostrożność, aby nie dopuścić do wytrącania się soli i zniszczenia kolumny, co zachodzi dla niektórych mieszanin faza organiczna/bufor. Pomiary HPLC faz stacjonarnych opartych na krzemionce powyżej pH 8 nie są polecane, gdyż użycie zasadowej fazy ruchomej powoduje gwałtowne pogorszenie się wydajności kolumny. Warto dodać, iż prowadzono badania nad użyciem wypełnień innych, niż oparte na chemicznie związanej krzemionce. Przebadano między innymi następujące wypełnienia: kopolimery poli(styrenodiwinylobenzenowe), kopolimer oktadecylopoliwinylowy, tlenek glinowy, tlenek cyrkonowy, oraz niedawno wprowadzony materiał do pakowania kolumn tzw. immobilizowana sztuczna membrana (IAM). W przypadku ODS proponuje się modyfikację fazy stacjonarnej bądź też ruchomej polegającej na np.: zastosowaniu pH od 2,5 do 3,5 i wyższych stężeń buforu, zastąpienie soli sodowych potasowymi i dodatek modyfikatorów aminowych (dimetylooktyloamina, trimetyloamina), dodanie oktanolu i decylaminy do fazy ruchomej składającej się między innymi z MeOH. Jednak nie istnieje sposób który umożliwiałby uczynienie układu RP HPLC identycznym z układem n-oktanol/woda. 2. Metody obliczeniowe Wszystkie metody obliczeniowe są oparte o formalną fragmentację cząsteczki na odpowiednie podstruktury dla których pewne przyrosty wartości log P są znane z eksperymentu. Wartość log P całej cząsteczki jest następnie obliczana jako suma wartości odpowiadająca jej fragmentom plus suma składników korekcji dla oddziaływań wewnątrzcząsteczkowych. Wiarygodność metod obliczeniowych obniża się ze wzrostem złożoności badanych związków. W przypadku prostych cząsteczek o niskiej masie cząsteczkowej i jednej lub dwu grupach funkcyjnych, można oczekiwać odchylenia od 0,1 do 0,3 jednostek log P między wynikami różnych metod fragmentaryzacji i 10 wartościami zmierzonymi. Jedną z pierwszych stosowanych półempirycznych metod obliczeniowych była metoda stałej podstawienia hydrofobowego π, definiowaną jako: (9) gdzie P (PhX) jest współczynnikiem podziału pochodnej aromatycznej, a P (PhH) związku macierzystego. Metoda stosowana jest głównie dla podstawienia aromatycznego. Wartości dla większej liczby podstawników zostały stabelaryzowane w licznych pozycjach literaturowych. Są one stosowane dla obliczeń log P cząsteczek aromatycznych lub podstruktur. Stosuje się również metodę Rekkera w której wartość log P jest obliczana z następującej zależności: (10) gdzie fi reprezentuje różne stałe fragmentów cząsteczki, natomiast ai, częstotliwość ich występowania w badanej cząsteczce. Składniki korekcji są wyrażone jako całkowita wielokrotność pojedynczej stałej Cj. Stałe fragmentu fi, i Cj zostały ustalone z wykazu z ponad tysiąca doświadczalnych wartości współczynnika podziału P. Dla prostych cząsteczek, równanie przyjmuje uproszczoną postać, gdzie suma składników korekcji wynosi 0,229: (11) Najbardziej zaawansowanym sposobem wyznaczania współczynnika podziału jest metoda Hansch-Leo zgodnie z którą wartość log P jest obliczana z: (12) gdzie fi przedstawia różne stałe fragmentu cząsteczkowego, Fj składniki korekcji oraz ai, bi odpowiadające częstotliwości występowania. Wyprowadzony z doświadczalnych wartości współczynników podziału wykaz atomowych i cząsteczkowych grup wartości, oraz wykaz składników korekcji Fj zostały ustalone metodą prób i błędów. Składniki korekcji zostały uporządkowane w kilka różnych klas. Wzięcie pod uwagę wszystkich zasad i składników korekcji jest względnie skomplikowane i zużywające czas. Dlatego współcześnie istnieje szereg programów komputerowych obliczających lipofilowość związku na podstawie zadanej struktury. 11 Celem ćwiczenia jest wyznaczanie współczynnika podziału oktanol/woda wybranych związków organicznych o działaniu toksycznym techniką wysokosprawnej chromatografii cieczowej oraz metodą obliczeniową. Odczynniki: metanol cz. HPLC, woda cz. HPLC, wodny roztwór fenolu (1 mmol/dm3), wodny roztwór o-nitrofenolu (1 mmol/dm3) Sprzęt laboratoryjny i aparatura pomiarowa: chromatograf HP 1050 z detektorem UV-Vis i pętlą nastrzykową o objętości 20 mm3, kolumna chromatograficzna oktadecylosilanowa ODS (RP-18) 125x4 mm, 5 m. SPOSÓB WYKONANIA 1. Wyznaczyć czas martwy teoretyczny układu chromatograficznego ze wzoru: Vm , F t0 gdzie: Vm - martwa objętość kolumny (objętość fazy ruchomej w kolumnie) w cm3, F - przepływ przez kolumnę w cm3/min. Martwą objętość kolumny można wyznaczyć z przybliżonego wzoru: Vm 0,5 L dc2 , gdzie: L - długość kolumny w cm, dc - wewnętrzna średnica kolumny w cm. 2. Przeprowadzić rozdzielenie chromatograficzne roztworów fenolu i o-nitrofenolu o stężeniach 1 mmol/dm3 w trzech układach elucyjnych metanol–woda: 50:50, 60:40, 70:30 (v/v) przy przepływie 0,8 cm3/min. Detekcję przeprowadzić przy długości fali 278 nm. Dla każdej z faz ruchomych należy wykonać nastrzyk po 25-30 μL każdego z roztworów i określić czasy retencji badanych związków. Na ich podstawie wyznaczyć współczynniki retencji k. 3. W trakcie wykonywania analiz należy obliczyć współczynniki podziału dla związków z Tabeli 1. 12 W tym celu należy skorzystać z programu EpiSuite, udostępnionego przez US EPA. Po otwarciu programu wybieramy po lewej stronie okna moduł KOWWIN, w kolejnym oknie NameLookup, w kolejnym wpisujemy nazwę związku i potwierdzamy OK. W otwartym oknie wyboru potwierdzamy nasz wybór lub wyszukujemy na liście żądany związek. W uzupełnionym o dane związku oknie programu KOWWIN wybieramy Calculate. Wyniki: przewidywany współczynnik podziału (w czerwonej ramce) oraz wartość literaturową (Exp Log P) wpisujemy do tabeli. Jeśli brakuje wartości eksperymentalnej, pozostawiamy wolne miejsce. Program KOWWIN wykorzystuje do obliczeń algorytm identyczny z opisanym w ćwiczeniu. Tabela 1. Wartości eksperymentalne i przewidywane dla szeregu homologicznego kwasów karboksylowych Liczba atomów węgla Nazwa 2 acetic acid 6 hexanoic acid 10 decanoic acid 14 tetradecanoic acid 20 eicosanoic acid 24 tetracosanoic acid 28 octacosanoic acid 32 dotriacontanoic acid log P log P obliczony eksperymentalny 13 OPRACOWANIE WYNIKÓW 1. Należy wykreślić zależność log k od procentowego udziału MeOH w fazie ruchomej zgodnie z równaniem Snydera-Soczewińskiego i odczytać wartość log kw. 2. Dla analizowanych związków należy obliczyć współczynniki podziału korzystając z równania (11) oraz stałych fi fragmentów cząsteczkowych zawartych w Tabeli 2. Tabela 2. Wartości stałych fi fragmentów cząsteczkowych Fragment 3. fi alifatyczny –CH3 0,5473 alifatyczny –CH2 - 0,4911 aromatyczny C lub CH 0,2940 Br- (połączony z aromatem) 0,8900 Cl- (połączony z aromatem) 0,6445 OH- (połączony z aromatem) -0,4802 aromatyczny –NH2 -0,9170 aromatyczny –NO2 -0,1823 Na podstawie uzupełnionej Tabeli 1 wykonać na jednym rysunku wykresy zależności log P eksperymentalnego oraz log P przewidywanego (y) od liczby atomów węgla w cząsteczce (x). Czy przebieg obu zależności jest liniowy? Dokonaj ekstrapolacji uzyskanej zależności przewidywanej dla kwasów o 35 i 40 atomach węgla w cząsteczce. Instrukcja opracowana na podstawie: Chemia fizyczna, Pigoń K., Podstawy chromatografii, Witkiewicz Z., Fizykochemiczne metody analizy w chemii środowiska, red. B. Buszewski, P. Kosobucki, Ćwiczenia laboratoryjne z chemii wody, B. i E. Gomółkowie. Opracowali: B. Krawczyk, D. Szczukocki 14