PDF file
Transkrypt
PDF file
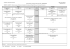
Biosensoryczne właściwości nanocząstek półprzewodnikowych Bożena Sikora Promotor: prof. Danek Elbaum Zespół Fizyki Biologicznej Instytut Fizyki Polskiej Akademii Nauk 1 Cel badań Wczesne wykrywanie chorób neurodegeneracyjnych (choroba Alzheimera, choroba Parkinsona) Choroby neurodegeneracyjne grupa wrodzonych lub nabytych postępujących chorób układu nerwowego, w których podstawowym zjawiskiem patologicznym jest utrata komórek nerwowych. W wyniku procesu chorobowego dochodzi do wystąpienia szeregu uszkodzeń neurologicznych (np. uszkodzenia związane z funkcją motoryczną, uszkodzenia związane z pamięcią). Proces prowadzący do wystąpienia objawów choroby neurodegeneracyjnej rozpoczyna się znacznie wcześniej i przebiega przez długi czas (często latami) bezobjawowo. Pierwsze objawy pojawiają się kiedy znacząca ilość neuronów ulegnie uszkodzeniu lub uszkodzenie dotyczy określonej części ośrodkowego układu nerwowego. Neurony – komórki nie dzielące się Brak diagnostyki na wczesnym etapie rozwoju choroby, dlatego brak jest skutecznych leków 2 Koloidalne nanocząstki półprzewodnikowe (nanokryształy, kropki kwantowe) • kryształy o rozmiarach nanometrowych • ograniczenia kwantowe (quantum confinement effect) Rysunek: W. H. Suh, Suh, K. S. Suslick, Suslick, G. D. Stucky, Stucky, Y. H. Suh, Suh, Progress in Neurobiology, 2009, 87, 133133-170. • interesujące właściwości optyczne ¾ możliwość regulowania długości fali luminescencji poprzez rozmiar ¾ duży współczynnik ekstynkcji ¾ wysoka wydajność kwantowa ¾ duży stosunek powierzchni do objętości ¾ brak fotowybielania (utrata zdolności do luminescencji po wyemitowaniu określonej liczby fotonów) Wady: brak specyficzności w systemach biologicznych, niska czułość na środowisko = brak „inteligencji” biologicznej Rysunek: W. H. Suh, Suh, K. S. Suslick, Suslick, G. D. Stucky, Stucky, Y. H. Suh, Suh, Progress in Neurobiology, 2009, 87, 133133-170. 3 „Inteligencja” koloidalnych nanocząstek półprzewodnikowych Pokrywanie nanocząstek związkami organicznymi • stabilizacja przeciw agregacji • modyfikacja właściwości powierzchni (hydrofobowe, hydrofilowe, amfifilowe) • Grupy funkcyjne wykorzystywane do przyłączania innych molekuł (np. molekuł biologicznie aktywnych) Nanocząstka (5 nm) pokryta różnymi hydrofilowymi ligandami: MAA (kwas merkaptooctowy), MPA (kwas merkaptopropionowy), MUA (kwas merkaptoundekanowy), MSA (kwas merkaptobursztynowy) DHLA (kwas dihydroliponowy), Nanocząstka (5 nm) pokryta różnymi hydrofobowymi ligandami: TOPO (tlenek bis-sulfonowana trifenylofosfina, mPEG5-SH, mPEG45SH (2000 g/mol), krótki peptyd (CALNN) trioktylofosfiny),TPP (trifenylofosfina), DDT (dodekanotiol), TOAB (bromek tetrabutyloamoniowy) R. A. Sperling, Surface Modification and Functionalization of Colloidal Nanoparticles, 2008, Marburg 4 „Inteligencja” koloidalnych nanocząstek półprzewodnikowych Przyłączanie biologicznie aktywnych molekuł nadaje biologiczną „inteligencję” • • • • • • • lipidy (składniki błon komórkowych) witaminy peptydy cukry białka (np. przeciwciała) enzymy DNA i RNA Nanocząstka (5 nm) pokryta warstwą organiczną (10 nm) z aktywnymi grupami, do których mogą być przyłączone: molekuły poliglikolu etylenowego PEG (2000 g/mol), PEG (5000 g/mol), streptoawidyna, transferyna, przeciwciało (IgG), albumina, pojedyncza nić DNA R. A. Sperling, Surface Modification and Functionalization of Colloidal Nanoparticles, 2008, Marburg 5 Toksyczność koloidalnych nanocząstek półprzewodnikowych Toksyczność nanocząstek półprzewodnikowych CdSe/ZnS: ¾ wysoka toksyczność spowodowana dysocjacją metali ciężkich[1],[2] powodujących śmierć komórek Toksyczność nanocząstek metali (Ag, Au) ¾ średnia toksyczność spowodowana przyłączaniem się do nici DNA[3] Toksyczność nanocząstek tlenków i nanocząstek polimerowych ¾ najmniejsza → rozpadają się całkowicie w ciele, sugerując, że są one najbardziej biokompatybilne [4],[5] [1] E. Chang, E. Thekkek, W. W. Yu, V. L. Colvin, R. Drezek, Small, 2006, 2, 1412–1417, [2] A. M. Derfus, W. C. W. Chan, S.N. Bhatia, Nano Lett. 2004, 4, 11–18, [3] M. Tsoli, H. Kuhn, W. Brandau, H. Esche, G. Schmid, Small, 2005, 1(8-9), 841-844, [4] R. Weissleder, D. Stark, B. L. Engelstad, B. R. Bacon, C. C. Compton, D. L. White, P. Jacobs, J. Lewis, American Journal of Roentgenology, 1989, 152, 167-173, [5] E. I. Altinoglu, T. J. Russin, J. M. Kaiser, B. M. Barth, B. C. Eklund, M. Kester, J. H. Adair, ACS Nano, 2008, [6] D. R. Cooper, J. L. Nadeau, Nanoscale, 2009 Nanocząstki CdSe z przyłączoną molekułą biologiczną, specyficzną dla danego receptora: • mogą być rozłożone do nanocząstek i biomolekuł przed przyłączeniem się receptora. Takie CdSe mogą uwalniać jony Cd2+, które są pochłaniane przez komórkę. • rozkład kompleksu może zachodzić wewnątrz komórki, gdzie są uwalniane jony Cd2+ • jony Cd2+ i biologiczne cząsteczki mogą wchodzić do jądra komórkowego [6] • jony Cd2+ wiążą się z atomami siarki, tlenu i wodoru zmieniając strukturę elementów komórki • jony Cd2+ zaburzają obieg mikroelementów: Fe, Cu, Mg, Ca, Se, Zn 6 Dlaczego nanocząstki ZnO i Fe2O3? 1. Niska toksyczność 33,6 mg/kg Cd2+/mysz 1,9 g/kg Zn2+/mysz Zaleznosc smiertelnosci myszy od dawki jonów Cd2+ Zaleznosc smiertelnosci myszy od dawki jonów Zn2+ Jung D. Park et.al., Toxicology, 2001, 163, 93–100 2. Ciekawe właściwości optyczne nanocząstek ZnO i magnetyczne nanocząstek Fe2O3 3. Bardzo wydajna, niedroga, „łatwa” i bezpieczna procedura otrzymywania w koloidach 7 Właściwości luminescencyjne Trap State h Pasmo walencyjne Długość fali [nm] Pasmo wzbronione Pasmo przewodnictwa e Nanocząstki ZnO mają dwa pasma emisyjne: - Wąskie pasmo emisji ekscytonowej przy długości fali około 380 nm, - Szerokie , intensywne pasmo przy długości fali około 535 nm przypisane stanom defektowym (trap state) np. luki tlenowe. N. S. Norberg, D. R. Gamelin, J. Phys. Chem. B, 109, 2005, 20810-20816. 8 Dalszy wzrost nanocząstek ZnO w roztworach 0,6 7,0E+05 po syntezie po 21 h 5,0E+05 po 45h 0,4 Emisja po 672 h 0,3 0,2 po 100 min po 21h po 45h 4,0E+05 3,0E+05 2,0E+05 0,1 1,0E+05 0 300 350 400 450 500 0,0E+00 375 Długość fali [nm] 425 475 525 długość fali [nm] 575 Widma absorbancji i luminescencji nanocząstek ZnO otrzymanych z octanu cynku (1 mM) oraz wody (407 mM) w temperaturze 35 °C w izopropanolu w zależności od czasu przechowywania. 10 9,5 9 8,5 2R [nm] Absorbancja 0,5 6,0E+05 Wykres zależności promienia nanocząstek ZnO od czasu ich przechowywania w temperaturze pokojowej. 8 7,5 7 6,5 6 5,5 5 0 10000 20000 30000 czas [min] 40000 50000 Synteza nanocząstek ZnO/MgO rdzeń/powłoka Zn(OAc)2*2H2O w alkoholu Dodanie H2O lub NaOH w alkoholu (CH3COO)2Zn → 2CH3COO- + Zn2+ H2O ↔ H+ + OH- or NaOH → Na+ + OHZn2+ + 2OH- ↔ Zn(OH)2 ↔ ZnO + H2O ZnO Dodanie Mg(OAc)2*4H2O w alkoholu i NaOH ZnO ZnO/MgO rdzeń/powłoka (CH3COO)2Mg → 2CH3COO- + Mg2+ NaOH → Na+ + OHMg2+ + 2OH- ↔ Mg(OH)2 ↔ MgO + H2O 10 Dlaczego powłoka MgO? 1. Doświadczalnie wykazano zapobieganie dalszego wzrostu nanocząstek ZnO [1] – potwierdzenie B. Sikora 2. Jest nietoksyczna i biokompatybilna 3. Powoduje znaczny wzrost luminescencji pochodzącej od defektów rdzenia ZnO [1][2] i wzrost luminescencji ekscytonowej rdzenia ZnO [2] MgO 2,56 eV ZnO EC EgMgO = 7,8 eV EgZnO = 3,44 eV Ev -1,74 eV Heterozłącze I rodzaju systemu rdzeń/powłoka: 1). Minimum poziomu przewodnictwa powłoki ma energię wyższą niż energia poziomu przewodnictwa rdzenia 2). Maksimum poziomu walencyjnego powłoki ma energię niższą niż energia poziomu walencyjnego rdzenia 3). W tym systemie ekscyton jest ograniczony do materiału rdzenia, powłoka pasywuje defekty odpowiadające za przejścia niepromieniste na powierzchni ZnO i przeciwdziała narażeniu ekscytonu na środowisko zewnętrzne [1] J. Lee, J. Bang, H. Yang, J. Phys. D: Appl. Phys. 2009, 42, 1-6, [2] X. Q. Meng, H. Peng, Y. Q. Gai, J. Li J. Phys. Chem. C, 11 2010, 114 (3), 1467–1471 Charakteryzacja nanocząstek ZnO/MgO rdzeń/powłoka Absorbancja 0,6 Wykresy zależności absorbancji i emisji nanocząstek ZnO/MgO w wodzie w zależności od czasu przechowywania (stosunek Mg/Zn wynosi 37 %). ZnO/MgO in H2O ZnO/MgO 21 days in H2O ZnO/MgO 42 days in H2O 0,5 0,4 0,3 0,2 0,1 0 300 350 400 450 500 550 długość fali [nm] Luminescencja 2,E+06 600 Średnia średnica nanocząstek ZnO/MgO core/shell wyznaczona z początku widm absorbancji korzystając z przybliżenia masy efektywnej. ZnOMgO in H2O ZnOMgO 21 days in H2O 1,E+06 t [dni] ZnOMgO 42 days in H2O rozpuszczone w wodzie 8,E+05 2R [nm] 6,2 4,E+05 21 5,9 0,E+00 42 5,9 366 416 466 516 566 długość fali [nm] 12 Pomiar AFM Pomiar TEM Histogram 100 C ounts 80 60 40 20 0 1,5 2,0 2,5 3,0 3,5 4,0 4,5 5,0 5,5 6,0 6,5 7,0 2R [nm] Pomiar X-Ray ZnO /M gO 18000 Intensity (arb. units) 16000 002 101 100 14000 12000 0.9λ t= B cos θ t – średnica cząstki (Å) λ – długość fali (1,54 Å) B – szerokość połówkowa (radiany) 10000 8000 110 102 103200 6000 4000 2000 0 0 20 40 60 80 o 2θ ( ) 100 120 2RX-ray [nm] 2Ropt [nm] 2RTEM [nm] 2RAFM [nm] ~7.9 ~6.0 ~5,5 ~5,4 13 Ale po co to wszystko? Trzy strategie budowania biosensorów: 1. Fluorescencyjny Rezonansowy Transfer Energii (FRET) między nanocząstką ZnO a barwnikiem organicznym czułym na środowisko zewnętrzne 2. Biosensor optyczno – magnetyczny do wykrywania krótkich oligomerów β-amyloidu (wczesne wykrywanie choroby Alzheimera) 3. FRET między nanocząstką ZnO pokrytą przeciwciałem a białkiem do którego zostaje przyłączona 14 Ale po co to wszystko? Trzy strategie budowania biosensorów: 1. Fluorescencyjny Rezonansowy Transfer Energii (FRET) między nanocząstką ZnO a barwnikiem organicznym czułym na środowisko zewnętrzne 2. Biosensor optyczno – magnetyczny do wykrywania krótkich oligomerów β-amyloidu (wczesne wykrywanie choroby Alzheimera) 3. FRET między nanocząstką ZnO pokrytą przeciwciałem a białkiem do którego zostaje przyłączona 15 Pierwsza strategia budowania biosensorów Fluorescencyjny Rezonansowy Transfer Energii (FRET) między nanocząstką ZnO a barwnikiem organicznym czułym na środowisko zewnętrzne FRET – Fluorescence Resonance Energy Transfer mechanizm przenoszenia energii między dwoma chromoforami na drodze innej niż promieniowanie. Donor w stanie wzbudzonym może przekazywać energię wzbudzenia akceptorowi znajdującemu się w odległości nie większej niż 10 nm. Obraz TEM i histogram wielkości ZnO/MgO S. Rakshit et al., ACS Nano, vol. 2, no. 7, 2008, 1473-1479 Data: Count1_Count Model: Gauss Equation: y=y0 + (A/(w*sqrt(PI/2)))*exp(-2*((x-xc)/w)^2) Weighting: y No weighting Chi^2/DoF = 22.43883 R^2 = 0.94944 liczba czastek 40 y0 xc w A 0.27333 5.26222 2.63185 150.47841 ±2.61713 ±0.11411 ±0.29893 ±20.78988 30 20 10 0 4 6 8 rozmiar czastek [nm] 10 16 FRET: nanocząstka ZnO/MgO rdzeń/powłoka pokryta CMCD (donor) i Czerwień Nilu (akceptor) Schemat syntezy nanocząstek ZnO/MgO pokrytych karboksymetylobeta-cyklodekstryną. β – cyklodekstryna - składa się z 7 merów glukozowych tworzących strukturę cykliczną - wnętrze otworu – hydrofobowe - całość cząsteczki - hydrofilowa - tworzy kompleksy inkluzyjne typu „gość – gospodarz” (funkcja gospodarza) 1). Zmiana rozpuszczalności nanocząstek w wodzie (zwiększenie hydrofilowości) 2). Nie zmienia absorpcji i emisji nanocząstek ZnO/MgO S. Rakshit et al., ACS Nano, vol. 2, no. 7, 2008, 1473-1479 17 1,0E+07 9,0E+06 ZnO/MgO/CMCD 0,16uM NR 0,40 uM N R 0,81 uM NR 1,6 uM NR 3,2 uM NR 6,4 uM NR 9,7 uM NR 13 uM NR 16 uM NR 19 uM NR 23 uM NR 26 uM NR 29 uM NR 32 uM NR 35 uM NR 39 uM NR 42 uM NR 45 uM NR 48 uM NR 8,0E+06 6,0E+06 5,0E+06 4,0E+06 3,0E+06 2,0E+06 FRET: ZnO/MgO/CMCD Æ Czerwień Nilu 1,0E+06 0,0E+00 420 470 520 570 620 670 długość fali [nm] 1,4E+06 ZnO/MgO/CMCD 3,2 uM NR 1,2E+06 0,060 g/l ZnO/MgO + Nile Red ex: 356 nm Tło 6,4 uM NR 9,7 uM NR 13 uM NR 16 uM NR 1,0E+06 luminescencja luminescencja 7,0E+06 4 g/l ZnO/MgO/CMCD + Nile Red ex: 356 nm 19 uM NR 23 uM NR 8,0E+05 26 uM NR 29 uM NR 32 uM NR 6,0E+05 35 uM NR 39 uM NR 42 uM NR 45 uM NR 4,0E+05 48 uM NR 2,0E+05 0,0E+00 420 470 520 570 dlugosc fali [nm] 620 67018 FRET: ZnO/MgO/CMCD i Czerwień Nilu 1 0,9 Q= Wydajnosc RET 0,8 0,7 I ZnO − I ZnO − NR I ZnO r = 3,4 nm. 0,6 0,5 0,4 nR06 Q= nR06 + r 6 0,3 0,2 0,1 exp teor 0 0 0,01 0,02 0,03 0,04 0,05 Nile Red / ZnO/MgO IZnO – intensywność luminescencji donora ZnO/MgO/CMCD w wodzie w przypadku braku Czerwieni Nilowej IZnO-NR - intensywność luminescencji donora ZnO/MgO/CMCD w wodzie w obecności różnych stężeń Czerwieni Nilowej (stężenie donora jest stałe) r – odległość między donorem a akceptorem R0 – krytyczna odległość (promień Forster’a), przy której transfer i spontaniczny zanik ekscytowanego donora są równie prawdopodobne, kZnO-NR = τZnO-1. 19 Wpływ temperatury na wydajność FRET 0,6 45 Wydajnosć RET 0,5 45 45 45 20 0,4 20 20 0,3 20 20 0,2 Q= I ZnO − I ZnO − NR I ZnO 0,1 0 temperatura [0C] Q – efektywność FRET IZnO – intensywność ZnO/MgO/CMCD w danej temperaturze IZnO-NR – intensywność ZnO w układzie ZnO/MgO/CMCD/NR 20 Wpływ temperatury na położenie piku luminescencji Czerwieni Nilu 653 79 mg/l ZnO/MgO 20 g/l ZnO/MgO/CMCD 13uM Nile Red 652 λ max [nm] 651 650 649 648 647 646 645 644 15 20 25 30 35 40 temperatura [0C] 45 50 55 21 ZnO/MgO/CMCD/Czerwień Nilu w komórkach HeLa Pobudzenie 560 nm Emisja 450 – 700 nm Pobudzenie 488 nm Autofluorescencja Emisja 520 – 560 nm Nalożenie Skład: 20 g/l ZnO/MgO/CMCD (w tym 79 mg/l ZnO/MgO) i 13 umol/l Czerwieni Nilowej w wodzie Do komórek HeLa zostało dodane 20 ul roztworu kompleksu Inkubacja 48 h z lipofektaminą 22 ZnO/MgO/CMCD/Czerwień Nilu w komórkach HeLa yz xz 23 Widma luminescencji pobudzenie 560 nm w zależnosci od miejsca na/w komórce HeLa 140 200 poza komórkami HeLa 160 luminescencja 100 luminescencja w komórkach HeLa 180 120 80 60 40 140 120 100 80 60 40 20 20 0 0 500 550 600 650 700 750 800 500 550 600 dlugosc fali [nm] 0,045 na komórkach HeLa 750 800 750 800 komórki HeLa bez ZnO/MgO/CMCD/NR 0,04 0,8 0,035 0,7 luminescencja luminescencja 700 dlugosc fali [nm] 1 0,9 650 0,6 0,03 0,025 0,5 0,4 0,02 0,015 0,3 0,01 0,2 0,005 0,1 0 0 500 550 600 650 700 dlugosc fali [nm] 750 800 500 550 600 650 700 dlugosc fali [nm] 24 Zestawienie λ max ± SD poza komórką λ max ± SD na komórce λ max ± SD w komórce 600 ± 3 nm 597 ± 9 nm 619 ± 3 nm I max poza komórką I max na komórce I max w komórce 23 – 120 arb. units 0,47 – 0,87 arb. units 54 – 167 arb. units 25 Widma luminescencji pobudzenie 560 nm Komórki bez ZnO/MgO/CMCD/NR 0,045 0,04 luminescencja 0,035 0,03 0,025 0,02 0,015 0,01 0,005 0 500 550 600 650 700 750 800 dlugosc fali [nm] Autofluorescencja komórek Pobudzenie 405 nm 26 ZnO/MgO/CMCD/Czerwień Nilu w komórkach HeLa Filtr pobudzający: 377 ± 25 nm Filtr emisyjny: 593 ± 20 nm FRET Filtr pobudzający: 377 ± 25 nm Filtr emisyjny: 536 ± 20 nm ZnO + autofluorescencja Filtr pobudzający: 377 ± 25 nm Filtr emisyjny: red FRET Filtr pobudzający: 482 ± 17 nm Filtr emisyjny: 536 ± 20 nm autofluorescencja 27 ZnO/MgO/CMCD/Czerwień Nilu w komórkach HeLa Filtr pobudzający: 377 ± 25 nm Filtr emisyjny: 593 ± 20 nm 28 ZnO/MgO/CMCD/Czerwień Nilu w komórkach HeLa Filtr pobudzający: 377 ± 25 nm Filtr emisyjny: red 29 Komórki HeLa - kontrola Filtr pobudzający: 377 ± 25 nm Filtr emisyjny: 593 ± 20 nm Filtr pobudzający: 377 ± 25 nm Filtr emisyjny: red Filtr pobudzający: 377 ± 25 nm Filtr emisyjny: 536 ± 20 nm Filtr pobudzający: 377 ± 25 nm Filtr emisyjny: 692 ± 20 nm 30 Kolejny etap: Zmiana sondy (Czerwień Nilu) na sondę czułą na rodniki Æ znaczenie w chorobach neurodegeneracyjnych 31 Ale po co to wszystko? Trzy strategie budowania biosensorów: 1. Fluorescencyjny Rezonansowy Transfer Energii (FRET) między nanocząstką ZnO a barwnikiem organicznym czułym na środowisko zewnętrzne 2. Biosensor optyczno – magnetyczny do wykrywania krótkich oligomerów β-amyloidu (wczesne wykrywanie choroby Alzheimera) 3. FRET między nanocząstką ZnO pokrytą przeciwciałem a białkiem do którego zostaje przyłączona 32 Druga strategia budowania biosensorów Biosensor optyczno – magnetyczny do wykrywania krótkich oligomerów β-amyloidu (wczesne wykrywanie choroby Alzheimera) Cząsteczki Analit Przeciwciało do analitu Nanocząstka ZnO (właściwości emisyjne) Nanocząstka Fe2O3 (właściwości magnetyczne) 33 Druga strategia budowania biosensorów Nanocząstki ZnO/MgO Cząsteczki Analit Przeciwciało do analitu Nanocząstka ZnO (właściwości emisyjne) Nanocząstka Fe2O3 (właściwości magnetyczne) 34 Druga strategia budowania biosensorów Cząsteczki Analit Przeciwciało do analitu Nanocząstka ZnO (właściwości emisyjne) Nanocząstka Fe2O3 (właściwości magnetyczne) 35 Druga strategia budowania biosensorów Nanocząstki Fe2O3 Cząsteczki Analit Przeciwciało do analitu Nanocząstka ZnO (właściwości emisyjne) Nanocząstka Fe2O3 (właściwości magnetyczne) 36 Druga strategia budowania biosensorów Cząsteczki Analit Przeciwciało do analitu Nanocząstka ZnO (właściwości emisyjne) Nanocząstka Fe2O3 (właściwości magnetyczne) 37 Druga strategia budowania biosensorów Magnes Cząsteczki Analit Przeciwciało do analitu Nanocząstka ZnO (właściwości emisyjne) Nanocząstka Fe2O3 (właściwości magnetyczne) 38 Druga strategia budowania biosensorów Detekcja luminescencji nanocząstek ZnO/MgO Magnes Cząsteczki Analit Przeciwciało do analitu Nanocząstka ZnO (właściwości emisyjne) Nanocząstka Fe2O3 (właściwości magnetyczne) Zalety: -) możliwość wykonywania testów w warunkach polowych -) nie potrzebny jest wysublimowany sprzęt laboratoryjny 39 Nanocząstki Fe2O3 Właściwości strukturalne Potwierdzenie romboedrycznej struktury Fe2O3 (hematyt) Pomiar X-Ray przed wygrzewaniem o Fe2O 3 (po wygrzaniu w 400 C) 1,0 0,9 Intensity [a.u.] Pomiar TEM 0,8 0,7 104 0,6 012 0,5 110 113 024 116 214 300 122 0,4 0,3 0,2 0 20 40 60 80 2 θ [o ] 100 2R TEM [nm] ~2,8 120 140 2R x-Ray [nm] 2R x-Ray [nm] (przed wypaleniem) (po wypaleniu) ~ 2,5 ~ 37,5 40 Nanocząstki Fe2O3 Właściwości magnetyczne Temperaturowa zależność magnetyzacji ZFC-FC zmierzona dla kropek kwantowych Fe2O3 w polu magnetycznym o wartości 10 Oe. Μ(emu/g) Nadprzewodnikowy interferometr kwantowy (SQUID) 1,0x10 -3 9,0x10 -4 8,0x10 -4 7,0x10 -4 6,0x10 -4 5,0x10 -4 4,0x10 -4 3,0x10 -4 2,0x10 -4 1,0x10 -4 0,0 ZFC FC ZFC – schładzanie próbki w zerowym polu magnetycznym FC – schładzanie próbki w polu magnetycznym 0 50 T (K ) 100 150 Powyżej TBmax (temperatura blokowania) cząstki wykazują zachowanie superparamagnetyczne, czego przejawem jest superpozycja krzywych ZFC i FC oraz spadek wartości magnetyzacji w miarę wzrostu temperatury 41 Nanocząstki Fe2O3 Właściwości magnetyczne Nanocząstki przed wygrzaniem (2R = 2,5 nm) Nanocząstki Fe2O3 po wygrzaniu (2R = 37,5 nm) Kolejny etap: Pokrywanie nanocząstek ZnO/MgO i Fe2O3 związkami organicznymi w celu przyłączenia przeciwciał do oligomerów β-amyloidu 42 Ale po co to wszystko? Trzy strategie budowania biosensorów: 1. Fluorescencyjny Rezonansowy Transfer Energii (FRET) między nanocząstką ZnO a barwnikiem organicznym czułym na środowisko zewnętrzne 2. Biosensor optyczno – magnetyczny do wykrywania krótkich oligomerów β-amyloidu (wczesne wykrywanie choroby Alzheimera) 3. FRET między nanocząstką ZnO pokrytą przeciwciałem a białkiem do którego zostaje przyłączona • pokrycie nanocząstek ZnO/MgO związkami organicznymi zakończonymi grupami karboksylowymi (-COOH), np. kwas oleinowy • przyłączenie przeciwciała specyficznego do danego miejsca w komórce bez denaturacji białka 43 Ale po co to wszystko? Trzy strategie budowania biosensorów: 1. Fluorescencyjny Rezonansowy Transfer Energii (FRET) między nanocząstką ZnO a barwnikiem organicznym czułym na środowisko zewnętrzne 2. Biosensor optyczno – magnetyczny do wykrywania krótkich oligomerów β-amyloidu (wczesne wykrywanie choroby Alzheimera) 3. FRET między nanocząstką ZnO pokrytą przeciwciałem a białkiem do którego zostaje przyłączona 4. FRET między nanocząstką NaYF4: Er, Yb wykazującą właściwości „upconvertujące” pokrytą przeciwciałem a białkiem do którego zostaje przyłączona lub barwnikiem przyczepionym do jej powierzchni 44 Upkonwersja 1. Upkonwersja opisuje konwersję promieniowania o niskiej energii (bliska podczerwień) do wyższego energetycznie promieniowania (widzialnego Er oraz ultrafioletu Gd) przez multifotonową absorpcję i późniejszą luminescencję. 2. Większość biologicznych struktur absorbuje światło w paśmie widzialnym i ultrafioletowym. Bliska podczerwień (długość fali 700 – 1000 nm) jest mało absorbowana przez molekuły biologiczne. 3. Układy biologiczne pobudzane bliską podczerwienią wykazują także mniej autofluorescencji niż pobudzane promieniowaniem ultrafioletowym. 4. Emisja w świetle widzialnym pozwala obserwować procesy życiowe wewnątrz komórek, a emisja w świetle UV pozwala na selektywne uśmiercanie komórek rakowych. 45 Mechanizm upkonwersji z transferem energii (ang. Energy transfer upconversion ETU) F. Wang, X. Liu, Chem. Soc. Rev, 2009, 38, 976-989 2H 7/2 2H 11/2 4S 3/2 4F 9/2 4I 9/2 4I 11/2 655 nm 520 nm Yb 3+ 540 nm 2F 5/2 980 nm Mechanizm jest oparty na sekwencyjnej absorpcji dwóch fotonów powodującej obsadzenie wyższego poziomu. Pobudzenie odbywa się przez transfer energii między dwoma sąsiadującymi jonami ziem rzadkich (między iterbem a erbem). Jeden jon działa jako absorber (donor energii) - iterb a drugi jako aktywator (akceptor energii) – erb. Aktywator jest pobudzany do stanu wyższego przez pierwszy niepromienisty transfer energii podczas gdy absorber relaksuje do stanu podstawowego. Drugie pobudzenie aktywatora i kolejny transfer energii umożliwia powstanie stanu emitującego. 4I 13/2 4I 15/2 2F 7/2 Er 3+ 46 Mechanizm upkonwersji z transferem energii (ang. Energy transfer upconversion ETU) ET – Energy Transfer EBT – Energy Back Transfer Mechanizm: -) Transfer energii między erbem (aktywator) a gadolinem (aktywator) (ET1 i ET2) -) Transfer energii między iterbem (absorber) a gadolinem (aktywator) -) Obserwujemy luminescencję przy dlugosci fali 246 nm, 252 nm, 276 nm, 311 nm G. Chen, H. Liang, H. Liu, G. Somesfalean, Z. Zhang, Optics Express, 2009, vol. 17, No. 19, 16366-16371. 47 Dlaczego NaYF4? Wydajność upkonwersji zależy od: -) stężenia absorbera i aktywatora (stężenia domieszek, co determinuje odległość między sąsiadującymi jonami domieszkowymi) -) struktury krystalicznej kryształu matrycowego -) wielkości nanocząstek (im większa średnica tym większa intensywność emisji) – ze względu na mniejszy stosunek powierzchni do objętości. Na powierzchni nanocząstki atomy metali ziem rzadkich nie wykazują właściwości upkonwertujących. Kryształ matrycowy powinien mieć sieć krystaliczną dopasowaną do jonów domieszkowych i niską energię fononową, aby zminimalizować niepromieniste procesy relaksacji. Te wymagania spełniają fluorki. 48 Synteza nanocząstek NaYF4: Er, Yb, Gd (1-0,02-x) mmol Y2O3 x mmol Yb2O3 0,02 mmol Er2O3 Y2O3 + 6HNO3 → 2Y(NO3)3 + 3H2O + 10 ml 10 % HNO3 Yb2O3 + 6HNO3 → 2Yb(NO3)3 + 3H2O (ogrzewanie w celu usunięcia wody) Er2O3 + 6HNO3 → 2Er(NO3)3 + 3H2O 4 mmol NH4F w glikolu etylenowym 80 °C Y(NO3)3, Yb(NO3)3, Er(NO3)3 + 10 ml glikolu etylenowego + 0,5560 g PVP + 1mmol NaCl, ogrzewanie 80 °C Reakcja: 2 h, 160 °C NaYF4: xYb, 0,02Er / PVP Na+ + (1 – 0,02 – x)Y3+ + xYb3+ + 0,02Er3+ + 4F- → NaYF4: xYb, 0,02 Er X. Li, Y. Zhang, Angew. Chem. Int. Ed, 2006, 45, 7732-7735 49 Pokrywanie nanocząstek NaYF4: Er, Yb, Gd warstwą SiO2 NaYF4: xYb, 0,02Er / PVP 0,06 ml tetraetoksysilan (TEOS) w 10 ml etanolu Do 20 ml etanolowego roztworu nanocząstek (0,05 mmol) dodano 4 ml H2O i 0,5 ml 30 % amoniaku Reakcja: ~ 15h, 25 °C NaYF4: xYb, 0,02Er / SiO2 Hydroliza TEOS w obecności wodorotlenku amonu jako katalizatora O O Si O Si OEt EtO Si OEt OEt TEOS NH4OH -EtOH OH HO Si OH -H2O OH Kwas monosilanowy X. Li, Y. Zhang, Angew. Chem. Int. Ed, 2006, 45, 7732-7735 OH OH HO Si O Si OH OH O O Si O Si OH Kwas disilanowy SiO2 50 Luminescencja nanocząstek NaYF4: Er, Yb, Gd 7,0E+03 6,0E+03 luminescencja 5,0E+03 10,9 g/l NaYF4/PVP 10,8 g/l NaYF4: 10% Yb, 2 % Er /PVP 10,1 g/l NaYF4: 18% Yb, 2 % Er /PVP 10,8 g/l NaYF4: 30% Yb, 2 % Er /PVP 11,4 g/l NaYF4: 20% Yb, 2 % Er, 5 % Gd /PVP 4,0E+03 Długość fali pobudzania: 980 nm 3,0E+03 2,0E+03 1,0E+03 0,0E+00 500 550 600 długość fali [nm ] 650 700 Próbka Stosunek powierzchni pod pikiem 660 nm do 540 nm (średnia 3 pomiarów) 2 % Er, 10 % Yb 6,4 2 % Er, 18 % Yb 5,9 2 % Er, 30 % Yb 11,4 20 % Yb, 2% Er, 5 % Gd 7,4 Wielkość i struktura nanocząstek NaYF4: Er, Yb, Gd 1,4E+05 111 NaYF4: NaYF4: NaYF4: NaYF4: NaYF4 1,2E+05 Intensywność 1,0E+05 8,0E+04 2 % Er, 2 % Er, 2 % Er, 2 % Er, / PVP 30 20 18 10 % % % % Yb / Yb / Yb / Yb / PVP PVP PVP PVP 220 6,0E+04 31 1 200 4,0E+04 2,0E+04 222 0,0E+00 10 30 50 420 400 311 422 70 90 o 2 theta [ ] Dyfrakcja rentgenowska – potwierdzenie kubicznej struktury 511 440 531 600 110 130 150 Próbka NaYF4 Średnica [nm] 0 % Er, 0 % Yb ~30 2 % Er, 10 % Yb ~30 2 % Er, 18 % Yb ~30 2 % Er, 20 % Yb ~36 2 % Er, 30 % Yb ~28 20 % Yb, 2 % Er, 5 % Gd ~32 Wielkość i struktura nanocząstek NaYF4: Er, Yb, Gd Transmisyjny Mikroskop Elektronowy Obraz nanocząstek NaYF4: 30 % Yb, 2 % Er / PVP Potwierdzenie kubicznej struktury Otoczka SiO2 Próbka NaYF4 Średnica [nm] 0 % Er, 0 % Yb ~35 2 % Er, 10 % Yb ~45 2 % Er, 18 % Yb ~45 2 % Er, 20 % Yb ~55 2 % Er, 30 % Yb ~35 20 % Yb, 2 % Er, 5 % Gd ~50 Nanocząstki NaYF4: Er, Yb, Gd wewnątrz komórek HeLa Kolor zielony: autofluorescencja (pobudzenie 488 nm), Kolor czerwony: nanocząstki (pobudzenie 960 nm) 1,2 5 6 1 2 3 1 2 3 4 lu m in e s c e n c ja 7 1 0,8 4 0,6 6 5 7 0,4 0,2 0 480 530 580 630 680 dlugosc fali [nm] 54 Nanocząstki NaYF4: Er, Yb, Gd wewnątrz komórek HeLa Kolor zielony: autofluorescencja (pobudzenie 488 nm), Kolor czerwony: nanocząstki (pobudzenie 960 nm) xz yz 55 Kolejny etap: Pokrycie nanocząstek NaYF4 warstwą organiczną w celu przyłączenia białka lub barwnika organicznego czułego na środowisko 56 Podsumowanie 1. Nanocząstki ZnO/MgO/CMCD użyto do zbudowania biosensora czułego na środowisko zewnętrzne dzięki fluorescencyjnemu rezonansowemu transferowi energii między nanocząstkami ZnO/MgO (donor) a Czerwienią Nilu (akceptor) ulokowaną wewnątrz cyklodekstryny 2. Nanocząstki ZnO/MgO/CMCD/Czerwień Nilu zostały wprowadzone do komórek nowotworowych HeLa i zaobserwowano zmianę luminescencji Czerwieni Nilu w zależności od miejsca ulokowania w/na/obok komórkach HeLa. 3. Prawdopodobnie zaobserwowano FRET wewnątrz komórek HeLa. 4. Utworzono nanocząstki Fe2O3 wykazujące właściwości superparamegnetyczne w temperaturze pokojowej w celu użycia ich razem z nanocząstkami ZnO/MgO do budowy biosensora do wykrywania krótkich oligomerów β - amyloidu (znaczenie w chorobie Alzheimera) 5. Zsyntetyzowano i scharakteryzowano nanocząstki NaYF4: Er, Yb, Gd wykazujące właściwości upkonwertujące i wprowadzono je do wnętrza komórek HeLa. 57 Podziękowanie Zespól Fizyki Biologicznej Prof. Danek Elbaum Dr Krzysztof Fronc Instytut Fizyki PAN Mgr Anna Baranowska - Korczyc Mgr Izabela Kamińska Instytut Biochemii i Biofizyki PAN Mgr Kamil Sobczak – pomiary TEM Mgr Piotr Dziawa – pomiary SQUID Dr Roman Minikayev – pomiary X-ray Prof. Wojciech Paszkowicz – pomiary X-ray Wydział Fizyki UAM Sebastian Szewczyk – synteza NaYF4: Er, Yb Kamil Koper – wprowadzanie cząstek do komórek Prof. Piotr Stępień Instytut Podstawowych Problemów Techniki PAN Dr Piotr Krakowian – mikroskop konfokalny Prof. Tomasz Kowalewski Dr Sławek Błoński, Mgr Krzysztof Zembrzycki – pomoc Instytut Biologii Doświadczalnej PAN Prof. Grzegorz Wilczyński – mikroskop konfokalny Dr Jakub Wlodarczyk – mikroskop konfokalny 58 Wpływ temperatury na intensywność luminescencji w układzie ZnO/MgO/CMCD i Czerwień Nilu 6,0E+06 Nile Red w FRET 20 ZnO w FRET 5,0E+06 ZnO/MgO/CMCD 20 20 20 20 Intensywność 4,0E+06 ZnO/MgO 20 3,0E+06 2,0E+06 1,0E+06 45 45 45 45 45 45 0,0E+00 temperatura [0C] ∆intNRwFRET ∆intZnOwFRET ∆intZnO/MgO/CMCD ∆intZnO/MgO/CMCD 2,3*10-6 1,0*10-6 1,3*10-6 1,4*10-6 59 FRET: ZnO/MgO/CMCD i Czerwień Nilu Równanie Fostera pozwala na określanie odległości między donorem a akceptorem, dlatego też jest używane przez chemików jako „elektroniczna suwmiarka” Przyjmując założenia: 1). Donor oddziałuje z wieloma akceptorami 2). Transfer energii do każdego z akceptorów można rozważać jako niezależne zdarzenie to wydajność transferu energii może być wyrażona równaniem: nR06 Q= 6 6 nR0 + r n – liczba molekuł akceptora Dla układu ZnO/MgO/CMCD Æ Czerwień Nilowa R0 = 3,4 nm [1] Wartość r, odległość donora od akceptora w układzie ZnO/MgO/CMCD Æ Czerwień Nilowa, może być wyznaczona przez dopasowanie powyższego równania do eksperymentalnie obserwowanych zależności między wydajnością rezonansowego transferu energii a stężeniem akceptora [1] S. Raksshit, S. Vasudevan, ACS Nano, 2008, 2(7), 1473 – 1479 60 FRET: ZnO/MgO/CMCD i Czerwień Nilu Wydajność rezonansowego transferu energii: I −I Q = ZnO ZnO − NR I ZnO IZnO – intensywność luminescencji donora ZnO/MgO/CMCD w wodzie w przypadku braku Czerwieni Nilowej IZnO-NR - intensywność luminescencji donora ZnO/MgO/CMCD w wodzie w obecności różnych stężeń Czerwieni Nilowej (stężenie donora jest stałe) 9000(ln 10)κ 2γ D0 R0 = J (λ ) 5 4 128π N Aη κ2 – czynnik orientacyjny, który wynosi 2/3 dla losowo zorientowanych dipoli donor – akceptor, γD0 – wydajność kwantowa donora w nieobecności akceptora NA – liczba Avogadro η - współczynnik załamania światła k ZnO − NR R06 Q= = 6 6 −1 k ZnO − NR + τ ZnO R0 + r τZnO – czas zaniku emisji donora ZnO/MgO w nieobecności Czerwieni Nilowej kZNO-NR – stała szybkości emisji donora ZnO/MgO/CMCD w obecności akceptora Czerwieni Nilowej r – odległość między donorem a akceptorem R0 – krytyczna odległość (promień Forster’a), przy której transfer i spontaniczny zanik ekscytowanego donora są równie prawdopodobne, kZnO-NR = τZnO-1. ∞ J (λ ) = ∫ I D (λ )ε A (λ )λ4 dλ 0 J(λ) – spektralne nałożenie emisji donora i absorpcji akceptora: S. Rakshit et al., ACS Nano, vol. 2, no. 7, 2008, 1473-1479 61 Toksyczność krótkich oligomerów β-amyloidu Zaobserwowano, po przebadaniu surowicy 20 pacjentów z Chorobą Alzheimera (AD) i 18 pacjentów zdrowych, zwiększoną ilość oligomerów i krótkich włókien amyloidowych w obecności surowicy z AD w porównaniu do populacji kontrolnej. Ma to potencjalna wartość diagnostyczną. Nowicka, et.al., JAD, 2010 62 Struktura Czerwieni Nilu 63