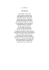Wpływ mutacji w genach regulatorowych nfxB klinicznych szczepów
Transkrypt
Wpływ mutacji w genach regulatorowych nfxB klinicznych szczepów
diagnostyka laboratoryjna Journal of Laboratory Diagnostics 2009 • Volume 45 • Number 4 • 285-292 Praca oryginalna • Original Article Wpływ mutacji w genach regulatorowych nfxB klinicznych szczepów Pseudomonas aeruginosa na oporność na fluorochinolony Zenobia Wydmuch1, Marta Adamek2, Olga Skowronek-Ciołek3 Laboratorium Analityczne Szpitala Specjalistycznego w Chorzowie; Instytut Fizjologii Człowieka Akademii Wychowania Fizycznego im. Bronisława Czecha w Krakowie; 3 Katedra i Zakład Mikrobiologii Wydziału Farmaceutycznego z Oddziałem Medycyny Laboratoryjnej Śląskiego Uniwersytetu Medycznego w Katowicach 1 2 Streszczenie Cel badań: Niepokojący jest narastający rozwój oporności szczepów Pseudomonas aeruginosa na fluorochinolony. Z badań genetycznych wynika, iż istotnym mechanizmem oporności są mutacje w genach regulatorowych, prowadzące do nadekspresji pomp MDR (ang. multi drug resistant) i powstawania oporności na wiele grup leków przeciwbakteryjnych. Celem pracy było wykrycie mutacji w genach regulatorowych nfxB klinicznych szczepów P. aeruginosa, odpowiedzialnych za oporność na fluorochinolony. Materiał i metody: Badaniem objęto 44 izolaty P. aeruginosa wyizolowane z materiałów klinicznych od pacjentów hospitalizowanych i ambulatoryjnych. Metodą E-testów oznaczono MIC fluorochinolonów dla badanych drobnoustrojów. Wyizolowany DNA chromosomalny pałeczek ropy błękitnej poddano reakcji amplifikacji, produkty reakcji PCR sekwencjonowano. Wyniki: Analiza sekwencyjna części kodującej fragmentu genu nfxB badanych pałeczek pozwoliła na wykrycie 3 typów mutacji punktowych w 24/44 izolaty (Glu-124→Ala, Arg-82→Leu, Ala-15→Val) i 7 typów mutacji cichych. W 10/24 szczepy, w których w genie nfxB występowała mutacja Glu-124→Ala, stwierdzono oporność na wszystkie użyte do badań fluorochinolony. Szczep posiadający podwójną mutację punktową: Ala-15→Val, Glu-124→Ala, również wykazywał całkowitą oporność. Najczęściej wykrywaną mutacją w badanym fragmencie genu była mutacja punktowa Glu-124→Ala, którą zidentyfikowano w 24/44 badane izolaty, wykazywały one wysoką oporność na fluorochinolony. Wnioski: Przedstawione wyniki badań wskazują na znaczący wpływ mutacji w genie nfxB pałeczek P. aeruginosa w nabywaniu oporności na fluorochinolony. nfxB genes mutations and their impact on resistance to fluoroquinolones of Pseudomonas aeruginosa clinical strains Summary Aim: The growing concern is rising resistance to fluoroquinolones of Pseudomonas aeruginosa strains. The genetic testing shows that an important mechanism of resistance is due to mutations in the analyzed ntxB regulatory genes, leading to overexpression of mutidrug resistance MDR pumps and to formation of resistance to many groups of antibacterial drugs. The purpose of this study was to detect mutations in nfxB regulatory genes of P. aeruginosa clinical strains, responsible for resistance to fluoroquinolones. Materials and methods: The study included 44 isolates of P. aeruginosa taken from patients hospitalized or from ambulatory patients. E-test method was used to determine MICs for all the fluoroquinolones tested. Bacterial DNA isolates were amplified, and subsequently the PCR reaction products were sequenced. Results: Sequencing analysis of the nfxB genes revealed 3 types of point mutations in the 24 of 44 isolates and 7 types of silent mutations. In 10 of 24 strains in which the nfxB genes mutations were detected, mutations at Glu-124-Ala were found to code resistance to all fluoroquinolones used in our research. The strain bearing the double point mutation: at Ala-15-Val, and Glu-124-Ala, also showed the total drug resistance. The most frequently detected nfxB gene mutation was point mutation described at Glu-124-Ala, which was identified in 24 of 44 isolates tested, and also showed high resistance to fluoroquinolones. Conclusions: Our results indicate a significant impact of nfxB genes mutations on the aquisition of Pseudomonas aeruginosa resistance to fuoroquinolones. Słowa kluczowe:Pseudomonas aeruginosa, oporność, geny regulatorowe, mutacja cicha, mutacja punktowa, nfxB, sekwencjonowanie, fluorochinolony 285 Wpływ mutacji w genach regulatorowych nfxB klinicznych szczepów Pseudomonas aeruginosa na oporność ... Key words:Pseudomonas aeruginosa, resistance, regulatory genes, silent mutation, point mutation, nfxB, sequence analysis, fluoroquinolones Wstęp Pałeczki P. aeruginosa należą do bakterii szeroko rozpowszechnionych w przyrodzie. Występują pospolicie w wodzie, glebie, ściekach i żywności. Stanowią również fizjologiczną florę przewodu pokarmowego ludzi i zwierząt. Szczepy tego gatunku mogą być także czynnikiem etiologicznym zakażeń układu oddechowego, dróg moczowych, zapalenia ucha środkowego i zatok, zapalenia opon mózgowo-rdzeniowych, kości i szpiku kostnego, zapalenia osierdzia i wsierdzia, zapalenia spojówek oka oraz zatrucia pokarmowego [4, 14]. Chemioterapia zakażeń wywołanych pałeczką P. aeruginosa stanowi jedno z najtrudniejszych zagadnień lecznictwa. Wynika to z faktu istnienia szczepów opornych na wiele antybiotyków oraz łatwości pojawiania się oporności na antybiotyki aktualnie stosowane. Pałeczka ropy błękitnej wykazuje wysoką naturalną oporność na penicylinę G, ampicylinę, cefalosporyny I i II generacji, tetracykliny, linkosamidy i stare chinoliny. Aktywność wobec tego gatunku mogą wykazywać karbenicylina, tykarcylina, ureidopenicyliny, aztreonam, cefalosporyny III i IV generacji, karbapenemy, aminoglikozydy i fluorochinoliny [2, 3, 10, 16, 18]. Fluorochinolony to grupa leków przeciwbakteryjnych, które w odróżnieniu od starych chinolonów charakteryzują się aktywnością wobec pałeczek niefermentujących (P. aeruginosa, Acinetobacter sp.), a także niektórych ziarenkowców Gramdodatnich. Rozwój oporności na fluorowane chinolony ogranicza skuteczność stosowania tych względnie nowych chemioterapeutyków. Niepokojący jest zwłaszcza niespodziewanie szybki rozwój oporności szczepów P. aeruginosa. Oporność na fluorochinolony u tych drobnoustrojów może wynikać z modyfikacji miejsca w komórce, będącego punktem uchwytu leku – mutacje w genach gyrA i parC, zmniejszonego przenikania leku przez zewnętrzną błonę komórkową oraz mutacji w genach regulatorowych prowadzących do nadekspresji pomp MDR (ang. multi drug resistant), skutecznie usuwających chinoliny z komórki bakteryjnej. Wymienione powyżej mechanizmy uwarunkowane są chromosomalnie [1, 8, 11]. Kodowana chromosomalnie oporność nie jest przenoszona horyzontalnie, a pojedyncza mutacja nie powoduje powstania oporności o znaczeniu klinicznym. Fenotyp oporności nadaje kombinacja mutacji w silnie konserwatywnym re- gionie chromosomu, tak zwanym regionie warunkującym oporność na chinolony – QRDR (ang. Quinolone Resistant Determination Region) i dodatkowo w regulatorowym locus mar, które jest zaangażowane w aktywne wydalanie leku z komórki oraz zmniejszone jego pobieranie, przez redukcję syntezy powierzchniowego białka OmpF. U P. aeruginosa za ten mechanizm odpowiedzialny jest operon kodowany przez geny mex (ang. multiple efflux). Pompy te zwykle współdziałają z systemami wspomagającymi. U P. aeruginosa zidentyfikowano 5 pomp efflux: MexAB-OprM, MexCD-OprJ, MexEF-OprN, MexXY-OprM i ostatnio odkryta MexVM-OprM. Cztery pierwsze pompy efflux są regulowane m.in. przez geny: nfxB, mexR, mexT i mexZ. Mutacje występujące w obrębie któregoś z wyżej wymienionych genów regulatorowych są odpowiedzialne za zwiększenie ekspresji odpowiednich pomp efflux, wyrzut fluorochinolonu z komórki i rozwój oporności. Proces ten przyczynia się do spadku stężenia wewnątrzkomórkowego leku i wzrostu wartości MIC [1, 8, 9, 13, 15, 17, 20]. Celem niniejszej pracy było poszukiwanie mutacji w genach regulatorowych nfxB klinicznych szczepów P. aeruginosa odpowiedzialnych za oporność na fluorochinolony. Materiał i metody Przedmiotem badań były 44 szczepy pałeczek P. aeruginosa, które wyizolowano z materiału klinicznego (wymazy z gardła, z rany, z ucha, przetoki, mocz), pochodzącego od pacjentów hospitalizowanych i ambulatoryjnych, w Zakładzie Mikrobiologii Wojewódzkiego Szpitala Specjalistycznego Nr 5 im. Św. Barbary w Sosnowcu. Metodą E-testów wykonano badanie lekowrażliwości szczepów P. aeruginosa, oznaczając MIC 5. fluorochinolonów: ciprofloksacyny (CI), ofloksacyny (OF), pefloksacyny (PE), sparfloksacyny (SO) i norfloksacyny (NX). Do badania wykorzystano podłoże agar Hinton-Müller (HMA) oraz paski E-test® (firmy AB®Biodisk), posiewy inkubowano w temperaturze 35°C 18-24 h, następnie odczytywano wartości MIC użytych do badań antybiotyków, zgodnie z zalecanymi NCCLS (National Committee for Clinical Laboratory Standards) (tab. I). Wykonano również badanie kontrolne z użyciem szczepu wzorcowego P. aeruginosa ATCC 27853 [5]. Tabela I. Zakresy wrażliwości szczepów P. aeruginosa na wybrane do badań fluorochinolony. Stopień wrażliwości Wrażliwy 286 Zakresy wartości stężeń (μg/ml) fluorochinolonów na pasku E-testu CI OF PE SO NX ≤1 ≤2 ≤2 ≤0,5 ≤4 Średnio wrażliwy 2 4 4 1 8 Oporny ≥4 ≥8 ≥8 ≥2 ≥16 Z. Wydmuch, M. Adamek i O. Skowronek-Ciołek Kolejnym etapem badania była izolacja chromosomalnego DNA z komórek badanych szczepów, przy użyciu zestawu QIAmp® DNA Mini Kit(QIAGEN), zgodnie z załączonym protokołem. W celu potwierdzenia obecności wyizolowanego DNA wykonano elektroforezę w 1,5% żelu agarozowym. Następnie dobrano odpowiednie startery i warunki reakcji PCR do identyfikacji fragmentów genu nfxB. Sekwencję genu nfxB (GB:X65646) P. aeruginosa wyszukano w bazie GenBank® (www.ncbi.nlm.nih.gov/), następnie dobrano właściwe startery komplementarne do amplifikowanej sekwencji badanego genu, które przedstawiono w tabeli II. Potwierdzenie sekwencji nukleotydowej starterów dla genu nfxB uzyskano z danych literaturowych [20] i potwierdzono w GenBank®. Ustalone doświadczalnie warunki reakcji PCR programowano w termocyklerze Personal Thermocycler (BIOMETRA). Do reakcji amplifikacji wykorzystano zestaw 2xPCR Master Mix (Fermentas) oraz startery robocze o stężeniu 5 pmol/μl. Doświadczalnie ustalono profil temperaturowy reakcji PCR dla amplifikowanego fragmentu genu nfxB: I etap: Termiczna aktywacja polimerazy DNA Taq (95˚C – 3 min) II etap: Denaturacja (94˚C – 1 min) Przyłączenie starterów (56˚C – 1 min) Wydłużanie starterów (72˚C – 1 min) 35 cykli reakcji PCR (I i II etap) dla amplifikowanego fragmentu genu nfxB III etap: Końcowe wydłużanie (72˚C – 10 min). Produkty amplifikacji badanego fragmentu genu uzyskano dla 24 szczepów. Potwierdzeniem obecności genu nfxB był prążek na żelu agarozowym o wielkości 584 pz. Fragmenty genu nfxB poddawano reakcji sekwencjonowania, badanie to przeprowadzono w Pracowni Sekwencjonowania DNA i Syntezy Oligonukleotydów IBB PAN w Warszawie. PCR sekwencyjny produktów amplifikacji genu nfxB wykonano z wykorzystaniem komercyjnego zestawu DNA Sequencing Kit Big Dye Terminator Cycle Sequencing v3.1. Badany fragment genu nfxB amplifikowano w warunkach przedstawio- nych w tabeli III. Analizę uzyskanych wyników dotyczących sekwencji nukleotydowej i aminokwasowej przeprowadzono z zastosowaniem programów: FinchTV ≥ 1.3.0 oraz GenDoc A.zip. Przy użyciu wyżej wymienionych programów przeprowadzono porównanie sekwencji genu nfxB szczepu dzikiego (GB:X65646) (http://www.ncbi.nlm.nih.gov/) z genami nfxB badanych izolatów. Wyniki Szczegółową ocenę wrażliwości 44 klinicznych szczepów P. aeruginosa oraz szczepu wzorcowego przedstawiono w tabeli IV. Analizując wyniki badań, zaobserwowano, iż pałeczki ropy błękitnej wykazują najwyższą wrażliwość na norfloksacynę: 25/44 szczepy (56,82%) i ciprofloksacynę: 21/44 szczepy (47,73%), natomiast badane izolaty najbardziej oporne były na sparfloksacynę: 33/44 szczepy (75%), pefloksacynę: 27/44 (61,36%) i ofloksacynę: 24/44 szczepy (54,54%). W badaniach stwierdzono, że szczepy kliniczne izolowane z materiału od pacjentów hospitalizowanych charakteryzowały się dużo wyższą opornością niż te wyhodowane od pacjentów z poradni. Wszystkie badane szczepy, w których wykryto gen nfxB (24/44 szczepy), poddano sekwencjonowaniu. Wyniki uzyskanych fragmentów genu nfxB 24 badanych izolatów przedstawiono w tabeli V w zestawieniu z wartościami MIC fluorochinolonów. Wykonując sekwencjonowanie fragmentu genu nfxB badanych pałeczek ropy błękitnej, wykryto 3 typy mutacji punktowych ze zmianą w sekwencji nukleotydowej i aminokwasowej: GAA→GCC(Glu-124→Ala), CGC→CTC(Arg82→Leu) i GCA→GTA( Ala-15→Val) oraz 7 typów mutacji cichych, wyłącznie ze zmianą w sekwencji nukleotydowej, w 13 badanych szczepach. Na rycinie 1 pokazano miejsce mutacji punktowej w kodonie 82, którą porównano z sekwencją fragmentu genu nfxB szczepu POA. Mutację punktową Glu-124→Ala wykryto we wszystkich poddanych analizie sekwencyjnej szczepach, zmianę aminokwasową Arg-82→Leu w 8 izolatach, zaś mutację Ala15→Val stwier- Tabela II. Startery użyte w reakcji PCR. Nazwa Sekwencja nukleotydowa ( 5’ - 3’) nfxB 1F nfxB 2R Stężenie μM μg/μl 5’-AAAACCAACCGGGACCCATC-3’ (20 nukleotydów) 313 1,89 5’-CAGGAGCGAGCCGGATT-3’ (17 nukleotydów) 314 1,65 Tabela III. Profil temperaturowy i czasowy amplifikacji sekwencyjnej genu nfxB (ilość cykli 25). Temperatura Czas 94°C 10 s 52°C 20 s 60°C 4 min Długość fragmentu genu 584 pz dzono u 1 mutanta pałeczki ropy błękitnej. Spośród 24 badanych szczepów mutację cichą posiadało: 10 izolatów w kodonie 160. (Arg-160→Arg), 8 w kodonach 13. (Ala-13→Ala), 61. (Val-61→Val), 141. (Ala-141→Ala) i 162. (Gly-162→Gly) oraz 1 szczep w dwóch kodonach: 42. (Arg-42→Arg) i 129. (Gly-129→Gly). Stwierdzono, że szczepy P. aeruginosa posiadające mutację w genie regulatorowym nfxB izolowane 287 Wpływ mutacji w genach regulatorowych nfxB klinicznych szczepów Pseudomonas aeruginosa na oporność ... Tabela IV. Wrażliwość (MIC) badanych szczepów P. aeruginosa oraz szczepu wzorcowego ATCC 27853 na fluorochinolony (CI, OF, PE, SO, NX). Wrażliwość na fluorochinolony [MIC (μg/ml)] Numer szczepu Wb CI OF PE SO NX MICa MICa MICa MICª MICa Sb Ob Wb Sb Ob Wb Ob Wb Sb Ob Wb Sb 2 3 >32 32 >32 8 3 3 16 24 16 8 >32 24 16 8 8 4 2 5 1,5 6 9 4 2 >32 0,125 10 0,75 24 1 2 >32 6 8 12 0,5 8 0,32 24 >32 8 8 8 0,75 16 0,64 0,75 1 0,5 0,38 17 0,94 0,5 1 0,5 0,38 19 0,95 0,75 1 2 27 >32 0,38 4 0,5 16 16 24 >32 >256 >32 4 >256 29 0,94 0,75 1 0,5 0,38 30 0,94 0,5 1 0,5 0,38 36 2 40 42 >32 1 43 44 1,5 0,25 0,5 50 0,25 16 32 >256 >32 12 8 8 4 16 8 12 4 2 1 >256 >32 2 >32 49 32 >32 2 47 >32 3 3 2 2 Ob 3 15 26 8 >256 >256 3 2 2 1 54 >32 >32 >256 >32 >256 69 >32 >32 >256 >32 >256 70 >32 >32 >256 >32 >256 71 >32 >32 >256 >32 >256 76 >32 >32 >256 >32 >256 90 0,094 0,75 0,75 0,5 0,25 91 >32 >32 >256 >32 >256 93 >32 >32 >256 >32 >256 94 >32 >32 >256 >32 >256 95 96 >32 0,25 >32 1 102 0,064 105 1 106 0,094 107 1 110 0,094 112 0,5 115 0,75 120 0,38 0,25 >256 1 1,5 0,5 0,75 4 4 16 6 0,38 6 8 8 2 2 A – MIC w μg/ml B – stopień wrażliwości: W – wrażliwy, S – średnio wrażliwy, O – oporny 0,5 1,5 3 16 2 >256 0,25 0,38 32 4 >32 8 1 >256 0,5 0,25 3 1,5 >32 0,5 >32 0,5 2 ATCC 27853 >256 1,5 >32 104 119 288 Sb 4 0,38 3 1,5 4 2 4 4 2 1 1 Z. Wydmuch, M. Adamek i O. Skowronek-Ciołek Tabela V. Zestawienie MIC fluorochinolonów ze zmianami w genach regulatorowych nfxB zmutowanych szczepów P. aeruginosa. CI OF PE SO NX Zmiany w sekwencji nukleotydowej i aminokwaowej w genie nfxB ATCC 27853 0,25 1,5 2 0,5 1 -a 2 3 >32 32 >32 8 Arg(CGC)82→Leu(CTC) Glu(GAA)124→Ala(GCC) 3 3 16 24 16 8 Arg(CGC)82→Leu(CTC) Glu(GAA)124→Ala(GCC) 4 2 >32 24 16 8 Arg(CGC)82→Leu(CTC) Glu(GAA)124→Ala(GCC) 6 2 >32 24 12 8 Glu(GAA)124→Ala(GCC) Ala(GCG)13→Ala(GCA)c Val(GTA)61→Val(GTG)c Glu(GAA)124→Ala(GCC) Ala(GCG)141→Ala(GCA)c Arg (CGT)160→Arg (CGC)c Gly(GGA)162→Gly(GGT)c 10 2 >32 24 12 8 26 2 16 16 24 4 36 2 32 16 32 8 Arg(CGC)82→Leu(CTC) Glu(GAA)124→Ala(GCC) >256 Ala(GCG)13→Ala(GCA)c Val(GTA)61→Val(GTG)c Glu(GAA)124→Ala(GCC) Ala(GCG)141→Ala(GCA)c 40 c >32 >32 >256 >32 Arg(CGC)82→Leu(CTC) Glu(GAA)124→Ala(GCC) 42 1 12 8 8 4 Ala(GCG)13→Ala(GCA)c Val(GTA)61→Val(GTG)c Glu(GAA)124→Ala(GCC) Ala(GCG)141→Ala(GCA)c Arg (CGT)160→Arg (CGC)c Gly(GGA)162→Gly(GGT)c 43 1,5 16 8 12 4 Arg(CGC)82→Leu(CTC) Glu(GAA)124→Ala(GCC) 44 0,25 2 2 2 1 Arg(CGC)82→Leu(CTC) Glu(GAA)124→Ala(GCC) 47 >32 >32 >256 >32 >256 Gly(GGA)162→Gly(GGT)c Glu(GAA)124→Ala(GCC) 50 0,25 2 2 2 1 Glu(GAA)124→Ala(GCC) >256 Ala(GCG)13→Ala(GCA)c Val(GTA)61→Val(GTG)c Glu(GAA)124→Ala(GCC) Ala(GCG)141→Ala(GCA)c Arg (CGT)160→Arg (CGC)c Gly(GGA)162→Gly(GGT)c 54 a MIC(µg/ml) Numer szczepu >32 >32 >256 >32 70 >32 >32 >256 >32 >256 Ala(GCG)13→Ala(GCA)c Val(GTA)61→Val(GTG)c Glu(GAA)124→Ala(GCC) Ala(GCG)141→Ala(GCA)c Arg (CGT)160→Arg (CGC)c Gly(GGA)162→Gly(GGT)c 71 >32 >32 >256 >32 >256 Gly(GGA)129→Gly(GGC)c Glu(GAA)124→Ala(GCC) – brak mutacji – mutacja cicha 289 Wpływ mutacji w genach regulatorowych nfxB klinicznych szczepów Pseudomonas aeruginosa na oporność ... Tabela V. cd. CI OF PE SO NX Zmiany w sekwencji nukleotydowej i aminokwaowej w genie nfxB ATCC 27853 0,25 1,5 2 0,5 1 -a >256 Ala(GCG)13→Ala(GCA)c Val(GTA)61→Val(GTG)c Glu(GAA)124→Ala(GCC) Ala(GCG)141→Ala(GCA)c Arg (CGT)160→Arg (CGC)c Gly(GGA)162→Gly(GGT)c 76 a c MIC(µg/ml) Numer szczepu >32 >32 >256 >32 91 >32 >32 >256 >32 >256 Ala(GCG)13→Ala(GCA)c Val(GTA)61→Val(GTG)c Glu(GAA)124→Ala(GCC) Ala(GCG)141→Ala(GCA)c Arg (CGT)160→Arg (CGC)c Gly(GGA)162→Gly(GGT)c 93 >32 >32 >256 >32 >256 Arg(CGT)160→Arg(CGC)c Glu(GAA)124→Ala(GCC) 94 >32 >32 >256 >32 >256 Arg(CGT)160→Arg(CGC)c Glu(GAA)124→Ala(GCC) 102 >32 >32 >256 >32 >256 Ala(GCA)15→Val(GTA) Arg(CGT)160→Arg(CGC)c Glu(GAA)124→Ala(GCC) 105 1 3 8 4 1,5 Glu(GAA)124→Ala(GCC) 107 1 32 16 16 4 Ala(GCG)13→Ala(GCA)c Arg(CGC)42→Arg(CGA)c Val(GTA)61→Val(GTG)c Glu(GAA)124→Ala(GCC) Ala(GCG)141→Ala(GCA)c Arg (CGT)160→Arg (CGC)c Gly(GGA)162→Gly(GGT)c 112 0,5 4 2 3 1,5 Arg(CGC)82→Leu(CTC) Glu(GAA)124→Ala(GCC) – brak mutacji – mutacja cicha były w większości z materiału klinicznego pochodzącego od pacjentów hospitalizowanych. W 10/24 badane izolaty, w których występowała mutacja punktowa Glu-124→Ala w badanym fragmencie genu nfxB: stwierdzono oporność na wszystkie użyte do badań fluorochinolony. Mutanty posiadające jednocześnie 2 zmiany aminokwasowe: Glu-124→Ala i Arg-82→Leu w większości wykazywały oporność na 3 chemioterapeutyki (SO, PE, OF), podczas gdy jeden szczep nr 102, posiadający podwójną mutację: Ala-15→Val i Glu-124→Ala, był oporny na wszystkie wykorzystane do badań fluorochinolony. Dyskusja Chemioterapia zakażeń wywołanych pałeczką P. aeruginosa stanowi obecnie jedno z najtrudniejszych zagadnień lecznictwa. Wynika to z faktu istnienia szczepów opornych na wiele antybiotyków oraz łatwości pojawiania się oporności na antybiotyki aktualnie stosowane. Zagadnienie to dotyczy także, jednej z najnowszych grup leków przeciwbakteryjnych – flu290 orowanych chinolonów. Z badań genetycznych wynika, że za oporność na tę grupę chemioterapeutyków u P. aeruginosa jest odpowiedzialnych kilka mechanizmów. Jeden z nich dotyczy występowania mutacji w genach regulatorowych P. aeruginosa prowadzących do nadekspresji pomp efflux [6, 12, 19]. W niniejszej pracy zajęto się poszukiwaniem mutacji w genach regulatorowych nfxB odpowiedzialnych za oporność na fluorochinolony klinicznych szczepów P. aeruginosa. Przeprowadzona przez nas analiza sekwencyjna fragmentu genu nfxB pałeczek ropy błękitnej pozwoliła na wykrycie 3 typów mutacji punktowych: Glu-124→Ala (24 szcz.), Arg-82→Leu (8 szcz.) i Ala-15→Val (1 szcz.) oraz 7 typów mutacji cichych w 13 badanych szczepach. Podobne badania w swojej pracy przeprowadzili Jalal i Wretling [8]. Spośród 16 poddanych analizie sekwencyjnej szczepów P. aeruginosa w pracy badaczy 2 izolaty posiadały mutację punktową z wymianą aminokwasu w genie nfxB. Jeden ze szczepów posiadał substytucję aminokwasu w kodo- Z. Wydmuch, M. Adamek i O. Skowronek-Ciołek Rycina 1. Zmiana sekwencji nukleotydowej i aminokwasowej w genie nfxB szczepu badanego Pseudomonas aeruginosa nr 2: CGC→CTC (Arg-82→Leu), w odniesieniu do genu nfxB szczepu dzikiego PAO (GB X 65646). nie 30 (Ala-30→Thr), zaś drugi w kodonie 62 (Leu-62→Val). Identyczne zmiany w przeprowadzonych przez siebie badaniach uzyskali Oh i wsp. [13]. Wykryli oni obecność tych samych mutacji punktowych w genie nfxB co Jalal i Wretling. Badacze zaobserwowali także, iż mutacje w genie nfxB występowały najczęściej w szczepach o wysokim poziomie oporności na norfloksacynę (MIC>64μg/ml) i ciprofloksacynę (MIC>32 μg/ml). W celu zidentyfikowania mutacji punktowych w genach gyrA, gyrB, parC, parE, nfxB oraz mexR Kugelberg i wsp. [9] wykonali sekwencjonowanie produktów PCR wymienionych fragmentów genów szczepów P. aeruginosa. Uzyskane przez badaczy wyniki wykazały obecność 2 nowych mutacji punktowych w genie nfxB: Leu-40→Gln, Gln-131→stop w 2 badanych izolatach. Oba zmutowane szczepy charakteryzowały się wysoką opornością na norfloksacynę (MIC>256 μg/ml). Jalal i wsp. [7] badali 20 szczepów P. aeruginosa pobranych od pacjentów ze zwłóknieniem torbielowatym. Izolaty ba- dano pod kątem mutacji punktowych w genach gyrA, parC, nfxB i mexR związanych z opornością na fluorochinolony. 16 szczepów P. aeruginosa posiadało mutacje w genie nfxB w pozycji 82 (Arg 82→Leu). Średnie wartości MIC ciproflkosacyny dla tych szczepów wyniosły 4-8 μg/ml. Dla porównania w naszych badaniach mutację w kodonie 82 wykryliśmy w 8/24 izolaty. Wartości MIC CI dla zmutowanych szczepów wyniosły od 0,25 do 3 μg/ml. Przedstawione wyniki badań wskazują na znaczący udział mutacji w genie nfxB w nabywaniu oporności na fluorochinolony. Nadmierna ekspresja pompy bakteryjnej MexCD-OprJ spowodowana mutacjami w badanym genie regulatorowym doprowadza do redukcji wewnątrzkomórkowego stężenia leku i obniżenia wartości stężenia hamującego MIC antybiotyków. Lomovskaya i wsp. [11] twierdzą w swojej pracy, iż hamowanie pomp wypływu P. aeruginosa może znacząco zwiększyć kliniczne zastosowanie fluorochinolonów. Można się spodziewać, że hamowanie pomp bakteryjnych spowoduje zmniejszenie poziomu wewnętrznej oporności, znaczą291 Wpływ mutacji w genach regulatorowych nfxB klinicznych szczepów Pseudomonas aeruginosa na oporność ... co cofnie nabytą oporność i zmniejszy częstość występowania mutantów wysoce opornych na chinolony. Dlatego też należy prowadzić dalsze badania dotyczące pomp bakteryjnych, a także innych mechanizmów oporności pałeczek ropy błękitnej na fluorochinolony, które pozwolą zwiększyć skuteczność tych leków w leczeniu zakażeń bakteryjnych. Wnioski Analiza sekwencyjna fragmentu genu nfxB pałeczek Pseudomonas aeruginosa opornych na fluorochinolony (CI, OF, PE, SO, NX) pozwoliła na wykrycie 3 typów mutacji punktowych: Glu(GAA)124→Ala(GCC), Arg(CGC)82→Leu(CTC), Ala(GCA)15→Val(GTA) oraz 7 typów mutacji cichych. Najczęściej wykrywaną mutacją w badanym genie nfxB pałeczek ropy błękitnej była mutacja punktowa: Glu-124→Ala, którą stwierdzono u wszystkich poddanych sekwencjonowaniu szczepów. Stwierdzono, że szczepy pałeczki ropy błękitnej wykazujące obecność mutacji w genie nfxB izolowane były w większości z materiału klinicznego pochodzącego od pacjentów hospitalizowanych niż leczonych ambulatoryjnie. Nabywanie oporności na antybiotyki, może odbywać się na drodze mutacji w bakteryjnym genomie. Ze względu na szybki cykl replikacyjny drobnoustrojów, spontaniczne mutacje punktowe oraz rearanżacje materiału genetycznego, mogą być przyczyną powstawania szczepów opornych, a stosowany antybiotyk może odgrywać rolę selekcjonera, pozwalającego na wzrost jedynie tym komórkom, które prezentują oporność. Piśmiennictwo 1. Bedearden DT, Danziger LH. Mechanizm ��������������������������������� of action of and resistance to quinolones. Pharmacotherapy 2001; 21 (10): 224-232. 2. Betlejewska-Kielak K, Fiett J. Nowe fluorochinolony w leczeniu bakteryjnych zakażeń układu oddechowego. Nowa Klinika Antybiotykoterapia 2001; 8: 925-927. 3. Carewicz R. Fluorochinolony w zakażeniach układu oddechowego. Nowa Klinika 1999; 6(3): 338-340. 4. Gniadkowski M, Gryko R, Grzybowski J i wsp. Pałeczki Gram-ujemne niefermentujące glukozy (rodzaje: Pseudomonas, Burkholderia, Stenotrophomonas i Acinetobacter) Grzybowski J, Reiss J. Praktyczna bakteriologia lekarska i sanitarna. Dom Wydawniczy Bellona. Warszawa 2001. 5. Hryniewicz W, Sulikowska A, Szczypa K i wsp. Rekomendacje doboru testów do oznaczania wrażliwości bakterii na antybiotyki i chemioterapeutyki. Diagn Lab 2004; 40: 41-64. 6. Hryniewicz W, Mészáros J. Antybiotyki w profilaktyce i leczeniu zakażeń. Wydawnictwo Lekarskie PZWL. Warszawa 2001. 7. Jalal S, Ciofu O, Hoiby N i wsp. Molecular ������������������������������� mechanisms of fluoro- 292 quinolone resistance in Pseudomonas aeruginosa isolates from cystic fibrosis patients. Antimicrob Agents Chemother 2000; 44: 710-712. 8. Jalal S, Wretling B. Mechanisms of quinolone resistance in clinical strains of Pseudomonas aeruginosa. Microb Drug Resist 1998; 4(4): 257-261. 9. Kugelberg E, Löfmark S, Wretlind B i wsp. ��������������������� Reduction of the fitness burden of quinolone resistance in Pseudomonas aeruginosa. J Antimicrob Chemother 2005; 55: 22-30. 10. Laudy AE, Starościak BJ. ß – laktamazy pałeczek z rodziny Pseudomonadaceae. Postępy Mikrobiol 2000; 39: 99-132. 11. Lomovskaya O, Warren MS, Lee A i wsp. Identyfication ������������������������ and characterization of inhibitors of multidrug resistance efflux pumps in Pseudomonas aeruginosa: novel agents for combination therapy. Antimicrob Agents Chemother 2001; 45(1):105-116. 12. Nowak K, Suryło P, Kowalski P. Chinolony – przeciwbakteryjne chemioterapeutyki. Farmacja Pol 2002; 58(7): 336-342. 13. Oh H, Stenhoff J, Jalal S i wsp. Role ������������������������������ of efflux pumps and mutations in genes for topoisomerases II and IV in fluoroquinolone – resistant Pseudomonas aeruginosa strains. Microb Drug Resist 2003; 9: 323-328. 14. Romaniszyn D. Pałeczki Gram(-) w zakażeniach szpitalnych. Zakażenia. Antybiotykoterapia 2005; 5: 28-30. 15. Schweitzer HP. Efflux as a mechanizm of resistance to antimicrobials in Pseudomonas aeruginosa and related bacteria: unanswerd questions. Genetics and Molecular Research 2003; 2(1): 48-62. 16. Steciwko A, Kurpas D. Chinolony w praktyce lekarza rodzinnego. Standardy Med 2003; 2(38): 808-812. 17. Wydmuch Z, Pacha J, Kępa M i wsp. Oporność na chinolony wybranych ziarenkowców Gram-dodatnich izolowanych z materiału klinicznego w szpitalu regionu śląskiego. Diagn Lab 2003; 39: 515-521. 18. Wydmuch Z, Pacha J, Kępa M i wsp. Wrażliwość na fluorochinolony szczepów Pseudomonas aeruginosa izolowanych z materiału klinicznego. Med Dośw i Mikrob 2003; 55: 165-171. 19. Wydmuch Z, Skowronek-Ciołek O, Cholewa K i wsp. ��������� Gyr A mutations in ciprofloxacin-resistant clinical isolates of Pseudomonas aeruginosa in a Silesian Hospital in Poland. Polish J Microb 2005; 54(3): 201-206. 20. Ziha-Zarifi I, LLanes C, Kohler T i wsp. In vivo emergence of multidrug-resistant mutants of Pseudomonas aeruginosa overexpressing the active efflux system MexA-MexB-OprM. Antimicrob Agents and Chemother 1999; 43(2): 287-291. Adres Autorów: Laboratorium Analityczne Szpitala Specjalistycznego w Chorzowie ul. Zjednoczenia 10 41-500 Chorzów e-mail: [email protected] (Praca wpłynęła do Redakcji: 2009-02-12) (Praca przekazana do opublikowania: 2009-12-04)