Zastosowanie technologii GPU do rozpoznawania i analizy
Transkrypt
Zastosowanie technologii GPU do rozpoznawania i analizy
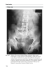
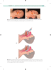
Zastosowanie technologii GPU do rozpoznawania i analizy (np. rezonansu magnetycznego) Karol Miszalski-Jamka Opiekun naukowy: dr hab. prof. UŚ Marcin Kostur I. Prowadzone badania naukowe oraz uzyskane wyniki W okresie ostatniej dekady miał miejsce ogromny postęp technologiczny nieinwazyjnych metod obrazowania układu krążenia. Jest to skutkiem pracy powstających coraz częściej interdyscyplinarnych zespołów złożonych z fizyków, informatyków i lekarzy. Stosowane coraz bardziej zaawansowane technologie dostarczają ogromne ilości danych wymagających z kolei rosnącej mocy obliczeniowej i zaawansowanych strategii postprocessingowych. Z jednej strony coraz bardziej rozwijane są technologie, które po uzyskaniu szczegółowych trójwymiarowych modeli serca i dużych naczyń pozwalają na symulację komputerową przepływu krwi w układzie krążenia. Do takich technologii należy obliczeniowa mechanika płynów CFD (ang. - Computational Fluid Dynamics), a trójwymiarowy model układu krążenia uzyskuje się najczęściej na podstawie obrazów tomografii komputerowej CT (ang. – Computed Tomography) lub rezonansu magnetycznego MRI (ang. – Magnetic Resonance Imaging). Z drugiej strony powstają innowacyjne technologie, które po raz pierwszy pozwalają nieinwazyjnie trójwymiarowo zmierzyć i zobrazować złożone zjawiska przepływowe w układzie krążenia u ludzi in vivo. Takim narzędziem diagnostycznym jest technika 4D kontrastu fazy rezonansu magnetycznego PC-MRI (ang. – Phase Contrast Magnetic Resonance Imaging). Obie wymienione wyżej technologie mogłyby się rozwijać jeszcze szybciej i być powszechniej stosowane w praktyce klinicznej, gdyby nie ogromna moc obliczeniowa której potrzebują. Do uzyskania wiarygodnych wyników potrzeba często wielogodzinnych, a nawet wielodniowych obliczeń, co wymaga zastosowania potężnych komputerów. Jednym z możliwych rozwiązań problemu byłoby wykorzystanie zamiast jednostek centralnych komputerów CPU (Central Processing Unit) architektury GPU (Graphical Processing Units), która umożliwia nawet kilkusetkrotne przyśpieszenie wykonywanych obliczeń. Wykorzystanie mocy obliczeniowej kart graficznych w zastosowaniach nie związanych tylko z wyświetlaniem grafiki umożliwia zastosowanie technologii CUDA (Compute Unified Device Architecture). Wykorzystanie technologii GPU wymaga jednak innego niż klasyczne podejścia do obliczeniowej dynamiki płynów. Zamiast numerycznego rozwiązywania równania Naviera-Stokesa, na klastrach GPU lepiej sprawdza się metoda siatkowa Boltzmanna LBM (ang. – Lattice Boltzmann Method). Jest to alternatywne podejście do problemu numerycznej symulacji płynów. Dzięki prostocie implementacji warunków brzegowych i lokalności obliczeń metoda ta dość dobrze skaluje się w implementacjach równoległych. Metodę LBM wykorzystuje się już z dobrym skutkiem do symulacji przepływów w układzie krążenia u ludzi, m.in. do oceny tętniaków tętnic wewnątrzczaszkowych.1 Obie wymienione strategie wykorzystania architektury GPU oraz metody siatkowej Boltzmanna wykorzystuje m. in. otwarty pakiet oprogramowania Sailfish, który jest ciągle rozwijany w ramach zespołu zajmującego się projektem dot. symulacji biomedycznych. Celem badań w ramach niniejszego projektu jest docelowo wykorzystanie metody siatkowej Boltzmana implementowanej na klastrach GPU do symulacji zjawisk przepływowych w układzie krążenia u ludzi. Wykorzystanie dwóch podejść do obliczeniowej mechaniki płynów CFD, klasycznego numerycznego rozwiązywania równania NavieraStokesa oraz alternatywnego LBM pozwoli na bezpośrednie porównanie head-to-head wyników uzyskanych przy pomocy obu metod. Oba podejścia są symulacjami i do walidacji obliczeń potrzebne jest narzędzie umożliwiające jak najbardziej dokładny pomiar i trójwymiarową analizę rzeczywistych zjawisk przepływowych zachodzących w układzie krążenia. Jako metodę walidacji wybrano wspomnianą już powyżej technologię 4D kontrastu fazy rezonansu magnetycznego PC-MRI. Technika 4D kontrastu fazu rezonansu magnetycznego PC-MRI umożliwia pomiar prędkości przepływającej krwi we wszystkich trzech kierunkach przestrzennych w czasie trwania całego cyklu pracy serca (stąd nazwa 4D: 3D + czas). Metoda pomiaru opiera się na fakcie, że zmiana fazy ΔΦ protonów poruszających się wzdłuż zewnętrznego gradientu pola magnetycznego jest wprost proporcjonalna do ich prędkości ν, zgodnie z równaniem2: gdzie γ oznacza współczynnik żyromagnetyczny. Zrekonstruowane obrazy posiadają rozdzielczość przestrzenną ok. 2,5mm x 2,5mm x 4,5mm i pozwalają w czasie 20-30 minutowej akwizycji uzyskać obrazy z całego serca i aorty piersiowej u danego pacjenta. Technika ta posiada rozdzielczość czasową ok. 40-50ms, a zatem pozwala uzyskać 20-25 faz w obrębie całego cyklu pracy serca (w zależności od tętna spoczynkowego pacjenta, średnio ok. 70 uderzeń/min). Podstawowym ograniczeniem metody wydaje się konieczność uśredniania danych z kilkunastu następujących po sobie cykli pracy serca. Uśrednione dane mają jednak pewną zaletę praktyczną, są bardziej powtarzalne u konkretnego pacjenta i łatwiejsze do porównania między pomiarami w różnym czasie. Uzyskane obrazy charakteryzują się niezbyt dużym stosunkiem sygnału do szumu SNR (Signal to Noise Ratio), stąd wiele wysiłku poświęcono na optymalizację odpowiednich parametrów wykorzystywanej sekwencji MRI (m.in. optymalizacja czasu echa TE, czasu relaksacji TR, prędkości kodowania VENC, wybór optymalnej wielkości voxela jako wypadkowej grubości warstwy, FOV oraz matrycy). Poniżej zamieszczono obrazy PC-MRI uzyskane przy pomocy skanera 1,5 Tesla Avanto (Siemens, Erlangen, Niemcy) dzięki uprzejmości Zakładu Radiodiagnostyki, Instytut Onkologii w Gliwicach. Ryc. 1. Poszczególne składowe wektora prędkości przepływającej krwi przez aortę piersiową zdrowego ochotnika w czasie jednej fazy cyklu pracy serca zobrazowane przy pomocy techniki kontrastu fazy PC-MRI. Z zestawu uzyskanych obrazów 4D każda faza cyklu pracy serca została zrekonstruowana przy pomocy programu mri-flower. Pola prędkości zostały następnie zapisane w formacie VTK. Poniżej zamieszczono wizualizację uzyskaną przy pomocy programu ParaView poprzez nałożenie dwóch obrazów magnetyzacji (format DICOM) oraz pola prędkości (format VTK). Ryc. 2. Wizualizacja pola prędkości przepływającej krwi przez aortę piersiową oraz prawy i lewy przedsionek serca (zdrowy ochotnik jak na Ryc. 1). Kolejnym wykonywanym zadaniem było stworzenie trójwymiarowego modelu aorty piersiowej na podstawie obrazów tomografii komputerowej CT, a następnie przeprowadzenie symulacji komputerowej przepływu krwi wykorzystując obliczeniową mechanikę płynów CFD. Do symulacji wybrano pacjenta z tętniakowatym poszerzeniem aorty wstępującej, schorzeniem które często wymaga zabiegu kardiochirurgicznego o podwyższonym ryzyku, a jednym z kluczowych elementów jest wybór optymalnego czasu interwencji zanim dojdzie do pęknięcia ściany aorty. W literaturze jest opisanych coraz więcej prób użycia technologii CFD do oszacowania ryzyka pęknięcia ściany tętniaka.3 Wykorzystując obrazy tomografii komputerowej dokonano najpierw segmentacji aorty piersiowej (Ryc. 3). Dla uproszczenia nie modelowano zastawki aortalnej. Do symulacji komputerowej przepływu krwi użyto platformy OpenFOAM, algorytm SIMPLE. Numeryczne rozwiązanie równania Naviera-Stokesa wykonano metodą objętości skończonych. Ryc. 3. Segmentacja aorty piersiowej przedstawiona przy pomocy programu Inspace, w prawym dolnym rogu widoczna wizualizacja modelu aorty w obrębie klatki piersiowej. Dla potrzeb obliczeń przyjęto m.in. następujące założenia: - gęstość krwi ϱ = 1,050 g/cm3 - lepkość kinematyczna krwi ν = 0,033 cm2/s - prędkość symulowanego płynu na ściance wynosi zero (=brak poślizgu) - na wlocie zadano stałą prędkość v = 1,5 m/s - na wylotach założono swobodny wypływ krwi Uzyskane wyniki przedstawiono jako pole prędkości w każdym punkcie aorty piersiowej i tętnic dogłowowych odchodzących od łuku aorty (Ryc. 4A) oraz jako rozkład naprężeń ścinających na ściankach aorty (Ryc. 4B). Ryc. 4. Wizualizacja pola prędkości (A) oraz rozkładu naprężeń ścinających WSS (B) w obrębie aorty piersiowej. Zwracają uwagę podwyższone wartości naprężeń ścinających w zakresie ścian tętniaka aorty wstępującej. Mam nadzieję, że badanie zjawisk przepływowych w sercu i w naczyniach krwionośnych pozwoli na lepsze zrozumienie złożonej patofizjologii układu krążenia i w przyszłości będzie wykorzystywane do opracowania skuteczniejszych i bardziej zindywidualizowanych metod terapeutycznych. II. Formy upowszechniania wyników: Wyniki prowadzonych badań zostały dotychczas zaprezentowane na następujących konferencjach i są punktem wyjścia do dalszych analiz: 1. The Rationale for Different Cut-off Values of Non-Compacted to Compacted Ratio in the Diagnosis of Left Ventricular Non-Compaction. American College of Cardiology ACC, Chicago, USA, 24-27 marzec 2012 2. Paradoxical Increase in Left Ventricular Twist in Patients With Left Ventricular NonCompaction With Preserved Ejection Fraction. EuroCMR Annual Meeting, Vienna, Austria, 17-19 maj 2012 Praca #2 zaprezentowana w trakcie EuroCMR Annual Meeting, Vienna, Austria, 17-19 maj 2012 zdobyła Nagrodę „Best Poster Presentation Award”. Literatura: 1 Bernsdorf J, Wang D. Non-Newtonian blood flow simulation in cerebral aneurysms. Computers & Mathematics with Applications 2009;58:1024–9 2 Lotz J, Meier C, Leppert A, Galanski M. Cardiovascular Flow Measurement with PhaseContrast MR Imaging: Basic Facts and Implementation. RadioGraphics 2002; 22:651–671 3 Georgakarakos E, Ioannou CV, Papaharilaou Y, Kostas T, Katsamouris AN. Computational evaluation of aortic aneurysm rupture risk: what have we learned so far? J Endovasc Ther 2011;18:214-25.