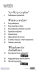plik PDF - Wydział Biologii i Biotechnologii
Transkrypt
plik PDF - Wydział Biologii i Biotechnologii
dr Beata Kurowicka Katedra Fizjologii Zwierząt Wydział Biologii i Biotechnologii Uniwersytet Warmińsko-Mazurski w Olsztynie ul. Oczapowskiego 1A 10-719 Olsztyn tel. (089) 523 42 18 e-mail: [email protected] AUTOREFERAT OPIS DOROBKU I OSIĄGNIĘĆ NAUKOWYCH 1. Imię i Nazwisko Beata Kurowicka 2. Posiadane dyplomy, stopnie naukowe Praca magisterska 1991 – „Analiza stanu mikrobiologicznego wód kompleksu Wielkich Jezior Mazurskich” Promotor: dr Aleksander Świątecki. Zakład Mikrobiologii i Immunologii, Wydział Matematyczno-Przyrodniczy, Wyższa Szkoła Pedagogiczna w Olsztynie Rozprawa doktorska 1997 – „Dywergencja wydolności termoregulacji u szczurów wyhodowanych w chłodzie i cieple” Promotor: prof. dr hab. Michał Caputa, Zakład Fizjologii Zwierząt, Wydział Biologii i Nauk o Ziemi, Uniwersytet M. Kopernika w Toruniu 3. Informacje o dotychczasowym zatrudnieniu w jednostkach naukowych/ artystycznych 1991 – 1998 r. Katedra Biologii Ogólnej, Instytut Biologii, Wydział MatematycznoPrzyrodniczy, Wyższa Szkoła Pedagogiczna w Olsztynie (asystent) 1993-1997 r. Studia doktoranckie na Wydziale Biologii i Nauk o Ziemi, Uniwersytet M. Kopernika w Toruniu, Zakład Fizjologii Zwierząt 1998 – 1999 r. Katedra Biologii Ogólnej, Instytut Biologii, Wydział MatematycznoPrzyrodniczy, Wyższa Szkoła Pedagogiczna w Olsztynie (adiunkt) 1999 – 2013 r. Katedra Fizjologii Zwierząt, Wydział Biologii, Uniwersytet WarmińskoMazurski w Olsztynie (adiunkt) 2014 r. – obecnie Katedra Fizjologii Zwierząt, Wydział Biologii i Biotechnologii, UWM w Olsztynie (asystent) 2 4. Wskazanie osiągnięcia wynikającego z art. 16 ust. 2 ustawy z dnia 14 marca 2003 r. o stopniach naukowych i tytule naukowym oraz o stopniach i tytule w zakresie sztuki (Dz. U. nr 65, poz. 595 ze zm.): a) tytuł osiągnięcia naukowego: Oddziaływanie wysokiej temperatury otoczenia w okresie neonatalnym na rozwój układu rozrodczego i funkcjonowanie osi przysadka-jądra u samców szczura b) publikacje wchodzące w skład osiągnięcia (przy publikacjach podano punkty MNiSW wg Komunikatu Ministra Nauki i Szkolnictwa Wyższego w sprawie wykazu czasopism naukowych z dnia 23. grudnia 2015 r. oraz roku wydania. IF podano z roku wydania, a dla publikacji z 2015 r. i 2016 r. IF podano z 2015 r.) 1. Kurowicka B, Gajewska A, Amarowicz R, Kotwica G (2008) Effect of warm-rearing and heat acclimation on pituitary-gonadal axis in male rats. International Journal of Andrology 31(6): 579-587. (MNiSW2008 = 24 pkt, MNiSW2015 = 50 pkt, IF = 4,021) Mój wkład w powstanie publikacji: jestem autorem korespondencyjnym, przygotowałam pracę do druku, miałam wiodący udział w planowaniu eksperymentów i znaczący udział w wykonaniu eksperymentów, przeprowadzeniu analizy jakościowej oraz w analizie statystycznej, interpretacji i opracowaniu wyników. Swój udział w powstawaniu publikacji szacuję na 60%. 2. Kurowicka B, Dietrich G, Kotwica G (2015) Effect of neonatal or adult heat acclimation on testicular and epididymal morphometry and sperm production in rats. Reproductive Biology 15(1):1-8. doi: 10.1016/j.repbio.2015.01.001 (MNiSW2015 = 15 pkt, IF = 1,722) Mój wkład w powstanie publikacji: jestem autorem korespondencyjnym, przygotowałam pracę do druku, miałam wiodący udział w planowaniu eksperymentów i znaczący udział w wykonaniu eksperymentów, przeprowadzeniu analizy jakościowej oraz w analizie statystycznej, interpretacji i opracowaniu wyników. Swój udział w powstawaniu publikacji szacuję na 75%. 3. Kurowicka B, Chrusciel M, Zmijewska A, Doroszko M, Kotwica G, Rahman NA (2015) Distinct testicular steroidogenic response mechanisms between neonatal and adult heatacclimated male rats. Cellular Physiolology and Biochemistry. 35(5):1729-1743. doi: 10.1159/000373985. (MNiSW2015 = 25 pkt, IF = 4,652) Mój wkład w powstanie publikacji: jestem autorem korespondencyjnym, przygotowałam pracę do druku, miałam wiodący udział w planowaniu eksperymentów i znaczący udział w wykonaniu eksperymentów, przeprowadzeniu analizy jakościowej oraz w analizie statystycznej, interpretacji i opracowaniu wyników. Swój udział w powstawaniu publikacji szacuję na 72%. 4. Kurowicka B, Chrusciel M, Zmijewska A, Kotwica G (2016) Effect of neonatal or adult heat acclimation on plasma T3 level, testicular thyroid receptors expression in male rats and testicular steroidogenesis in vitro in response to triiodothyronine treatment. Polish Journal of Veterinary Science, 19: 379-386. (MNiSW2015 = 20 pkt, IF = 0,719) Mój wkład w powstanie publikacji: jestem autorem korespondencyjnym, przygotowałam pracę do druku, miałam wiodący udział w planowaniu eksperymentów i znaczący udział w wykonaniu eksperymentów, przeprowadzeniu analizy jakościowej oraz w analizie statystycznej, interpretacji i opracowaniu wyników. Swój udział w powstawaniu publikacji szacuję na 80%. Razem liczba punktów MNiSW z roku wydania = 84 liczba punktów MNiSW z roku 2015 = 110 Szacunkowy sumaryczny IF = 11,114 Oświadczenia współautorów o udziale własnym w przygotowaniu prac stanowiących szczególne osiągnięcia naukowe w załączniku nr 7. 3 c) omówienie celu naukowego/artystycznego ww. pracy/prac i osiągniętych wyników wraz z omówieniem ich ewentualnego wykorzystania Wpływ środowiska na kształtowanie się fenotypu organizmu stanowi w ostatnich latach znaczącą część badań ekologicznych, ewolucyjnych lecz również tych, związanych ze zdrowiem człowieka. Udział środowiska w przebiegu procesów rozwojowych organizmu, określany jako plastyczność fenotypowa, objawia się poprzez intensywnie badane mechanizmy epigenetycznej modyfikacji ekspresji genów podczas rozwoju embrionalnego oraz znacznie słabiej poznane mechanizmy kształtujące fenotyp osobnika, pod wpływem środowiska, w okresie neonatalnym. Plastyczność fenotypowa oznacza stopień do jakiego doświadczenia, zbierane przez organizm w trakcie rozwoju ontogenetycznego, w różnych warunkach środowiska zewnętrznego, wpływają na jego fenotyp. Oznacza to zatem możliwość kształtowania różnych fenotypów na podstawie jednego genotypu, w zależności od odmiennych warunków środowiskowych. Siła oddziaływania poszczególnych elementów środowiska na kształtowanie fenotypu zależy od wrażliwości organizmu podczas jego rozwoju na działanie danego czynnika. Wrażliwość ta dotyczy tzw. wartości krytycznych danego czynnika środowiskowego (wielkość zmiany danego elementu środowiska wywołująca zmiany fenotypu) oraz istnienia tzw. okien czasowych w trakcie rozwoju osobniczego, podczas których czynnik środowiskowy może wpływać na ostateczny fenotyp osobnika. Są to tzw. okresy krytyczne w kształtowaniu się poszczególnych cech fenotypu. Jednym z istotnych dla funkcjonowania organizmu czynników środowiska jest temperatura otoczenia. U ssaków i ptaków układ regulacji temperatury zapobiega wahaniom temperatury wnętrza ciała podczas zmian temperatury otoczenia. Ponieważ rozwój tego układu kształtuje się podczas życia płodowego i po urodzeniu, możliwe jest zatem dostosowanie czynności tego układu do środowiska termicznego, czyli podlega on programowaniu przez środowisko w okresie rozwoju. U zwierząt laboratoryjnych, hodowanych w niskiej bądź wysokiej temperaturze, wielokrotnie stwierdzano nieodwracalne modyfikacje odruchowej odpowiedzi na temperaturę otoczenia, podczas kształtowania się ich układu regulacji temperatury. Moje wcześniejsze badania naukowe koncentrowały się właśnie na ocenie wpływu podwyższonej lub obniżonej temperatury otoczenia podczas rozwoju ontogenetycznego szczurów na czynność układu regulacji temperatury [1, 2, 3]. Stwierdziłam podwyższenie set-point temperatury organizmu, wyższą odporność na hipertermię oraz obniżoną aktywność mechanizmów obrony przed zimnem u szczurów hodowanych w wysokiej temperaturze otoczenia w okresie neonatalnym. 4 Inspiracją do następnego etapu moich badań (już po osiągnięciu stopnia doktora nauk biologicznych), było wykazanie przez innych Autorów na wielu modelach doświadczalnych upośledzenia czynności rozrodczych samców podczas ich ekspozycji na gorąco (Ryc. 1). Gonady dorosłych samców poddane hipertermii Wyższa śmiertelność potomstwa Niedotlenienie i niedokrwienie jąder Stres oksydacyjny Apoptoza spermatocytów i spermatyd Degeneracyjne zmiany nabłonka plemnikotwórczego Dorosłe samce aklimowane do gorąca Wzrost aktywności enzymów szlaku steroidogenezy w jądrach oraz metabolizmu steroidów w wątrobie Obniżone stężenie testosteronu we krwi obwodowej Obniżone stężenie LH, prolaktyny i T3/T4 we krwi obwodowej Niepłodność lub obniżona płodność Rycina 1. Najważniejsze skutki działania wysokiej temperatury na organizm dojrzałych płciowo samców. Ich konsekwencją jest niepłodność lub obniżona płodność samców. Bazując na wynikach moich poprzednich doświadczeń dotyczących plastycznego dostosowania układu regulacji temperatury szczurów - po nabyciu umiejętności badania układu rozrodczego - postawiłam hipotezę, że u samców szczura hodowanych od urodzenia w wysokiej temperaturze otoczenia zmiany czynności układu rozrodczego nie muszą być tak znaczne, jak w przypadku ekspozycji dorosłych samców na gorąco (Ryc. 1). Weryfikacja tej hipotezy stanowiła główny cel podjętych przeze mnie badań, przedstawionych w niniejszym opracowaniu. Kolejnym celem było wyjaśnienie, czy zmiany morfologii i czynności jąder samców, hodowanych w gorącu od urodzenia, są nieodwracalne podczas deaklimacji, czyli spełniają kryteria plastyczności fenotypowej. Nie bez wpływu na podjęcie przeze mnie tych badań były także liczne doniesienia o spadającej produkcji plemników w jądrach współczesnych mężczyzn i wpływie przegrzewania gonad na to zjawisko. Przegrzewanie gonady może być powodowane, między innymi, siedzącym trybem życia, stylem ubierania się, lub też używaniem pieluch jednorazowych w okresie niemowlęcym. Badania prowadziłam na samcach szczura norweskiego (Rattus norvegicus) rasy Wistar, podzielonych na cztery grupy doświadczalne. Grupę pierwszą stanowiły samce kontrolne (CR) – urodzone i hodowane w temperaturze otoczenia 20 C przez 90 dni. Drugą grupę (NHA/WR) stanowiły samce aklimowane do gorąca w okresie neonatalnym, czyli urodzone i hodowane w temperaturze otoczenia 34 C przez 90 dni. Badałam również trwałość przystosowań układu rozrodczego samców do wysokiej temperatury otoczenia, poprzez ocenę czynności i morfologii układu rozrodczego samców urodzonych w wysokiej temperaturze otoczenia (34 C) i po osiągnięciu dojrzałości płciowej (45 dzień życia) przeniesionych do temperatury standardowej (20 C) na okres 45 dni (grupa deaklimowana - DA). Porównanie morfologii i czynności układu 5 rozrodczego samców pod wpływem neonatalnej aklimacji do wysokiej temperatury otoczenia oraz aklimacji dorosłych samców do takiej temperatury, umożliwiła grupa samców dorosłych aklimowanych do gorąca, czyli samców urodzonych w temperaturze otoczenia 20 C i po osiągnięciu dojrzałości płciowej (45 dzień życia) poddanych aklimacji do temperatury 34 C przez kolejne 45 dni (AHA/WA). Schemat aklimacji termicznej szczurów grup doświadczalnych przedstawia rycina 2. poród dojrzewanie płciowe 0 45 uśmiercanie i pobieranie tkanek 90 Grupy Dni Ta = 20 C CR Ta = 20 C Ta = 34 C AHA/WA Ta = 34 C NHA/WR DA Ta = 34 C Ta = 20 C Rycina 2. Schemat grup doświadczalnych. CR – samce kontrolne wyhodowane w temperaturze otoczenia (Ta) równej 20 C, AHA/WA – samce aklimowane do gorąca (Ta=34 C) po osiągnięciu dojrzałości płciowej; NHA/WR – samce aklimowane do gorąca (Ta=34 C) w okresie neonatalnym; DA – samce deaklimowane w temperaturze otoczenia 20 C po osiągnięciu dojrzałości płciowej. Linia ciągła i przerywana oznaczają czas utrzymywania zwierząt w określonej temperaturze. Środowisko może wpływać na regulację ekspresji genów poprzez zmiany w produkcji hormonów oraz metylacji DNA lub potranslacyjnych modyfikacji białek histonowych. W badaniach innych autorów wykazano, że regulacja hormonalna leży u podstaw plastyczności rozwojowej. Z tego powodu, pierwszym etapem moich badań była ocena stężenia hormonów gonadotropowych, prolaktyny i steroidów płciowych oraz hormonów tarczycy u samców szczurów badanych grup doświadczalnych [1, 2, 4]. Na ty etapie prowadzonych badań wykazałam: podwyższone stężenie LH we krwi obwodowej szczurów aklimowanych do gorąca po osiągnięciu dojrzałości płciowej [1, 2] oraz tych aklimowanych do gorąca w okresie neonatalnym [2], jak również szczurów deaklimowanych [1] w stosunku do szczurów kontrolnych; podwyższenie stężenia FSH we krwi obwodowej szczurów aklimowanych do gorąca w okresie neonatalnym [2] i deaklimowanych [1] oraz prolaktyny (PRL) [1, 2] we krwi obwodowej szczurów aklimowanych do gorąca w okresie neonatalnym w porównaniu do samców kontrolnych i aklimowanych do gorąca po osiągnięciu dojrzałości płciowej; brak wyraźnych zmian w stężeniu hormonów płciowych (androstendionu, testosteronu, estradiolu-17 ) w osoczu samców aklimowanych do gorąca, oprócz nieznacznie obniżonego stężenie androstendionu (A4) w osoczu samców aklimowanych do gorąca w okresie 6 neonatalnym [1, 2] i testosteronu (T) w osoczu samców aklimowanych do gorąca po osiągnięciu dojrzałości płciowej [1]; obniżenie stężenia wolnej trijodotyroniny (fT3) we krwi obwodowej szczurów poddanych działaniu gorąca, niezależnie od okresu rozwojowego zwierząt [4]. Stwierdziłam również, że obniżenie aktywności wydzielniczej tarczycy, u szczurów poddanych neonatalnej ekspozycji na wysoką temperaturę, ma charakter trwały i nie zmienia się pod wpływem aklimacji szczurów do temperatury kontrolnej (grupa szczurów deaklimowanych). Podsumowując, wyniki te wskazują na, zależne od fazy rozwoju układu rozrodczego podczas ekspozycji na wysoką temperaturę otoczenia, zmiany w regulacji czynności przysadki i gruczołu tarczowego samców. Ciekawym jest, że zmiany te nie wpływały jednak znacząco na endokrynną czynność jąderoraz nie były spowodowane reakcją stresową na niekorzystną temperaturę otoczenia, gdyż stężenie kortykosteronu we krwi krążącej nie różniło się pomiędzy szczurami z badanych grup. Siła oddziaływania hormonów na tkanki docelowe zależy, między innymi, od gęstości swoistych receptorów tych hormonów w komórkach tkanek docelowych. Dlatego też, w jądrach szczurów grup doświadczalnych sprawdziłam ekspresję receptorów LH, prolaktyny i T3, po inkubacji skrawków jąder in vitro w warunkach kontrolnych, jak również w odpowiedzi na egzogenny ligand danego receptora. W badaniach tych wykazałam: wzrost podstawowej ekspresji mRNA receptorów LH, jedynie u szczurów deaklimowanych, przy jednoczesnym hamowaniu ekspresji tego receptora przez LH. W pozostałych grupach doświadczalnych egzogenne LH stymulowało ekspresję mRNA tego receptora [2]; brak zmian ekspresji mRNA długiej formy receptora prolaktyny (Prlr1, jest to forma aktywna w transdukcji sygnału prolaktynowego) w jądrach samców aklimowanych do gorąca oraz wzrost ekspresji mRNA krótkiej formy receptora prolaktyny (Prlr2, forma nieaktywna w procesie transdukcji sygnału prolaktynowego) w jądrach samców aklimowanych do gorąca podczas okresu neonatalnego [2]; wzrost ekspresji mRNA receptora 1 hormonów tarczycy (Thra1) w podstawowych warunkach inkubacji skrawków jąder samców aklimowanych do gorąca w okresie neonatalnym i deaklimowanych w porównaniu do ekspresji tego genu w jądrach samców kontrolnych oraz wzrost ekspresji mRNA receptora 1 (Thrb1) w skrawkach jąder samców deaklimowanych w porównaniu do innych grup doświadczalnych [4]. Podsumowując, wyniki te wskazują, że w jądrach samców szczurów, hodowanych w gorącu podczas rozwoju układu rozrodczego, dochodzi do dostosowania poziomu ekspresji receptorów PRL i T3 do zmienionych ilości krążących w osoczu ligandów tych receptorów. 7 Kolejnym zagadnieniem, które badałam, była ocena wpływu wysokiej temperatury otoczenia w różnych okresach rozwoju szczurów na syntezę hormonów płciowych przez izolowane komórki Leydiga [1]. W badaniach tych wykazałam: wyższą podstawową sekrecję A4 przez komórki Leydiga szczurów aklimowanych do gorąca po osiągnięciu dojrzałości płciowej oraz niższą podstawową sekrecję T przez komórki Leydiga samców aklimowanych do gorąca niezależnie od okresu rozwojowego (grupy AHA/WA, NHA/WR oraz DA); wyższą sekrecję E2 przez komórki Leydiga samców aklimowanych do gorąca w okresie neonatalnym; niższą wrażliwość komórek Leydiga samców aklimowanych do gorąca w okresie neonatalnym na egzogenny LH; iż obniżenie aktywności steroidogenezy w komórkach Leydiga samców aklimowanych do gorąca po osiągnięciu dojrzałości płciowej, może zachodzić na wczesnych etapach procesu, poprzedzających powstawanie pregnenolonu, gdyż dodanie tego hormonu do inkubowanych komórek Leydiga samców tej grupy znacznie podwyższało produkcję steroidów. Podsumowując, wyniki te wskazują na różnice w aktywności enzymów szlaku syntezy hormonów steroidowych w jądrach samców aklimowanych do gorąca w różnych okresach rozwoju układu rozrodczego. Powyższe wyniki skłoniły mnie do podjęcia kolejnych badań, w których oceniłam ekspresję mRNA i aktywność enzymów szlaku syntezy hormonów steroidowych1. Do realizacji tego celu użyłam skrawków jąder samców doświadczalnych, które poddano krótkotrwałej (8h) inkubacji in vitro. Badałam podstawową, jak również stymulowaną przez LH, PRL i T3, ekspresję i aktywność białka StAR oraz enzymów szlaku syntezy hormonów steroidowych [2, 4]. Badania te wykazały: obniżenie podstawowej ekspresji mRNA białka StAR w jądrach szczurów aklimowanych do gorąca po osiągnięciu dojrzałości płciowej. W pozostałych grupach poddanych ekspozycji na wysoką temperaturę otoczenia ekspresja ta nie ulegała zmianie; 1 Szlak syntezy steroidów w jądrach składa się z następujących po sobie reakcji enzymatycznych prowadzonych przez następujące białka i enzymy: - StAR – białko umożliwiające transport cholesterolu do wewnętrznej błony mitochondrium, - CYP11A1 – desmolaza C20-22 cholesterolowa, przekształcająca cholesterol do pregnenolonu, - HSD3B1 – dehydrogenaza 3 -hydroksysteroidowa/ 5- 4 izomeraza typ 1 – przekształca pregnenolon w progesteron, - CYP17A1 – 17 hydroksylaza/17-20 liaza - przekształca progesteron do androstendionu, HSD17B3 – dehydrogenaza 17 hydroksysteroidowa typ3 - przekształca androstendion w testosteron, CYP19A1 – aromataza – przekształca testosteron do estradiolu-17 . 8 wzrost podstawowej ekspresji mRNA genów Cyp11a1 i Hsd3b1 w jądrach szczurów aklimowanych do gorąca przed osiągnięciem dojrzałości płciowej (grupy NHA/WR i DA), jednak bez zmiany aktywności enzymów, kodowanych przez te geny, w obu grupach; obniżenie podstawowej ekspresji genu Cyp19a1 u szczurów aklimowanych do gorąca w okresie neonatalnym oraz po osiągnięciu dojrzałości płciowej, jak również aktywności aromatazy w jądrach szczurów aklimowanych do gorąca przed osiągnięciem dojrzałości płciowej (grupy NHA/WR i DA); wzrost ekspresji Cyp11a1 w jądrach szczurów aklimowanych do gorąca w okresie neonatalnym i po osiągnięciu dojrzałości płciowej oraz Hsd17b3 w jądrach samców aklimowanych do gorąca po osiągnięciu dojrzałości płciowej, bez wpływu na aktywność enzymów, kodowanych przez te geny, podczas krótkotrwałej ekspozycji na LH; wzrost aktywności enzymów HSD3B1, CYP17A1 oraz brak hamowania aktywności enzymu CYP19A1 przez LH, dodane do inkubowanych in vitro skrawków jąder samców aklimowanych do gorąca przed osiągnięciem dojrzałości płciowej (grupy NHA/WR i/lub DA); wzrost ekspresji mRNA oraz aktywności enzymu CYP17A1 w skrawkach jąder samców aklimowanych do gorąca przed osiągnięciem dojrzałości płciowej (grupy NHA/WR i/lub DA) pod wpływem egzogennej PRL; brak stymulującego wpływu T3 na ekspresję mRNA białka StAR tylko w jądrach samców aklimowanych do gorąca po osiągnięciu dojrzałości płciowej; hamowanie, przez T3, ekspresji Cyp11a1 w skrawkach jąder samców aklimowanych do gorąca przed osiągnięciem dojrzałości płciowej (grupy NHA/WR i DA) oraz podwyższenie ekspresji Hsd17b3 w skrawkach jąder samców aklimowanych do gorąca w okresie neonatalnym; iż znany efekt hamowania transkrypcji genu Cyp19a1 przez T3 był słabiej wyrażony w jądrach samców aklimowanych do gorąca w okresie neonatalnym; brak pozagenomowego wpływu T3 na aktywność enzymów steroidogenezy oraz sekrecję steroidów przez inkubowane skrawki jąder samców grup doświadczalnych. Podsumowując, konsekwencją wykazanych zmian ekspresji i aktywności enzymów szlaku syntezy hormonów steroidowych, była wyższa w warunkach podstawowych, jak i po stymulacji LH, sekrecja A4 w jądrach samców aklimowanych do gorąca w okresie neonatalnym oraz sekrecja T i E2 przez skrawki jąder szczurów wszystkich grup poddanych aklimacji do gorąca w porównaniu do jąder samców kontrolnych. Nie stwierdziłam natomiast wpływu PRL i T3 na sekrecję steroidów w żadnej z grup doświadczalnych [2, 4]. Powyższe wyniki, w porównaniu do uzyskanych po inkubacji izolowanych komórek Leydiga samców grup doświadczalnych, wykazały istotną rolę współzależności między tkanką śródmiąższową a komórkami kanalika nasiennego podczas syntezy i uwalniania hormonów steroidowych u szczurów poddanych 9 aklimacji do gorąca, niezależnie od okresu rozwojowego. Potwierdziły one również, że w komórkach Leydiga, samców aklimowanych do gorąca po osiągnięciu dojrzałości płciowej, przebieg steroidogenezy może być hamowany na etapie dostępności białka StAR. Badanie syntezy hormonów steroidowych w jądrach samców poddanych ekspozycji na wysoką temperaturę otoczenia w różnych okresach rozwojowych pozwoliło wykazać, że szkodliwy wpływ tego czynnika środowiskowego jest kompensowany poprzez zmiany ekspresji poszczególnych enzymów szlaku syntezy steroidów i wrażliwości komórek Leydiga na badane hormony (LH, PRL i T3). W konsekwencji, umożliwia to utrzymanie w miarę prawidłowego stężenia steroidów we krwi obwodowej szczurów długotrwale aklimowanych do gorąca. Jednocześnie stwierdziłam, że przystosowania u szczurów dorosłych, poddanych działaniu gorąca, różnią się w porównaniu do szczurów hodowanych w gorącu przed osiągnięciem dojrzałości płciowej. Wykazałam jednak, że efekt końcowy, czyli produkcja hormonów steroidowych i ich stężenie we krwi obwodowej są podobne w obu przypadkach. Najważniejszą funkcją gonad samców jest produkcja plemników, wspierana przez hormony płciowe. Od dawna wiadomo, że wysoka temperatura gonady powoduje u dorosłych samców zaburzenia produkcji plemników, aż do czasowej niepłodności włącznie. W okresie przed podjęciem przeze mnie niniejszych badań, nieznane były możliwości adaptacji procesu spermatogenezy do wysokiej temperatury otoczenia w okresie ostatecznego kształtowania się kanalika nasiennego, czyli przed okresem dojrzałości płciowej. W celu zbadania tego problemu dokonałam oceny procesu spermatogenezy poprzez morfometryczną charakterystykę histologicznych skrawków jąder i najądrzy samców doświadczalnych, ocenę liczebności plemników zgromadzonych w ogonie najądrza oraz ich aktywności ruchowej u szczurów kontrolnych, aklimowanych do gorąca w okresie dojrzałości płciowej, w okresie postnatalnego rozwoju układu rozrodczego oraz samców deaklimowanych [1, 2, 3]. W wyniku podjętych badań wykazałam: zmniejszenie masy jąder u samców wszystkich grup poddanych działaniu wysokiej temperatury otoczenia, niezależnie od okresu rozwojowego [1, 2], przy równoległym zmniejszeniu masy ciała. W konsekwencji, indeks gonado-somatyczny (GSI) nie ulegał znaczącym zmianom w żadnej grupie doświadczalnej [1, 2]; zmiany względnej masy narządów układu rozrodczego samców hodowanych w gorącu obejmujące: − zmniejszenie względnej masa głowy najądrza oraz zwiększenie masy ogona najądrza u szczurów aklimowanych do gorąca w okresie neonatalnym w porównaniu do szczurów kontrolnych [3], 10 − rozrost pęcherzyków nasiennych i brzusznej prostaty, szczególnie u szczurów poddanych działaniu wysokiej temperatury w okresie przed osiągnięciem dojrzałości płciowej (grupy NHA/WR i DA) [3], zaburzenia struktury i morfometrii kanalików nasiennych jąder samców aklimowanych do gorąca po osiągnięciu dojrzałości płciowej oraz samców deaklimowanych, obejmujące: − zmniejszenie powierzchni kanalików nasiennych jader dorosłych samców aklimowanych do gorąca i samców deaklimowanych, obniżenie częstości stadium XI-XIV cyklu kanalika nasiennego oraz zmniejszenie liczby komórek Sertoliego w kanalikach nasiennych jądra u szczurów aklimowanych do gorąca po osiągnięciu dojrzałości płciowej, − obecność degeneracyjnych zmian nabłonka nasiennego, aż do całkowitego zaniku aktywnej spermatogenezy w jądrach samców aklimowanych do gorąca po osiągnięciu dojrzałości płciowej; zmiany te obejmowały 17,6 7,4% przekrojów kanalików nasiennych, − zmniejszenie pola powierzchni kanalika najądrza od końcowych segmentów głowy do końcowych segmentów ogona tego narządu u samców aklimowanych do gorąca po osiągnięciu dojrzałości płciowej; towarzyszył im wzrost powierzchni nabłonka kanalikowego i spadek powierzchni zajmowanej przez plemniki, obniżenie liczebności plemników w ogonie najądrza samców aklimowanych do gorąca po osiągnięciu dojrzałości płciowej; zmiany parametrów ruchu plemników z ogona najądrza samców aklimowanych do gorąca w okresie neonatalnym, obejmujące obniżoną prędkość ruchu krzywoliniowego oraz amplitudy bocznych wychyleń główki plemnika. Podsumowując, wykazałam, że przebieg spermatogenezy jądrowej jest bardziej zaburzony u samców poddanych aklimacji do gorąca po osiągnięciu dojrzałości płciowej niż u samców poddanych aklimacji w okresie neonatalnym. Jednocześnie u szczurów aklimowanych do gorąca podczas rozwoju układu rozrodczego stwierdziłam przerost gruczołów rozrodczych dodatkowych, który stanowił najbardziej widoczny, niekorzystny efekt działania wysokiej temperatury na morfologię układu rozrodczego tej grupy szczurów. PODSUMOWANIE KOŃCOWE W przedstawionych badaniach wykazałam, że wysoka temperatura otoczenia w okresie neonatalnym wpływa na kształtowanie się oraz czynność układu rozrodczego samców szczura poprzez zmiany regulacji aktywności wydzielniczej przysadki i gruczołu tarczowego. Jednocześnie zmiany stężenia hormonów gonadotropowych, prolaktyny i T3 mogą być częściowo kompensowane zmianami ekspresji receptorów dla tych hormonów w jądrach oraz ekspresji i 11 aktywności enzymów szlaku syntezy hormonów steroidowych. Prowadzi to do utrzymania prawie nie zmienionego stężenia steroidów płciowych we krwi obwodowej. Prawidłowa regulacja produkcji hormonów steroidowych umożliwia również prawidłowy przebieg procesu spermatogenezy, a w konsekwencji utrzymanie prawidłowej liczebności plemników w ogonie najądrza. Najwyraźniejszym skutkiem negatywnym działania gorąca, podczas kształtowania się układu rozrodczego samców szczura, jest rozrost gruczołów płciowych dodatkowych i zaburzenie aktywności ruchowej plemników. Część różnic w ekspresji i aktywności enzymów szlaku syntezy A. Przebieg steroidogenezy Zmiany stężenia LH, FSH, steroidów płciowych, prolaktyny i fT3 we krwi obwodowej Samce aklimowane do gorąca po osiągnięciu dojrzałości płciowej Przez izolowane komórki Leydiga T Zmiany ekspresji receptorów LH, prolaktyny i T3 w jądrach Zmiany sekrecji hormonów Przez skrawki jąder A4 Samce aklimowane do gorąca po osiągnięciu dojrzałości płciowej T, E2 Samce aklimowane do gorąca w okresie neonatalnym A4, Prlr2 PRL T LH, A4 Samce aklimowane do gorąca w okresie neonatalnym E2 Samce deaklimowane Samce deaklimowane FSH Zmiany ekspresji i aktywności enzymów szlaku syntezy steroidów w jądrach warunkach podstawowych i po stymulacji: Samce aklimowane do gorąca w okresie neonatalnym B. Brak zmian indeksu gonado-somatycznego Hsd3b1, CYP19A1 Cyp19a1 Cyp11a1 HSD3B1, CYP17A1 PRL T3 Samce deaklimowane Cyp11a1, Hsd17b3 Thrb1 Lhr Samce aklimowane do gorąca po osiągnięciu dojrzałości płciowej Star LH Thra1 fT3 Cyp17a1, CYP17A1 Hsd17b3 Cyp11a1 Morfologia układu rozrodczego i jej zaburzenia Samce aklimowane do gorąca po osiągnięciu dojrzałości płciowej Samce aklimowane do gorąca w okresie neonatalnym Zmiany względnej masy gruczołów dodatkowych Samce deaklimowane Liczebności plemników w ogonie najądrza Zaburzenia struktury i morfometrii kanalików nasiennych Prędkości ruchu krzywoliniowego i amplitudy bocznych wychyleń główki plemnika Rycina 3. Schemat opracowany na podstawie wyników własnych, uzyskanych podczas badania aktywności osi przysadka–jądro (A) oraz morfologii układu rozrodczego i przebiegu spermatogenezy (B) w jadrach samców aklimowanych do gorąca po osiągnięciu dojrzałości płciowej, samców aklimowanych do gorąca w okresie neonatalnym oraz samców deaklimowanych po osiągnięciu dojrzałości płciowej. oznaczają odpowiednio podwyższenie lub spadek danej wartości stwierdzonej w grupie doświadczalnej w porównaniu do tej wartości stwierdzonej w grupie kontrolnej. Cyp11a – sposób oznaczenia ekspresji mRNA badanego genu, CYP11A1 – sposób oznaczenia aktywności enzymu kodowanego przez badany gen. steroidów w jądrach, wykazanych przeze mnie, pomiędzy szczurami poddanymi neonatalnej ekspozycji na wysoką temperaturę oraz szczurami kontrolnymi, wydaje się być nieodwracalna 12 poprzez proces deaklimacji. Przykładowo, podstawowa ekspresja Cyp11a1 i Hsd3b1 lub regulowana prolaktyną ekspresja i aktywność CYP17A1 są podobnie zmienione w jądrach szczurów deaklimowanych, jak w jądrach szczurów aklimowanych do gorąca w okresie neonatalnym. Wydaje się, że badanie regulacji aktywności promotora tych genów może stanowić atrakcyjny cel kolejnych doświadczeń, które pogłębią wiedzę o relacjach między środowiskiem a rozwijającym się układem rozrodczym. Poddanie dorosłych samców szczura działaniu wysokiej temperatury otoczenia w dłuższym okresie czasu również modyfikuje czynność osi przysadka - jądro oraz ekspresję i aktywność enzymów szlaku syntezy steroidów. Jednakże modyfikacje te różnią się w porównaniu do tych stwierdzonych u szczurów eksponowanych na gorąco w okresie neonatalnym. Jednocześnie u dorosłych samców szczura poddanych aklimacji do gorąca stwierdza się zaburzenie procesu produkcji plemników oraz ich liczby w ogonie najądrza. Takich zmian nie wykazałam u szczurów poddanych neonatalnej aklimacji do gorąca. Sugeruje to istnienie mechanizmów plastycznego dostosowania regulacji przebiegu spermatogenezy, lub też innych niedostrzeżonych do tej pory mechanizmów, zapobiegających jego zaburzeniom. Przedstawioną, na początku opracowania, hipotezę badawczą potwierdziłam wynikami przedstawionymi powyżej (rycina 3), a dalsze poszukiwanie możliwych przyczyn lepszego dostosowania układu rozrodczego samców aklimowanych do wysokiej temperatury w okresie neonatalnym stanowi cel planowanych, przeze mnie, w przyszłości badań . 5. Omówienie pozostałych osiągnięć naukowo - badawczych (wykaz omawianych publikacji podano na końcu akapitu) 5.1. Czynność układu regulacji temperatury szczurów w warunkach endotoksemii i stresu termicznego Opracowano i przetestowano metodę oceny górnej temperatury krytycznej (CTmax) u szczurów, której podstawą jest ocena zachowania zwierzęcia podczas ekspozycji na wysoką temperaturę otoczenia. Test ten umożliwia przyżyciowe badanie CTmax bez konieczności uśmiercania zwierząt. Zbadano CTmax u szczurów hodowanych od urodzenia w wysokiej temperaturze otoczenia i porównano z wynikami uzyskanymi u szczurów kontrolnych oraz szczurów otrzymujących różne dawki lipopolisacharydu bakteryjnego [2, 3]. Wykazano, iż bardzo wysokie = toksyczne dawki lipopolisacharydu (LPS) ze ścian bakterii gram ujemnych, choć zwiększają śmiertelność zwierząt doświadczalnych, to nie upośledzają czynności układu regulacji temperatury. Wyniki przeprowadzonych badań nie potwierdziły udziału LPS, pochodzącego ze ścian bakterii jelitowych, w zaburzeniach mechanizmów termoregulacji i w konsekwencji śmierci cieplnej w warunkach szoku termicznego [3, 4]. Stwierdzono również zmiany w stężeniu osoczowych lipoprotein w odpowiedzi na stres termiczny oraz LPS [3]. 5.2. Czynność układu oksytocyna/receptor oksytocyny w układzie rozrodczym świni podczas cyklu rujowego i wczesnej ciąży oraz cyklu rujowym u krowy 13 Wykazano zmiany w ekspresji receptora oksytocyny w macicy świń pomiędzy 14-16 dniem cyklu rujowego a 14-16 dniem ciąży oraz w jajowodzie krów w przebiegu cyklu rujowego [5, 6]. Wykazano zależne od ekspresji receptora oksytocyny, zmiany w aktywności skurczowej mięśniówki macicy świń oraz jajowodu krów. Zbadano również wpływ progesteronu na aktywność skurczową mięśniówki macicy świń w 14-16 dniu cyklu rujowego i wczesnej ciąży [6, 7]. Wykazano wpływ oksytocyny na ekspresję enzymów szlaku syntezy prostaglandyny F2 i E2 oraz produkcję obu prostaglandyn przez mięśniówkę i śluzówkę macicy świń z okresu luteolizy i wczesnej ciąży. Wykazano również wpływ progesteronu na szlak przekazywania sygnału przez oksytocynę w mięśniówce i śluzówce macicy świń w obu okresach reprodukcyjnych [8, 9, 10, 11]. 5.3. Wykazanie wpływu oksytocyny na oś podwzgórze-przysadka-nadnercza dojrzałych płciowo loszek - badania in vivo i in vitro. Oksytocyna w warunkach in vitro zwiększa sekrecję hormonów tropowych przysadki (ACTH, PRL i LH) oraz -endorfiny z komórek przedniego płata przysadki świń z fazy lutealnej cyklu rujowego [12]. Oksytocyna podawana i.v. zwiększa stężenie kortyzolu i kortykosteronu w osoczu loszek, wzrost koncentracji glikokortykoidów był wyższy u loszek w fazie lutealnej niż w pęcherzykowej cyklu rujowego [13, 14]. Oksytocyna in vitro zwiększa sekrecję kortyzolu przez komórki kory nadnerczy uzyskane od loszek w fazie lutealnej cyklu rujowego [13, 14]. 5.4. Udział oksytocyny w regulacji wydzielania progesteronu przez ciałko żółte świni Stwierdzono, że oksytocyna stymuluje produkcję progesteronu przez komórki lutealne świń z 8-10 dnia cyklu rujowego poprzez wzrost hydrolizy fosfatydyloinozytolu i następnie zwiększenie stężenia wewnątrzkomórkowych jonów Ca2+ [15]. 5.5. Udział czynników procesu zapalnego w regulacji produkcji prostaglandyn przez błonę śluzową i mięśniową macicy świń w okresie cyklu rujowego i wczesnej ciąży Wykazano udział TNF , IL1β i IL6 w regulacji syntezy, uwalniania oraz metabolizmu prostaglandyny F2α przez endometrium świń i możliwość udziału tych cytokin w mechanizmie ochrony ciałka żółtego w okresie wczesnej ciąży oraz luteolizie ciałka żółtego podczas cyklu rujowego świń [16]. Zbadano udział IL1β w regulacji syntezy prostaglandyny E2 przez śluzówkę i mięśniówkę macicy świń podczas cyklu rujowego i wczesnej ciąży. Wykazano stymulujący wpływ badanej cytokiny na ekspresję enzymów szlaku syntezy PGE2 oraz wzrost sekrecji badanej prostaglandyny przez śluzówkę i mięśniówkę macicy świń ciężarnych z dni 10-11 oraz 12-13 lecz nie w dniach 14-15. Śluzówka i mięśniówka macicy we wszystkich badanych dnia cyklu rujowego wydzielała więcej PGE2 pod wpływem IL1 β, przy zróżnicowanym wpływie badanej cytokiny na ekspresję enzymów szlaku syntezy PGE2 co wskazuje na możliwość akumulacji prostaglandyny E2 w mięśniówce [17]. 5.6. Wpływ środowiska termicznego w okresie życia postnatalnego na czynność układu rozrodczego samic szczurów 14 Hodowla samic szczurów w wysokiej temperaturze otoczenia w okresie neonatalnym (WR) powoduje opóźnienie dojrzewania płciowego, lecz nie wpływa na długość cykli płciowych samic szczura. Jednocześnie wywołuje wzrost stężenia PRL i progesteronu oraz obniżenie stężenia FSH w osoczu samic w fazie metaestrus cyklu rujowego. Zmianom tym odpowiada wyższa sekrecja progesteronu przez ciałka żółte samic WR zarówno w warunkach podstawowych jak i w odpowiedzi na LH [18]. Wykaz prezentowanych publikacji 1. Caputa M, Demicka A, Dokladny K, Kurowicka B (1996) Anatomical and physiological evidence for efficacious selective brain cooling in rats. Journal of thermal Biology 2(1): 21-28. (Praca opublikowana przed doktoratem) 2. Caputa M, Dokladny K, Kurowicka B (1998) Behavioral approeach to the study of the upper limit of temperature tolerance in rats. Physiology & Behavior 65: 183-189. 3. Caputa M, Dokladny K, Kurowicka B (2000) Endotoxaemia does not limit heat tolerance in rats: the role of plasma lipoproteins. European Journal of Applied Physiology 82:142-50. 4. Caputa M, Dokładny K, Kurowicka B, Rogalska J (2004) Brain and body temperature changes and behavior of rats injected with various doses of endotoxin. Acta Biologica Cracoviensia Series Zoologia 46:13-25. 5. Oponowicz A, Franczak A, Kurowicka B, Kotwica G (2006) Relative transcript abundance of oxytocin receptor gene in porcine uterus during luteolysis and early pregnancy. Journal of Applied Genetics 47: 345-351. 6. Kotwica G, Kurowicka B, Franczak A, Grzegorzewski W, Wrobel M, Mlynarczuk J, Kotwica J (2003). The concentrations of catecholamines and oxytocin receptors in the oviduct and its contractile activity in cows during the estrous cycle. Theriogenology 60:953-64. 7. Kurowicka B, Franczak A, Oponowicz A, Kotwica G (2005): In vitro contractile activity of porcine myometrium during luteolysis and early pregnancy: effect of oxytocin and progesterone. Reproductive Biology 5: 151-169. 8. Franczak A, Kurowicka B, Oponowicz A, Petroff BK, Kotwica G (2006): The effect of progesterone on oxytocin-stimulated intracellular mobilization of Ca2+ and prostaglandin E2 and F2 secretion from porcine myometrial cells. Prostaglandins & other Lipid Metabolics 81 (1-2): 37-44. 9. Franczak A, Wocławek-Potocka I, Oponowicz A, Kurowicka B, Kotwica G (2004) Oxytocin stimulates prostaglandin F2 secretion and prostaglandin F synthase protein expression in porcine myometrial tissue. Reproductive Biology 4: 177-184. 10. Franczak A, Kotwica G, Kurowicka B, Oponowicz A, Wocławek-Potocka I, Petroff BK (2006) Expression of enzymes of cyclooxygenase pathway and secretion of prostaglandyn E2 and F2 by porcine myometrium during luteolysis and early pregnancy. Theriogenology 66: 1049-1056. 11. Kotwica G, Oponowicz A, Kurowicka B, Franczak A, Bogacka I 2010 The effect of progesterone on oxytocin-stimulated intracellular Ca2+ mobilisation and prostaglandin secretion in porcine endometrium. Polish Journal of Veterinary Sciences 13: 615-622. 12. Kotwica G, Staszkiewicz J, Skowroński MT, Siawrys G, Bogacka I, Franczak A, Kurowicka B, Kraziński B, Okrasa S (2006) Effects of oxytocin alone and in combination with selected hypothalamic hormones on the ACTH, -endorphin, LH and PRL secretion by anterior pituitary cells of cyclic pigs. Reproductive Biology 6: 115-131. 15 13. Kotwica G, Franczak A, Okrasa S, Koziorowski M, Kurowicka B (2002): Effects of mating stimuli and oxytocin on plasma cortisol concentration in gilts. Reproductive Biology 2: 25-37. 14. Kotwica G, Kamińska B, Franczak A, Kurowicka B, Staszkiewicz J, Skowroński M, Kraziński B, Okrasa S (2004) The effect of oxytocin on cortisol and corticosterone secretion in cyclic gilts – in vivo and in vitro studies. Reproductive Biology 4: 35-50. 15. Franczak A, Kurowicka B, Kowalik M, Ciereszko RE, Kotwica G (2009): The effect of oxytocin on progesterone secretion, phosphoinositide hydrolysis and intracellular mobilisation of Ca2+ in porcine luteal cells. Acta Veterinaria Hungarica 57: 115-125. 16. Franczak A, Zmijewska A, Kurowicka B, Wojciechowicz B, Kotwica G (2010) Interleukin 1β-induced synthesis and secretion of prostaglandin E2 in the porcine uterus during various periods of pregnancy and the estrous cycle. Journal of Physiology and Pharmacology 61:73342. 17. Franczak A, Zmijewska A, Kurowicka B, Wojciechowicz B, Petroff BK, Kotwica G (2012) The effect of tumor necrosis factor α (TNFα), interleukin 1β (IL1β) and interleukin 6 (IL6) on endometrial PGF2α synthesis, metabolism and release in early-pregnant pigs. Theriogenology 77: 155-165. 18. Kurowicka B, Gajewska A, Franczak A (2006) Effect of early thermal experience on pituitary-gonadal axis in female rats. Reproductive Biology 6: 63-77. 16