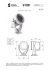Automatyczna analiza ilościowa cytologicznych obrazów
Transkrypt
Automatyczna analiza ilościowa cytologicznych obrazów
AUTOMATYCZNA ANALIZA ILOŚCIOWA
CYTOLOGICZNYCH OBRAZÓW MIKROSKOPOWYCH
WOJCIECH BIENIECKI, SZYMON GRABOWSKI
Katedra Informatyki Stosowanej Politechniki Łódzkiej, Al. Politechniki 11, Łódź
Streszczenie: Niniejszy artykuł powstał dzięki
współpracy Katedry Informatyki Stosowanej z
Instytutem Patomorfologii Akademii Medycznej w
Łodzi. Praca opisuje techniki przetwarzania
kolorowych obrazów biomedycznych na przykładzie cytologicznych obrazów mikroskopowych.
Techniki te obejmują redukcję defektów obrazu
powstałych podczas akwizycji obrazu oraz zakłóceń
wynikłych z niedoskonałości preparatu mikroskopowego. Praca opisuje także proces kwantyzacji i
segmentacji badanego obrazu.
Omówiono projekt systemu informatycznego
wspomagającego pracę laboranta wykonującego
analizę ilościową badanego materiału cytologicznego.
W dalszej części pracy przedstawiono wybrane
metody rozpoznawania obrazu mogące mieć
zastosowanie
dla
obrazów
cytologicznych.
Szczególny nacisk położono na statystyczne
metody rozpoznawania obrazów, w tym metodę k
najbliższych sąsiadów (k-NN).
Słowa kluczowe: obrazy cytologiczne, segmentacja,
k-NN.
1. Badania patomorfologiczne
1.1. Istota badania
Do badania raka sutka wykorzystuje się
następujące techniki pozyskiwania materiału:
- wycinek tkanki histologiczny –
podczas badania śródoperacyjnego;
pobrany
- odcisk tkanki
(inprint);
szkiełku
- rozmaz
BAC).
(biopsja
na
zamrożonym
aspiracyjna
cienkoigłowa
Badanie przeprowadza się w celu wykrycia w
komórkach nowotworowych receptorów estrogenowych (ER) i progesteronowych (PR). Obecność
tych receptorów kwalifikuje pacjentkę do dalszego
leczenia. W celu stwierdzenia obecności
receptorów w jądrach komórkowych raka, materiał
biologiczny barwi się immunohistochemicznie.
Jądra komórkowe wykazujące ekspresję dodatnią
receptorów barwią się na kolor brunatno-czerwony,
podczas gdy pozostałe jądra komórkowe pozostają
nie zabarwione i mają kolor niebieski (barwnik ten
to hematoksylina Mayera).
Badanie
histopatologiczne
jest
metodą
najdokładniejszą, jednak pozyskanie i przygotowanie preparatu jest kłopotliwe. Skrawany jest płat o
grubości 4 mikronów i umieszczany na szkiełku
mikroskopowym. Dzięki takiej obróbce widoczna
na preparacie tkanka guza tworzy wyraźne pola,
łatwe do odróżnienia od tkanki zdrowej. W badaniu
tym, ze względu na dobrą jakość tkanki, można
naliczyć 500–700 jąder komórkowych i określić ich
ekspresję.
Preparat cytologiczny zawiera wymieszane
komórki zdrowe i nowotworowe, jądra komórkowe
nie otoczone cytoplazmą, krwinki czerwone i
struktury niekomórkowe, takie jak śluz, włókna,
masy martwicze, skrzepy krwi i włóknika.
Wyodrębnienie jąder komórek nowotworowych i
określenie ich ekspresji jest kłopotliwe i wymaga
analizy większej powierzchni preparatu niż w
przypadku
badania
histologicznego,
gdyż
pojedynczy obraz mikroskopowy zazwyczaj
obejmuje zbyt małą liczbę jąder. Następnie
obliczana jest frakcja jąder zawierających receptory
i na tej podstawie stawia się diagnozę. Do zbadania
pozostaje skuteczność tej metody, tj. określenie, na
ile takie badanie jest porównywalne z badaniem
wycinka tkanki, a co za tym idzie, ile jąder
komórkowych należy brać pod uwagę i z jaką
dokładnością należy policzyć frakcję jąder o
dodatniej ekspresji.
1.2. Przebieg pomiaru podczas rutynowych
badań patomorfologicznych
1. Przygotowanie
odpowiedniej
ilości
preparatów. Od pacjentki pobiera się materiał
na jeden preparat histologiczny, jeden preparat
typu inprint i 1–2 preparaty rozmazowe. Na
każdym szkiełku połowę materiału barwi się
odczynem reagującym z ER i połowę
odczynem reagującym z PR.
2. Umieszczenie pod mikroskopem preparatu i
wykonanie pewnej ilości zdjęć. Do liczenia
jąder komórkowych stosuje się powiększenie
400x. Wybieramy te zdjęcia, na których jądra
komórkowe nie są ze sobą zlepione i można
wydzielić granice pomiędzy nimi, aby
dokładnie je policzyć. Ruch stolika
mikroskopowego
powinien
być
tak
zaplanowany, aby
wybór fragmentów
preparatu był możliwie przypadkowy, a
jednocześnie,
aby
zaobserwować
jak
największą ilość jąder komórkowych. W
przypadku materiału histopatologicznego
wystarczy wydzielić obszary nie zawierające
tkanki zdrowej.
3. Liczenie jąder komórkowych. Etap ten
wymaga sporej uwagi. Pomijając obszary
zawierające nie rozdrobnioną tkankę, a
skupiając się tylko na jądrach komórkowych
pływających swobodnie, należy ustalić
dodatkowe założenia:
a. jak traktować jądra komórkowe
wykazujące częściową ekspresję;
b. jak liczyć jądra komórkowe, jeśli nie są
widoczne w całości na ekranie (tu
można np. odrzucać obiekty).
2. Zadania półautomatycznego
systemu komputerowego
Celem naszych badań jest skonstruowanie w
pełni automatycznego systemu analizy obrazów
patomorfologicznych. Wymaga to rozwiązania
szeregu problemów, a zatem na etapie
projektowania niezbędna jest interakcja z
człowiekiem (lekarzem lub laborantem).
Poniżej podajemy fazy działania interakcyjnego
systemu.
1. akwizycja obrazów z kamery analogowej
poprzez kartę telewizyjną do komputera PC i
digitalizacja obrazów;
obrysu jądra komórkowego pozwoli obliczyć
jego objętość;
6. klasyfikacja jąder komórkowych: jądra z
ekspresją, jądra bez ekspresji, jądra z
częściową ekspresją. Ewentualna pomoc
operatora;
7. wykonanie
analizy
statystycznej
(w
najprostszym przypadku: obliczenie frakcji,
określenie maksymalnego błędu).
3. Techniki przetwarzania obrazu
Omówione poniżej techniki przetwarzania
obrazu mikroskopowego podzieliliśmy na trzy
grupy:
przetwarzanie
wstępne
eliminujące
większość defektów powstałych w procesie
akwizycji, segmentacja obiektów w obrazie i
analiza obrazu.
3.1. Przetwarzanie wstępne
Obraz mikroskopowy obserwowany przez
laboranta przechwytywany jest przez kamerę wideo
podłączoną do mikroskopu. Laborant może oglądać
obraz na żywo na ekranie monitora i odpowiednio
dostroić oświetlenie oraz ostrość obrazu.
Ustawienia tych parametrów mają istotny wpływ na
przydatność obrazu do dalszego przetwarzania.
Następnym etapem jest „wykonanie zdjęcia”, czyli
zapisanie obrazu w postaci cyfrowej w pamięci
komputera. Podczas tego procesu nieunikniona jest
częściowa utrata informacji, którą obrazuje Rys. 1.
2. obróbka wstępna obrazów polegająca na
eliminacji zakłóceń powstałych podczas
akwizycji, a także wyrównanie histogramu
jasności. Dzięki takiej obróbce algorytm
dokonujący segmentacji przy różnych
obrazach będzie działał w porównywalnych
warunkach;
3. określenie
parametrów
barwnych
i
morfologicznych obiektów, które będą
poszukiwane na obrazie. Krok ten może być
wspomagany przez operatora systemu, zaś
uzyskane dane zostają dołączane do zbioru
uczącego;
4. automatyczna
segmentacja
obrazu
na
podstawie powyższych kroków. Program musi
wydzielić rozłączne obszary zawierające po
jednym jądrze komórkowym. Obszary te będą
weryfikowane przez operatora systemu;
5. obrysowanie jąder komórkowych przy użyciu
algorytmów progowania. Dokładne określenie
Rys. 1. Digitalizacja obrazu. Proces składa się z dwóch etapów:
próbkowania i kwantyzacji. Podczas digitalizacji następuje
zmniejszenie rozdzielczości przestrzennej i barwnej
Rys. 2 przedstawia powiększony fragment
zdigitalizowanego obrazu pozyskanego podczas
rutynowego badania cytologicznego. Wyraźnie
dostrzegalne są m. in. następujące artefakty:
poziome prążki (efekt przeplotu), kolorowe paski z
lewej strony obrazu (zakłócenia synchronizacji
poziomej obrazu), rozmycie krawędzi obiektów
(skutek złego ustawienia ostrości).
Najprostszym rozwiązaniem, zastosowanym w
naszym systemie, jest wyrównanie histogramu
jasności, czyli liniowe przeskalowanie jasności.
Analizowany obraz cyfrowy jest dodatkowo
odszumiany poprzez filtr medianowy zastosowany
dla składowej jasności obrazu. Przeprowadzono
eksperymenty z maskami medianowymi różnej
wielkości. Dla analizowanych obrazów o
rozdzielczości 700 x 525 punktów, optymalną
maską dla filtru medianowego wydaje się być
maska kołowa o średnicy 7 punktów.
Należy zwrócić uwagę na fakt, iż w tej fazie
przetwarzania nie zajmujemy się poprawą ostrości
obrazu.
3.1. Segmentacja w dziedzinie kolorów
Rys 2. Powiększony fragment zdigitalizowanego obrazu
cytologicznego. Widoczne zakłócenia spowodowane są
niedoskonałością toru wizyjnego.
W analizie obrazów kolorowych najczęściej
stosuje się model barwny HSI (Hue, Saturation,
Intensity) – Rys. 3.
Efekt przeplotu jest spowodowany sposobem
kodowania obrazu w systemie telewizyjnym PAL.
Cykl tworzenia i przesyłania obrazu trwający 1/25
sek. składa się z dwóch półobrazów, jeden zawiera
linie parzyste, drugi nieparzyste. W rezultacie linie
parzyste nie są skanowane w tym samym czasie, co
linie nieparzyste. Dodatkowo, złe ustawienie
parametrów przechwytywania karty telewizyjnej
może spowodować, że zostanie zapisany tylko
jeden półobraz.
Efekt przeplotu można
następującymi metodami:
próbować
usunąć
-
poprzez wybranie co drugiej linii obrazu i
interpolację pozostałych linii;
Rys 3. Stożek barwny modelu HSI.
-
uśrednianie eliminujące również szum.
Wykonuje się N zdjęć tego samego obrazu.
Statystycznie wartość szumu rośnie wówczas
Model ten lepiej odzwierciedla ludzką percepcję
kolorów niż schemat RGB, standardowo używany
do kodowania obrazów. Barwniki użyte w
preparacie cytologicznym mają specyficzne zakresy
kolorów, możliwe do opisania w modelu HSI przez
składową H, czyli ton barwy.
N razy, podczas gdy wartość sygnału
rośnie N razy. Powoduje to procentowy
spadek szumu w obrazie;
-
poprzez zastosowanie filtru medianowego
współrzędnej pionowej.
Brzegi
obrazu,
na
których
powstają
charakterystyczne zakłócenia barwne, można
usunąć, zmniejszając tym nieznacznie powierzchnię
analizowanego obrazu.
Ze względu na fakt, iż obrazy mogą mieć
niedoskonałości związane z nieprawidłowym
oświetleniem, zastosowano również korekcję
jasności obrazu. Pole preparatu może być
oświetlone nierównomiernie (np. środek może być
oświetlony mocniej niż brzegi), dodatkowo każdy
obraz z analizowanego preparatu może być
oświetlony innym natężeniem. Nierównomierność
ta może wpływać na proces segmentacji.
zabarwienie
brunatno-czerwone
(ekspresja dodatnia)
niebieskie
(ekspresja ujemna)
zakres składowej H
[280; 360] i [0; 10]
[180; 280]
Tab. 1: Zakresy wartości składowej H (dla jąder kom.)
mierzone w przykładowym obrazie cytologicznym.
Podane w Tab. 1 zakresy wartości nie są,
niestety, stałe dla wszystkich obrazów użytych w
eksperymencie. Co gorsza, ze względu na opisane
powyżej defekty obrazów, zakresy te dla
wyróżnionych obiektów (tj. rodzajów zabarwień)
mogą częściowo się pokrywać. Na Rys. 4 pokazano
wynik działania algorytmu opartego na progowaniu
wartości
H
dla
przykładowego
obrazu
cytologicznego. W dalszej części eksperymentu
zastosowano
segmentację
barwną
z
wykorzystaniem algorytmu k-NN (opis w
następnym rozdziale). Jako cechy przyjęto wartości
H, S, I oraz gradient jasności dla każdego punktu.
Segmentacja barwna jest koniecznym, lecz nie
dostatecznym etapem analizy obrazu. Może ona
służyć np. do wstępnego oddzielania obiektów od
tła. Fragmenty obrazu posiadające ton barwy z
przedziału skojarzonego z interesującym nas
zabarwieniem nie muszą należeć do jąder
komórkowych (może to być np. cytoplazma,
krwinki).
Wydzielenie
pojedynczych
jąder
komórkowych
jest
zadaniem
segmentacji
morfologicznej.
3.2. Segmentacja morfologiczna obrazu
Preparaty mikroskopowe używane w rutynowych badaniach patomorfologicznych posiadają
szereg cech utrudniających automatyczną segmentację obrazu. Obiekty często łączą się w większe
grupy, co wymaga zastosowania algorytmów
rozdzielających je. Jednym z nich może być metoda
watershed.
Rys 4. Segmentacja barwna przy użyciu składowej H
dla obrazka cytologicznego. Zastosowano następujące
przedziały wartości H: tło {0,199}, ekspresja ujemna {200,299},
ekspresja dodatnia {300,359}.
Użytkownik programu generuje zbiór uczący
klikając w wybrane przez niego punkty obrazka i
przypisując je do jednej z trzech grup: obiekty z
ekspresją dodatnią, obiekty z ekspresją ujemną oraz
tło. Odległość w przestrzeni cech zdefiniowano
jako sumę modułów różnic poszczególnych
składników koloru i gradientu jasności:
Algorytm watershed został wymyślony dla
potrzeb segmentacji przez Beuchera i Lantuejoula
[6]. Opracowano zarówno sekwencyjną, jak i
równoległą implementację tej metody. Idea
algorytmu polega na traktowaniu obrazka jako
mapy topograficznej, gdzie wysokość oznacza
jasność, gradient jasności lub wartość pewnej
składowej koloru. Algorytm rozpoczyna pracę w
„kotlinach” obszaru, tj. minimach lokalnych. W
każdym
kroku
iteracji
„poziom
wody”
podwyższany jest o 1 dla każdej kotliny i następuje
zalewanie obszarów kotliny niższych niż ten
poziom wody.
ρ(x1,x2) = Hx1 −Hx2 + Sx1 −Sx2 + Ix1 −Ix2 + ∇x1 −∇x2 ,
a więc zastosowano metrykę miejską. Miało to na
celu poprawę wydajności algorytmu.
Wyniki działania algorytmu minimalnoodległościowego 1-NN dla tego samego obrazka prezentuje
Rys. 5.
Rys 5. Segmentacja barwna obrazu cytologicznego
algorytmem 1-NN dla cech H, S, I, grad(I).
Obraz wynikowy zawiera mniejsze zakłócenia,
niż obraz poddany progowaniu barw.
Rys 6. Porównanie metod segmentacji:
a) oryginalny obrazek, b) progowanie, c) watershed.
W momencie, gdy zalewane obszary zbliżają się
do siebie, konstruowane są na ich granicy linie
podziału. Efektywne działanie algorytmu możliwe
jest dla obrazów o małym zaszumieniu, gdyż w
przeciwnym wypadku następuje podział na zbyt
wiele regionów (ang. oversegmentation). Wynik
działania metody zależny jest także od określenia
sąsiedztwa punktów i kierunku zalewania.
jest rozkład histogramu wybranych cech należących
do obiektu punktów (jasności, nasycenia, tonu
koloru). Bardziej skomplikowane metody opisu
tekstury bazują na analizie Fouriera lub na analizie
fraktalnej.
3.4. Pomiar cech morfologicznych
Efekt działania metody watershed pokazano na
Rys. 6. Algorytm został w tym wypadku użyty w
celu rozdzielenia zlepionych obiektów. Wartości
użyte dla tego obrazu to jasności punktów.
Zastosowanie gradientu jasności jest przydatne przy
wyznaczaniu obrysu obiektów.
Przedmiotem eksperymentu medycznego jest
pomiar cech morfologicznych wyróżnionych
obiektów należących do dwóch klas, czyli jąder
komórkowych wykazujących ekspresję dodatnią i
ujemną. Pomiar obejmuje:
- liczbę obiektów widocznych na obrazku;
- pole powierzchni obiektów.
3.3. Analiza obrazów
Pomiar pola powierzchni
Interesujące patologa obiekty, czyli jądra
komórkowe, występują razem z innymi obiektami
opisanymi w rozdziale 1. Formalne opisanie cech
tych obiektów jest trudne, ponieważ w każdym
preparacie mogą wyglądać one nieco inaczej (por.
Rys. 2, 4, 7).
Problemy z pomiarem pola powierzchni jąder
komórkowych wynikają z tego, że preparat jest
pewnym dwuwymiarowym przekrojem przestrzeni
trójwymiarowej, w której znajdują się mierzone
obiekty. Mamy więc tylko przekroje obiektów,
które mogą wprowadzać pewne niedokładności.
Zjawisko to opisuje się jako efekt Holmesa.
Obrazuje je Rys. 8.
Rys. 8. Zniekształcenia wielkości obiektów w preparacie
mikroskopowym. Obiekty A i C są tej samej wielkości, podczas
gdy na preparacie obiekt C będzie większy. Podobna zależność
występuje pomiędzy obiektami B i D.
Rys 7. Fragment obrazu cytologicznego. Wskazano różne
struktury mogące zakłócić działanie automatycznej segmentacji.
Przeprowadzenie tego etapu w sposób
automatyczny
wymaga
metod
sztucznej
inteligencji, np. statystycznych metod rozpoznawania obrazów, sieci neuronowych. Podstawowym
założeniem dla skonstruowania klasyfikatora jest
formalny opis cech obiektów w celu ich
klasyfikacji.
Stosować
można
następujące
parametry morfologiczne:
- pole powierzchni;
- obwód;
- średnice;
- współczynniki kształtu;
- spójność obszaru;
- liczbę otworów.
Analizie podlegać może także tekstura danego
obiektu. Najprostszym sposobem opisania tekstury
Dokładna korekcja wielkości powierzchni jąder
komórkowych jest niemożliwa, gdyż nie widzimy
tak jak na Rys. 7, które jądra komórkowe są
przecięte i w jakiej płaszczyźnie. Można założyć, że
wielkość jąder komórkowych ma pewien rozkład
prawdopodobieństwa i na tej podstawie obliczać
pole powierzchni. Z kolei porównując jasność
obiektów i ostrość ich krawędzi można wykryć
odcinki kul takie jak A, B na Rys. 8 i
wyeliminować je z dalszych obliczeń.
Pomiar liczby obiektów
Pomiar liczby obiektów widocznych na jednym
obrazku powinien uwzględniać przypadki, gdy
pewne obiekty nie mieszczą się w całości na
obrazkach. Stosuje się w tym wypadku pewien
margines (Rys. 9), dzięki któremu możemy
wyróżnić obiekty brzegowe. Znając rozkład
wielkości i gęstość obiektów na obrazku, można
określić statystycznie błąd wynikający z operacji
wyłączania obiektów brzegowych.
W praktyce często testuje się parametr k w
ograniczonym zakresie, np. od 1 do 30. Wartość k,
która oferuje najmniejszą wartość frakcji błędów
klasyfikacji, może być stosowana do klasyfikacji
nowych punktów, czyli punktów spoza zbioru
uczącego.
Rys 9. Określanie obiektów brzegowych obrazka na podstawie
marginesu: a) wyłączamy obiekty leżące całkowicie
na marginesie, b) wyłączamy obiekty leżące częściowo
na marginesie.
4. Rozpoznawanie obrazów metodą
k najbliższych sąsiadów
Nieparametryczna
reguła
decyzyjna
k
najbliższych
sąsiadów
(k-NN)
została
zaproponowana prawie pół wieku temu w pracy [1]
i mimo to wciąż należy do najefektywniejszych
metod klasyfikacji. Klasyfikowanemu punktowi z
przestrzeni cech reguła ta przyporządkowuje klasę
najliczniej reprezentowaną wśród k najbliższych mu
punktów (sąsiadów) w zbiorze odniesienia,
zwanym też zbiorem uczącym. Liczbę k dobiera się
eksperymentalnie tak, aby prawdopodobieństwo
mylnej klasyfikacji było jak najmniejsze.
Zbiór uczący bardzo często zawiera cechy
nadmiarowe, nie mające związku z rozpatrywanymi
klasami. Znany jest fakt, że cechy nadmiarowe
komplikują i pogarszają jakość klasyfikacji. Z tego
powodu pożądane jest przeprowadzanie selekcji
cech. Gdy liczba cech jest niewielka, np. 10, to
wyboru najlepszego zestawu możemy dokonać
drogą pełnego przeglądu wszystkich kombinacji
cech, licząc dla każdej z nich frakcję błędów
odpowiadającą optymalnej wartości k.
W przypadku większej liczby cech stosujemy
często strategię kolejnego dołączania cech (FSS –
Forward Selection Strategy) lub strategię kolejnego
odrzucania cech (BSS – Backward Selection
Strategy). Obie te strategie zostały opisane w pracy
[2]. Opiszmy tylko strategię kolejnego dołączania
cech, gdyż wymaga ona mniejszego nakładu
obliczeń. Pierwszym krokiem tej strategii jest
wybór jednej cechy, która oferuje najmniejszy błąd
klasyfikacji. Następnie do tej cechy, na wszystkie
możliwe sposoby, dołączamy drugą cechę i
wybieramy parę z najmniejszym średnim błędem
klasyfikacji. Trzecią i kolejne cechy dołączamy w
podobny sposób, kończąc na pełnym zestawie cech.
Do klasyfikacji obrazów cytologicznych
używamy następujących czterech cech:
Rys 10. Przykład działania reguły 3-NN.
Próbka q będzie przypisana do klasy „kółek”.
Prawdopodobieństwo
mylnej
klasyfikacji
oszacowuje
się
poprzez
użycie
zbioru
walidacyjnego (ang. validation set) lub metodą
minus jednego elementu (ang. leave-one-out).
Metoda ta polega na klasyfikacji każdego punktu ze
zbioru odniesienia (tj. uczącego) wg reguły k-NN
ze zbiorem odniesienia pomniejszonym o
klasyfikowany aktualnie punkt. Stosunek liczby
mylnie klasyfikowanych w ten sposób punktów do
liczebności całego zbioru odniesienia, czyli frakcja
błędów klasyfikacji, estymuje prawdopodobieństwo
mylnej decyzji. Stosując metodę minus jednego
elementu możemy oszacować frakcje błędów
klasyfikacji dla wszystkich możliwych wartości k.
-
składowe barwne danego punktu H, S oraz I;
-
gradient jasności
punkcie.
estymowany
w
danym
W zadaniu segmentacji barwnej mamy do
czynienia z trzema klasami punktów: należące do
jąder komórkowych „niebieskich”, należące do
jąder „czerwonych” i pozostałe (np. należące do
cytoplazmy). Z analizy statystyk zbioru uczącego
wynika, iż zadanie trójdecyzyjne, z którym mamy
tu do czynienia, można zdekomponować do sieci
trzech zadań dwudecyzyjnych, tj. przypisywać
osobno każdy punkt po kolei tylko do jeden z
dwóch klas. W każdym z podzadań można
wykorzystywać osobne cechy i osobne wartości k
(jak podaliśmy wyżej, te parametry klasyfikacji
estymowane są w procesie uczenia przy pomocy
zbioru uczącego i reguły minus jednego elementu).
Finalna decyzja, tj. przypisanie próbki do jednej z
trzech klas, nastąpi w wyniku głosowania
klasyfikatorów składowych (dwudecyzyjnych).
5. Podsumowanie
Automatyczne systemy analizy obrazów
mikroskopowych są projektami bardzo złożonymi i
kosztownymi, tak więc nieliczne ośrodki badawcze
mogą sobie pozwolić na ich zakup. Celem
współpracy Katedry Informatyki Stosowanej
Politechniki Łódzkiej i Instytutu Patomorfologii
Akademii Medycznej jest stworzenie systemu
opartego o posiadany sprzęt komputerowy i
optyczny
oraz
technologie
wykonywania
preparatów mikroskopowych. Dlatego też obecnie
dążymy do stworzenia systemu informatycznego
półautomatycznego, wspomagającego uciążliwy dla
laboranta etap liczenia jąder komórkowych i
porządkującego otrzymane wyniki. Dalsze plany
przewidują poprawę algorytmów korekcji błędów
obrazu (np. braku ostrości), algorytmów
segmentacji oraz identyfikacji obiektów.
6. Bibliografia
[1] Fix E., Hodges J. L., Discriminatory Analysis: Nonparametric Discrimination Small Sample Performance. From
project 21-49-004, Report Number 11, USAF School of
Aviation Medicine, Randolph Field, Texas, pp. 280–322,
1952.
[2] Devijver P. A., Kittler J., Pattern Recognition: A Statistical
Approach. Prentice Hall, London, 1982.
[3] Gonzales R., Woods W., Digital Image Processing. Addison
Wesley, 1993.
[4] Teuber J., Digital Image Processing. Teknisk Forlag,
Copenhagen, Denmark 1989.
[5] Zieliński K., Strzelecki M., Komputerowa analiza obrazu
biomedycznego. PWN, W-wa, Łódź, 2002.
[6] Beucher S., Lantuejoul C., Use of watersheds in contour
detection. In Proc. International Workshop on Image
Processing, Real-Time Edge and Motion Detection/
Estimation, Rennes, Sept. 1979.
Internet
[http1] I. T. Young, J. J. Gerbrands, L. J. van Vliet Fundamentals of
Image Processing, http://www.ph.tn.tudelft.nl/Courses/FIP/
noframes/fip.html
[http2] Applied Scientific Instrumentation, Inc,
http://homepage.mac.com/myers/imaging/
[http3] Reindeer Graphics, The Image Processing and Measurement
Cookbook, http://www.reindeergraphics.com/tutorial/
[http4] Serge Beucher, Image Segmentation and mathematical
morphology, http://cmm.ensmp.fr/~beucher/wtshed.html
[http5] Matlab news and notes,
http://www.mathworks.com/company/newsletter/win02/
watershed.shtml
[http6] Holmes Effect, University of Dellware
http://www.udel.edu/Biology/Wags/b667/lect6/lect6_11.gif