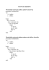Matematyczny model wzrostu fazy międzymetalicznej powstającej w
Transkrypt
Matematyczny model wzrostu fazy międzymetalicznej powstającej w
Matematyczny model wzrostu fazy międzymetalicznej powstającej w wyniku dyfuzji dwu składników M. Danielewski, S. Środa, H. Woźnica 1 Akademia Górniczo-Hutnicza Katedra Fizykochemii Ciała Stałego, Mickiewicza 30, 30-059 Kraków 2 Politechnika Krakowska Instytut Chemii i Technologii Nieorganicznej Warszawska 24, 31-155 Kraków 3 Wydział Inżynierii Materiałowej i Metalurgii, Politechnika Śląska, 40-019 Katowice słowa kluczowe: transport, kinetyka, dyfuzja, związki międzymetaliczne Streszczenie: W pracy zaprezentowano matematyczny model wzrostu związku, np., fazy międzymetalicznej. W prezentowanym mdelu warstwa produktu reakcji wzrasta w wyniku dyfuzji obu składników. W analizowanym przypadku niezależnych strumieni dyfuzyjnych dwa równania dyfuzji są wystarczające do ilościowego opisu procesu transportu dyfuzyjnego w takim układzie. Zostały one użyte do analizy wzrostu fazy międzymetalicznej powstającej w wyniku procesów dyfuzyjnych. W przeciwieństwie do modeli quasi-stacjonarnych, model ten umożliwia ilościowy opis dyfuzji reakcyjnej w związkach wykazujących duże odstępstwo od stechiometrii (takich jak związki międzymetaliczne) oraz w układach nierównowagowych. Abstract: In this paper a new model of single intermetallic phase growth was presented. In presented model the intermetallic phase grows due to diffusion of both elements. In case of solely diffusional fluxes the two diffusion equations are sufficient for the quantitative description of a diffusional transport process and are applied for the analysis of the diffusion-controlled growth of the product layer. Contrary to quasistationary simplifications, the presented model allows for the quantitative description of reactive diffusion in the compounds showing wide homogenity range (such as intermetallic compounds) and for the systems far from equilibrium. 1. Wstęp Istnieje wiele ważnych procesów technologicznych w których kontrolowany dyfuzją wzrost związków międzymetalicznych odgrywa znacząca rolę. Dobrze znane przykłady to wysokotemperaturowa korozja stopów i wytwarzanie międzymetalicznych pokryć ochronnych przez wygrzewanie dyfuzyjne [1], cynkowanie[2], łączenie i spajanie rożnych materiałów [3]. W powyższych procesach dyfuzja jednego lub kilku składników często warunkuje powstawanie nowej fazy (międzymetalicznej) i proces taki określany jest w literaturze jako dyfuzja reakcyjna [4-7]. Niekiedy procesy dyfuzji reakcyjnej określane są jako dyfuzja wzajemna. 2. Teoria Zakładamy, że wzrost fazy międzymetalicznej “j” spowodowany jest dyfuzją dwóch składników A i B przez utworzoną warstwę (Rys. 1). Na granicach faz Xj-1 i Xj panuje stan bliski równowagi termodynamicznej, tak więc stężenia na odpowiednich granicach faz nie są funkcja czasu (Rys. 1a): cAj(t, Xj-1) = const., cAj(t, Xj)= const., i cBj(t, Xj-1)= const., cAj(t, Xj) =const., (1) Lokalne stężenia obu składników w rosnącej warstwie fazy międzymetalicznej są zarówno funkcja położenia jak i czasu: cAj=cAj(t, x) and cBj =cBj(t, x) i prezentowana teoria umożliwia ich wyliczenie. Chwilową grubość rosnącej warstwy międzymetalicznej opisuje równanie: X (t) = Xj(t) – Xj-1(t) (2) gdzie Xj(t) I Xj-1(t) są poruszającymi się granicami faz, a ich szybkości są powiązane równaniem (3): dX dX dX j-1 j = − dt dt dt (3) 1 Proces dyfuzji składników A i B spełnia prawo zachowania masy, które dla i-tego składnika może być wyrażone przy pomocy równania dyfuzji (II prawo Fick’a): ∂ 2c ij ij =D i 2 ∂t ∂x ∂c (4) gdzie: i =A, B oraz j = 1, 2.....r; cij oznacza stężenie składnika A i B w rosnącej j-tej fazie międzymetalicznej, np. cAj i cBj. Ponadto zakładamy większość założeń postulowanych przez Wagnera [10] i) najwolniejszym procesem determinującym szybkość powstawania fazy międzymetalicznej jest dyfuzja sieciowa ( Jij = -Dij grad cij), ii) stężenia dyfundujących składników na poszczególnych granicach faz Xj-1 i Xj są stałe, tzn., nie są funkcją czasu, (Równanie 1), (jest to równoważne założeniu lokalnej równowagi termodynamicznej) iii) rosnący związek może mieć dowolnie szeroki zakres homogeniczności W modelu pomijamy: - dryft, dyfuzje wzajemną i reakcje chemiczne w strefie dyfuzji (Równanie 4), efekt pola elektrycznego (np. dyfuzję ambipolarną, Di=const) oraz inne efekty, które również mogą wpływać na warunki początkowe i brzegowe (np. reakcje powierzchniowe). - zależność współczynników dyfuzji poszczególnych składników od składu, Dij = const. Model ten jest całkowicie zdefiniowany przez następujące stałe (DANE): a) współczynniki dyfuzji DAj, i DBj; b) stałe stężenia na poszczególnych granicach faz c Aj (X j-1 (t)), c Aj (X j (t)), c Bj (X j-1 (t)) and c Bj (X j (t)) . Ponadto, zakładamy ze pierwszy składnik (A) dyfunduje z lewej strony na prawą, podczas gdy składnik drugi (B) w przeciwnym kierunku (Rys.1): c Aj (X j-1 (t)) > c Aj (X j (t)) , c Bj (X j-1 (t)) < c Bj (X j (t)) Matematycznie przedstawiony model opisany jest przez drugie prawo Ficka, rów.(4) z warunkiem początkowym: lim X (t) = lim X (t) = 0 j j-1 + + oraz warunkami brzegowymi: a) b) t→0 t→0 stałe stężenia na brzegach: c Aj (X j-1 (t)), c Aj (X j (t)), c Bj (X j-1 (t)) i c Bj (X j (t)) D ⎧ dX ∂c Bj Bj ⎪ j-1 = − (t, X j-1 (t)) c (t , X ) ∂x ⎪ dt B j −1 ⎪ ⎨ D ⎪ dX j (t) ∂c Aj Aj = − (t, X j (t)) ⎪ c (t , X ) ∂x ⎪⎩ dt A j Niewiadome (funkcje), których obliczenie umożliwia prezentowany model: Xj-1 (t), Xj (t), cAj (t,x), cBj (t,x) 2 Rys.1 Schemat wzrostu fazy międzymetalicznej „j” powstającej w wyniku dyfuzji dwu składników poprzez tworząca się fazę i ich reakcji na odpowiednich granicach faz Należy zaznaczyć, że zostało wykazane [11], iż istnieje jedyne rozwiązanie powyższego problemu, które można przedstawić w postaci: Xj-1(t) = -Λj-1 t Xj(t) = Λj t (6) gdzie (Λj-1, Λj) jest jedynym rozwiązaniem układu równań: ⎧ D Bj ⎛ Λ 2j-1 ⎞ c Bj ( x j , t ),−c Bj ( x j −1 , t ) ⎟* exp⎜ − ⎪Λ j-1 = ⎜ 4D Bj ⎟ F(Λ / 2D ) + F(Λ / 2D ) − 1 c Bj ( x j −1 , t ) π ⎪⎪ j-1 Bj j Bj ⎠ ⎝ ⎨ 2 D Aj ⎛ Λj ⎞ c Aj ( x j −1 , t ) − c Aj ( x j , t ) ⎪ ⎟* exp⎜ − ⎪Λ j = ⎜ 4D Aj ⎟ F(Λ / 2D ) + F(Λ / 2D ) − 1 c Aj ( x j , t ) π ⎪⎩ j-1 Aj j Aj ⎠ ⎝ (7) gdzie: F oznacza funkcję rozkładu normalnego: 3 F(z) = 1 2π z 1 ∫ exp( − 2 r 2 )dr (8) −∞ ponadto c ij (t, x) = B ji + A ij F(x/ 2D ij t ) c ij ( X , t ) − c ij ( X , t) j j −1 A = , B = c ij ( X , t ) − A F(Λ j / 2D ) ij F(Λ / 2D ) + F(Λ / 2D ) − 1 ij ij i j j-1 j ij ij (9) (10) gdzie i = (A, B). Biorąc pod uwagę równania (2) i (6), grubość powstającej fazy międzymetalicznej można opisać równaniem parabolicznym: X2(t) = 2kpt = = (Λj+Λj-1)2 t. (11) Tak, więc paraboliczna stała szybkości może być przedstawiona jako: kp = ½(Λj+Λj-1)2 (12) Z czysto matematycznego punktu widzenia dla dowolnych dodatnich wartości DAj, DBj and cij istnieje jedyne rozwiązanie (λj, λj-1, cAj, cBj) powyższego problemu zwanego problemem Stefana problem [8]. Podsumowanie W przeciwieństwie do modeli quasi-stacjonarnych, prezentowany model pozwala wyliczyć w sposób ilościowy rozkład poszczególnych składników oraz szybkość wzrostu faz z dużym odstępstwem od stechiometrii (np. wustyt, związki międzymetaliczne) oraz może być wykorzystywany w układach nie pozostających w stanie równowagi. Wyniki obliczeń dla układu Zn-Fe są prezentowane w innej pracy [13]. Podziękowania Praca finansowana była częściowo przez KBN projekt nr. 7 T08C 023 20. Literatura 1. Kofstad, P., High Temperature Corrosion (London, Elsevier, 1998). 2. Hot dip galvanizing of cast iron, Foundry Trade Journal, March 10, 1988, p. 191-194. 3. Nicholas, M.G., Joining Processes (London, Kluwer Academic Publisher, 1998). 4. Philbert, J., Atom Movements, Diffusion and Mass Transport in Solids. Les Ulis, France: Les Editions de Phisique, 1991. 5. 1998. Dybkov V. I., Growth Kinetics of Compound Layers, Cambridge International Science Publishing, 6. Van Loo F. J. J., Progress Solid State Chemistry, 20 (1990) 47. 7. Lengauer W. J Alloys and Compounds, 80 (1995) 229. 8. Wagner, C., Prog. Solid State Chemistry, 3 (1997) 10. 9. p.120. 10. Fromhold, A. T., Theory of Metal Oxidation, Vol. I Fundamentals (North-Holland, Amsterdam 1980), Wagner, C., Atom Movements (ASM Cleveland, USA 1951) p. 153. 11. Binkofski, R., "The mathematical description of the corrosion process", Jagiellonian Univ. Inst. of Math. thesis (1995). 12. Holly, K., E. Bobula, M. Danielewski i K. Szyszkiewicz, Sci. Bull., University of Mining and Metallurgy, Metall. And Foundry Eng. 20, 79 (1994). 13. H. Woźnica i M. Michalik, ten tom. 4 5