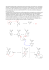wersja pdf - LHC Wielki Zderzacz Hadronów
Transkrypt
wersja pdf - LHC Wielki Zderzacz Hadronów
Co jest elementarne? cz. I Cząstki elementarne - składniki materii nie posiadające wewnętrznej struktury. John Dalton (1766 - 1844) - twórca nowożytnej teorii atomistycznej Od wieków ludzkość zastanawiała się nad otaczającym ją światem, starając się go opisać i zrozumieć procesy w nim zachodzące. Wraz z postępem badań okazało się, że materia składa się z ogromnej liczby malutkich cząstek, które zachowują się zupełnie inaczej niż świat skal do jakich przywykliśmy. Prześledźmy drogę, na której człowiek analizował budulec rzeczywistości. Ernest Rutherford (1871 - 1937) - odkrywca jądra atomowego (1911) i protonu (1919) w pierwszej zaobserwowanej i zinterpretowanej reakcji jądrowej. 3. Elektron 1. Cztery żywioły W połowie XIX wieku pojawiły się idee głoszące, że atom zawiera mniejsze cząstki o określonym ładunku oraz że istnieje najmniejszy ładunek elektryczny, którego wielokrotnościami są wszystkie obserwowane. W latach 70. tamtego wieku William Crookes skonstruował aparaturę, za pomocą której był w stanie obserwować przyspieszone elektrony wywołujące fluorescencję szkła, w które uderzały, choć on sam interpretował to nieco inaczej. Późniejsze eksperymenty z „promieniami katodowymi” pozwoliły Josephowi Johnowi Thompsonowi wykazać ich korpuskularną naturę oraz wyznaczyć ładunek elektronu i jego masę – tysiąckrotnie mniejszą od masy atomu wodoru. W V w. przed Chr. grecki filozof Empedokles sformułował pierwszy zachowany w myśli europejskiej pogląd, zgodnie z którym materia składa się z czterech podstawowych elementów (od czasów Arystotelesa zwanych żywiołami): ognia, ziemi, powietrza i wody – substancji, jakie otaczają ludzi na co dzień i wydawały się wyjaśniać charakter wszystkich zjawisk przyrody. Atomy niklu (Ni110) pod skaningowym mikroskopem tunelowym (STM). IBM Almaden Research Center 2. Atom Inni filozofowie tamtej epoki, m.in. Leucyp i Demokryt twierdzili, że wszystko składa się z podstawowych elementów, które nazwali atomami (gr. atomos – niepodzielny), zbyt małych by je ujrzeć i wyodrębnić z nich mniejsze części. W nowożytnej nauce silnym argumentem za ich istnieniem było wykorzystanie w 1803 r. przez Johna Daltona postulatu atomistycznej struktury materii do wyjaśnienia dlaczego w reakcjach chemicznych dane substancje uczestniczą zawsze w określonych proporcjach. Odkrycie swobodnego elektronu i promieniotwórczości obaliły pogląd o niepodzielności atomów, zaś w 1911 r. Ernest Rutherford wykazał że dodatni ładunek atomu jest skupiony w jądrze o rozmiarach bardzo małych (10-14m) w -10 porównaniu do rozmiarów atomu (10 m). WIELKI ZDERZACZ HADRONÓW Tuba Crookesa. Elektrony z rozrzedzonego gazu wewnątrz tuby są przyspieszane w kierunku poziomym, a padając na szkło po prawej stronie, tworzą cień krzyża maltańskiego. Autor: Mateusz Iskrzyński