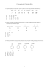pytania i odpowiedzi
Transkrypt
pytania i odpowiedzi
Imię i nazwisko ........................................................................................................... TEST MAGISTERSKI 9.04.05 1. Charakterystyczny osad błękitu pruskiego tworzy się po dodaniu do roztworu zawierającego jony Fe3+ roztworu: a) amoniaku b) heksacyjanożelazianu(II) potasu c) heksacyjanożelazianu(III) potasu d) tiocyjanianu potasu 2. Z 0,1-molowego roztworu zawierającego siarczan(VI) cynku(II) wytrąci się biały osad po dodaniu 0,1-molowego roztworu: a) b) c) d) kwasu chlorowodorowego HCl azotanu(V) kadmu(II) chlorku glinu(III) azotanu (V) ołowiu(II) 3. pH roztworu azotanu(V) bizmutu(III): a) b) c) d) jest niższe od 7 jest wyższe od 7 nie da się zmierzyć z powodu bardzo małej rozpuszczalności tej soli w wodzie takie samo jak pH czystej wody 4. Do 1 dm3 roztworu zawierającego 100 milimoli kwasu octowego dodano 0.05 mola stałego octanu sodu. Ile wynosi pH otrzymanego roztworu, jeśli pKa kwasu octowego wynosi 4,8 ? a) b) c) d) 4,8 5,1 4,5 9,2 5. Do pomiarów pH nie nadaje się: a) szklana elektroda kombinowana, b) nasycona elektroda kalomelowa, c) elektroda antymonowa, d) elektroda chinhydronowa. 6. Wskaż wzór cząsteczki, która wykazuje paramagnetyzm: a) CO2 b) SO2 c) NO2 d) XeO2 7. Wskaż wzór cząsteczki, która nie wykazuje trwałego momentu dipolowego a) SO2 b) NO2 c) ClO2 d) CO2 8. Wiązanie wodorowe nie powstaje między cząsteczkami a) CH4 b) NH3 c) H2O d) HF 9. Która z wymienionych niżej soli wapnia(II) jest najlepiej rozpuszczalna w wodzie: a) CaC2O4 b) CaCO3 c) CaCl2 d) Ca3(PO4)2 10. Która z poniżej przedstawionych liczb ma cztery cyfry znaczące ? a) 0,0010 b) 123×101 c) 0,0135 d) 1,358 11. Podczas miareczkowania kwasu octowego zasadą sodową jako wskaźnik punktu końcowego najlepiej jest zastosować: a) oranż metylowy b) skrobię c) fenoloftaleinę d) difenyloaminę 12. Roztwory pewnych substancji o stężeniach 0,1 mol/dm3 zostały uszeregowane według rosnącej wartości pH. Wskaż prawidłowy szereg wzorów tych substancji. a) b) c) d) NH4Cl, KCl, Na2CO3, CH3COONa; NH4Cl, CH3COONa, Na2CO3, KCl; CH3COONa, NH4Cl, KCl, Na2CO3; NH4Cl, KCl, CH3COONa, Na2CO3. 2 13. Wybierz zbiór jonów metali, których wodorotlenki wytrącą się w nadmiarze NH3(aq): a) Cr3+, Mg2+, Cu2+, Ba2+; b) Fe3+, Al3+, Zn2+, Mg2+; c) Fe3+, Al3+, Bi3+, Mg2+; d) Zn2+, Cr3+, Mg2+, Fe3+. 14. SiO2 rozpuszcza się w roztworze: a) HCl b) HNO3 c) HF d) NH3 15. Rząd wiązania w jonie cząsteczkowym O22- wynosi: a) 1 b) 1,5 c) 2 d) 2,5 16. W wyniku działania nadmanganianem potasu na trans-1,2-dimetyloeten powstają związki: CH3 H H CH3 HO OH H CH3 H H CH3 OH CH3 OH CH3 H CH3 H 2 1 a) 1,2 b) 1,4 H HO CH3 CH3 CH3 OH OH OH 4 3 c) 2,3 H H d) 3,4 17. Wskaż uprzywilejowany produkt poniższej reakcji przyłączania jodowodoru: + (CH3)3N-CH=CH2 a) 1 b) 2 c) 3 + (CH3)3N-CH2CH2I + (CH3)3N-CHI-CH3 + (CH3)3N-CH=CHI + (CH3)3N-CHI-CH2I HI d) 4 3 18. 2-jodoheksan potraktowano metanolanem sodu w metanolu otrzymując nienasycony alken. Jaki będzie skład mieszaniny poreakcyjnej? a) b) c) d) w przewadze wystąpi 2-heksen w przewadze wystąpi 1-heksen 1-heksen i 2-heksen w stosunku 1:1 mieszanina 2- i 3-heksenu 19. Który z wymienionych niżej odczynników nie nadaje się do przeprowadzenia poniższej reakcji ? H Br a) P Br3 b) CH3CH2CH2OH CH3CH2CH2Br N aBr/H2SO 4 c) AgBr d) 20. Wskaż, które z wymienionych eterów będą ulegały rozszczepieniu pod wpływem HBr według mechanizmu SN2: 1 eter dietylowy 2 eter ditert-butylowy 3 eter diallilowy 4 eter diizobutylowy 5 eter dibenzylowy 6 eter etylowo- metylowy a) 1,4,6 b) 2,3,4 c) 1,5,6 d) 3,4,5 21. Wskaż, w której z poniższych przemian podano błędnie produkt: a) b) O2N N2+ c) d) CuBr O2N Br O2N CN O2N NO2 O2N PO2 CuCN Cu(NO2)2 H3PO2 4 22. Przeprowadzono następujacy ciąg syntez: CH3OH HBr Mg A B 1) CO2 2) H 2O C SOCl2 D NH3 E NaOBr F Związek F to: a) metyloamina b) etyloamina c) dimetyloamina d) winyloamina 23. Które z wymienionych niżej związków mają charakter aromatyczny: 1 2 a) 2,3,4 b) 1,2,5 N O 3 4 c) 1,4,6 6 5 d) 2,5,6 24. Wskaż prawidłowy schemat syntezy: a) b) c) d) CH3CH=CH 2/H 2SO4 CH2CH2CH3 CH 3CH2CH 2Cl/AlCl3 1. CH3CH 2COCl/AlCl3 2. Zn(Hg)/HCl 1. CH 3CH=CHBr/H2SO 4 2. H2/Pd/C 25. Wskaż podstawniki kierujące w położenie orto i para podczas substytucji elektrofilowej w pierścieniu benzenowym: 1. -OH a) 1,2,6 2. –CH2CH3 b) 3,4,5 3. -NO2 4. -COOH c) 3,7,8 5. -SO3H d) 4,5,8 5 6. -Cl 7. -CN 8. –CHO 26. W wyniku działania 2 moli bromu na 1 mol fenyloetyloketonu, w temperaturze pokojowej, jako główny produkt powstanie: b) a) O C CH2CH3 O C d) c) C(Br)2CH3 O C CH2CHBr2 O Br 27. Następujące pochodne kwasowe: 1. RCOCl 2. (RCO)2O 3. RCOOR’ 4. RCOOH 5. RCONH2 ustawione według malejącej zdolności acylowania, tworzą szereg: a) b) c) d) 1>2>3>4>5 3>2>5>1>4 5>4>3>2>1 1>4>2>5>3 28. Kwas walerianowy posłużył jako substrat do następującej sekwencji reakcji: CH3CH2CH2CH2COOH SOCl2 A NH 3 B NaOBr C 1 mol CH 3I K2CO 3 D Związek D to: a) b) c) d) butylometyloamina amid kwasu α-bromowalerianowego ester metylowy kwasu walerianowego dibutylometyloamina 29. Pojęcie kodonu oznacza: a) pełną sekwencję zasad nukleinowych w DNA b) nukleotyd kodujący określony aminokwas w strukturze białka c) trójkę nukleotydów kodujących określony aminokwas w strukturze białka d) typ wiązania między aminokwasem i cząsteczką tRNA 6 C CHBrCH2Br 30. W strukturze podwójnej helisy kwasu deoksyrybonukleinowego (DNA) wiązania wodorowe powstają między parami zasad nukleinowych: a) adenina z tyminą i guanina z cytozyną b) adenina z cytozyną i guanina z tyminą c) między identycznymi zasadami obu nici DNA d) adenina z guaniną i tymina z cytozyną 31. Który z podanych rzędów wielkości odpowiada typowej długości wiązania chemicznego ? a) 10-6 m b) 10-12 m c) 10-20 m d) 10-10 m 32. Które z podanych rodzajów promieniowania elektromagnetycznego ma największą energię ? a) widzialne światło czerwone b) widzialne światło fioletowe c) mikrofale d) fale radiowe 33. Konfigurację elektronową 1s22s22p63s1 ma atom: a) potasu b) magnezu c) chloru d) sodu 34. Widmo EPR można uzyskać dla próbki składającej się z molekuł: a) CO2 b) N2 c) NO d) CO 35. Reakcja opisana równaniem: CaO + H2O → Ca(OH)2 przebiega z wydzieleniem energii na sposób ciepła. Obniżenie temperatury układu spowoduje, że: a) szybkość reakcji zmniejszy się, a stan równowagi przesunie się w kierunku produktów b) szybkość reakcji zmniejszy się bez wpływu na stan równowagi c) szybkość reakcji wzrośnie bez wpływu na stan równowagi d) szybkość reakcji zmniejszy się, a stan równowagi przesunie się w kierunku substratów 7 36. Układ, w którym przebiega spontanicznie reakcja chemiczna w warunkach izotermicznoizobarycznych, zmierza zawsze do: a) maksimum entropii układu b) minimum energii wewnętrznej układu c) minimum łącznej entropii układu i otoczenia d) minimum entalpii swobodnej układu 37. Para redoks Ox/Red charakteryzuje się potencjałem standardowym E0, a para redoks związków kompleksowych Ox(L)N/Red(L)N – potencjałem standardowym E10 (L – ligand, N – liczba koordynacyjna). Jeśli stała trwałości kompleksu Ox(L)N jest większa od stałej trwałości kompleksu Red(L)N, to między wartościami E0 i E10 spełniona jest relacja: a) E10 = E0 b) E10 > E0 c) E10 < E0 d) E10 = (E0)N 38. Wodorek sodu NaH rozpuszczono w wodzie, a powstały roztwór poddano elektrolizie z użyciem elektrod platynowych. W wyniku elektrolizy otrzymano następujące produkty: a) na katodzie i anodzie – wodór b) na katodzie – wodór, na anodzie - tlen c) na katodzie – sód, na anodzie – wodór d) na katodzie – sód , na anodzie - tlen 39. Między sumą mas swobodnych nukleonów a masą utworzonego z nich jądra atomowego zachodzi zależność: a) masy te są równe, na mocy prawa zachowania masy b) masa jądra jest nieco większa od sumy masy nukleonów c) masa jądra jest nieco mniejsza od sumy masy nukleonów d) masa jądra jest mniejsza lub większa od sumy mas nukleonów, w zależności od energii ich wiązania w jądrze 40. Jeśli stała rozpadu α promieniotwórczego izotopu 218Po wynosi 3,78×10-3 s-1, to okres półtrwania tego izotopu wynosi: a) kilka sekund b) kilka minut c) kilka miesięcy d) kilka lat 41. W strukturze krystalicznej grafitu występują wiązania: a) kowalencyjne i van der Waalsa b) kowalencyjne i metaliczne a) wyłącznie kowalencyjne b) wyłącznie van der Waalsa 8 42. Środek symetrii umieszczony w początku (0,0,0) kartezjańskiego układu współrzędnych przekształca punkt o współrzędnych (x,y,z) na punkt o współrzędnych: a) (x,y,z) b) (-x,-y-,-z) c) (2x,2y,2z); d) (0,0,0) 43. Ze wzrostem masy odległości poziomów energetycznych oscylatora harmonicznego: a) zmniejszają się b) zwiększają się c) nie ulegają zmianie d) zmniejszają się dla cząsteczek liniowych, a zwiększają dla nieliniowych 44. Pojęcie iż proces może przebiegać „w obszarze dyfuzyjnym” (dla odróżnienia od przebiegu „w obszarze kinetycznym”) oznacza iż: a) podczas reakcji zachodzi dyfuzja reagentów b) transport dyfuzyjny jest wolniejszy od reakcji chemicznej c) zjawisko dyfuzji nie ma wpływu na szybkość reakcji d) transport dyfuzyjny jest szybszy od reakcji chemicznej 45. Wysokooktanową benzynę otrzymujemy w procesie: a) destylacji ropy naftowej b) pirolizy frakcji ropy naftowej c) krakingu frakcji ropy naftowej d) koksowania węgla kamiennego 9 10 ODPOWIEDZI 1. b 2. d 3. a 4. c 5. b 6. c 7. d 8. a 9. c 10.d 11. c 12. d 13. c 14. c 15. a 16. b 17. a 18. a 19. d 20. a 21. d 22. a 23. a 24. c 25. a 26. b 27. a 28. a 29. c 30. a 31. d 32. b 33. d 34. c 35. a 36. d 37. c 38. b 39. c 40. b 41. a 42. b 43. a 44. b 45. c 11