Wpływ palenia papierosów na stężenie albumin i aktywność β
Transkrypt
Wpływ palenia papierosów na stężenie albumin i aktywność β
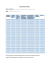
PRACE ORYGINALNE Anna Bizoń1 Katarzyna Witt1 Małgorzata Milnerowicz2 Halina Milnerowicz1 Wpływ palenia papierosów na stężenie albumin i aktywność β-glukuronidazy w moczu hutników Effect of tobacco smoking on albumin concentration and β-glucuronidase activity in urine of smelters Katedra i Zakład Biomedycznych Analiz Środowiskowych, Wydział Farmaceutyczny z Oddziałem Analityki Medycznej, Uniwersytetu Medycznego we Wrocławiu, Kierownik: Prof. dr hab. Halina Milnerowicz 1 Wydział Lekarski, Uniwersytet Medyczny we Wrocławiu 2 Dodatkowe słowa kluczowe: palenie papierosów narażenie zawodowe metale ciężkie albuminy β-glukuronidazy mikroalbuminuria Additional key words: tobacco smoking occupational exposure heavy metals albumin β-glucuronidase microalbuminuria Adres do korespondencji: Dr Anna Bizoń Katedra i Zakład Biomedycznych Analiz Środowiskowych, Wydział Farmaceutyczny z Oddziałem Analityki Medycznej Uniwersytet Medyczny we Wrocławiu Ul. Borowska 211 50-556 Wroclaw Tel.: (71) 784 0175 Fax: (71) 784 0172 e-mail: [email protected] Przegląd Lekarski 2014 / 71 / 11 Celem prezentowanej pracy była ocena nefrotoksycznego działania metali ciężkich na podstawie oznaczania stężenia albumin i aktywności β-glukuronidazy w moczu u palących i niepalących pracowników Huty Miedzi. Materiałem do badań był mocz pobrany od 101 palących i niepalących hutników oraz od 65 palących i niepalących osób nienarażonych zawodowo na metale ciężkie. Podział na grupy palące i niepalące dokonano na podstawie danych uzyskanych z bezpośredniego, indywidualnego wywiadu oraz otrzymanego wyniku oznaczania stężenia kotyniny w surowicy. Stężenie albumin w moczu zmierzono przy użyciu komercyjnego, enzymatycznego testu (Micro-Albumin ELISA Nr kat. 5MA 742 12, ORGENTEC Diagnostika Gmbh, Niemcy). Aktywność β-glukuronidazy w moczu oznaczono z wykorzystaniem p-nitrofenylo-β-Dglukuronidu jako substratu. Zaobserwowano występowanie mikroalbuminurii u palących i niepalących hutników oraz stwierdzono podwyższoną aktywność β-glukuronidazy w moczu palących i niepalących hutników w stosunku do niepalących osób z grupy kontrolnej. Wykazano wpływ palenia papierosów na stężenie albumin w moczu, zarówno u hutników, jak i w grupie kontrolnej oraz zaobserwowano wpływ ilości wypalanych papierosów na stężenie tych białek w moczu hutników. Istotne statystycznie różnice w aktywności β-glukuronidazy w moczu stwierdzono pomiędzy palącymi i niepalącymi hutnikami, co sugeruje dodatkowy negatywny wpływ palenia papierosów na aktywność tego enzymu. Występowanie mikroalbuminurii oraz wzrost aktywności β-glukuronidazy w moczu osób narażonych zawodowo na metale ciężkie oraz palących papierosy wskazuje, że ekspozycja środowiskowa na te czynniki skutkuje zaburzeniem w funkcjonowaniu nerek. The aim of present study was to estimate the nephrotoxicity of occupational exposure to heavy metals on albumin concentration and β-glucuronidase activity in the urine of smoking and non-smoking smelters. The study was performed in urine of 101 smoking and non-smoking smelters as well as 65 smoking and nonsmoking male subjects unexposed to heavy metals. Section into smoking and nonsmoking groups was made on basis on direct personal interview and by determination of serum cotinine concentration. The concentration of albumin in urine was measured with commercial test (Micro-Albumin ELISA Cat. No 5MA 742 12, ORGENTEC Diagnostika Gmbh, Germany). The activity of β-glucuronidase in urine were determined in urine using 4-nitrophenyl β D-glucuronide (Cat. No 73677, Sigma Aldrich, Germany) as a substrate. We have observed higher albumin concentration and β-glucuronidase activity in urine of smoking and nonsmoking smelters when compared to control groups. We have also found the influence of tobacco smoke as well as amount of cigarettes smoked on albumin concentration in urine of smoking smelters. A statistically significant difference was detected between activity of β-glucuronidase in urine of smoking and non-smoking smelters, which suggest as additional negative factor of exposure to tobacco smoke. Analyzing the impact of smoking intensity we have found higher albumin concentration and β-glucuronidase activity in urine of smelters smoking ≥20 cigarettes per day when compared to smelters smoking <20 cigarettes per day. The elevation of albumin concentration and β-glucuronidase activity in urine of workers occupational exposure to heavy metals and tobacco smoke indicated, that environmental exposure on these factors can disorders kidney functions. 581 Wstęp Palenie papierosów działa szkodliwie na cały organizm, w tym na wszystkie narządy. Wykazano negatywny wpływ palenia tytoniu na nerki, głównie ze względu na zawarty w dymie tytoniowym kadm (Cd) i ołów (Pb) [1]. Palenie papierosów może powodować progresję chronicznej choroby nerek oraz zwiększa ryzyko rozwoju mikroalbuminurii a w konsekwencji proteinurii [2]. Ryzyko rozwoju nefropatii zwiększa się wraz ze wzrostem ilości wypalanych papierosów [3]. Mechanizm nefrotoksycznego działania składników dymu tytoniowego nie jest do końca poznany. Zaburzenie pracy nerek może wynikać z negatywnego wpływu składników dymu tytoniowego na naczynia krwionośne w nerkach, wynikające z uszkadzania komórek śródbłonka i indukcji proliferacji komórek mięśni gładkich [4]. Funkcja nerek, w podstawowych badaniach diagnostycznych, określana jest na podstawie pomiaru objętości moczu, jego pH, ciężaru właściwego, przesączania kłębuszkowego (GFR), sekrecji białek z moczem i zaburzeń elektrolitowych [5]. Wadą tych parametrów jest fakt, że zmiany wartości obserwuje się dopiero w momencie znacznego upośledzenia funkcji nerek. W przypadku środowiskowej lub zawodowej ekspozycji na potencjalnie nefrotoksyczne czynniki, istotne jest znalezienie w moczu specyficznych wskaźników uszkodzeń. Takimi markerami może być oznaczanie stężeń albumin i aktywności β-glukuronidazy w moczu [6, 7]. Ludzka, osoczowa albumina jest globularnym, nieglikozylowanym białkiem o masie cząsteczkowej 66 kDa nieulegającym przesączaniu przez błonę kłębuszków nerkowych. W stanie fizjologicznym występuje w moczu w śladowych ilościach (do 20 mg/g kreatyniny) [8]. Przefiltrowane cząsteczki albuminy są następnie reabsorbowane na drodze endocytozy w kanalikach proksymalnych, gdzie ulegają degradacji przez enzymy lizosomowe [8]. W wielu stanach chorobowych nerek dochodzi do zwiększenia przepuszczalności membran filtracyjnych kłębuszków, czego skutkiem jest proteinuria. Białkami najczęściej oznaczanymi są albuminy. Oznaczanie albumin znalazło zastosowanie w diagnostyce wielu schorzeń. Wydalanie albumin z moczem w stężeniu w zakresie 20-200 mg/g kreatyniny nazywane jest mikro-albuminurią [6,9]. Podwyższone stężenie albumin w moczu może być istotnym czynnikiem predykcyjnym w pojawieniu się i progresji nefropatii czy retinopatii [10, 11] oraz wskazywać na zwiększone ryzyko rozwoju chorób wieńcowo-naczyniowych i w konsekwencji śmierci [12]. Oznaczanie stężeń albumin w moczu jest także istotne w warunkach ekspozycji na substancje o działaniu nefrotoksycznym [13,14]. Istotną funkcję w degradacji białek pełnią enzymy lizosomalne, do których należy β-glukuronidaza zlokalizowana w lizosomach oraz mikrosomach większości komórek [15]. Wzrost aktywności tego enzymu w moczu stwierdzono w wyniku uszkodzenia elementów układu wydalniczego – odmiedniczkowego zapalenie nerek, ostrej nekrozy nerkowej, nowotworów nerek i pęcherza 582 oraz nefropatii cukrzycowej [16,17]. Celem prezentowanej pracy była ocena nefrotoksycznego działania metali ciężkich takich jak arsen (As), Pb i Cd w wyniku ekspozycji zawodowej pracowników Huty Miedzi Zagłębia Legnicko-Głogowskiego oraz narażenia na dym tytoniowy na podstawie oznaczania stężenia albumin i aktywności β-glukuronidazy w moczu. Materiały Badania przeprowadzono w moczu pracowników Huty Miedzi Zagłębia Legnicko-Głogowskiego oraz u osób nie narażonych zawodowo na metale ciężkie, zakwalifikowanych do grupy kontrolnej. Na wykonanie badań uzyskano zgodę Komisji Bioetycznej Uniwersytetu Medycznego im. Piastów Śląskich we Wrocławiu (Nr KB: 469/2008). Badania wykonano u 101 hutników, w tym 51 niepalących (44,02±8,86 lat) i 50 palących hutników (39,52±9,71 lat) oraz 65 osób z grupy kontrolnej, w tym 25 niepalących (36,64±11,49 lat) i 40 palących osób (32,56±8,19 lat). Podziału na grupy palące i niepalące dokonano na podstawie danych uzyskanych z bezpośredniego, indywidualnego wywiadu oraz otrzymanego wyniku oznaczania stężenia kotyniny w surowicy przy użyciu komercyjnego testu (Cotinine ELISA, Nr kat. EIA-3242, DRG International, Inc. USA). Metody Stężenie Pb w pełnej krwi oraz Cd i As w moczu oznaczano metodą bezpłomieniową w kuwecie grafitowej Massmana na spektrofotometrze absorpcji atomowej SOLAAR M6 firmy Thermo Elemental [18, 19]. Stężenie albumin w moczu oznaczono przy użyciu komercyjnego enzymatycznego testu (Micro-albumin ELISA, Nr kat. 5MA 742 12, ORGENTEC Diagnostika Gmbh, Niemcy). Aktywność β-glukuronidazy w moczu oznaczono za pomocą spektrofotometrycznej metody wg Cobben i wsp. [20] z wykorzystaniem substratu p-nitrofenylo-β-Dglukuronidu. Ilość uwalnianego p-nitrofenolu oznaczano spektrofotometrycznie przy długości fali λ=405 nm. Zmierzona absorbancja była wprost proporcjonalna do aktywności enzymu. Oznaczenie przeprowadzono na 96-dołkowych mikropłytkach. Analiza statystyczna Dane wyrażono jako wartości średnie (X) z odchyleniem standardowym (SD). Normalność analizowano testem Shapiro- Wilka, a jednorodność wariancji testem Levean’a. Różnice między grupami analizowano testem t-Studenta. W przypadku braku rozkładu normalnego oraz jednorodności wariancji stosowano nieparametryczny test U-Manna Whitneya. Korelację pomiędzy analizowanymi parametrami zmierzono przy użyciu testu istotności współczynnika korelacji Spearmana. W procedurach weryfikacyjnych istotności statystycznej przyjęto poziom ufności p<0,05. Do obliczeń wykorzystano program Satistica wersję 9.0 PL. Wyniki Stężenie Pb w pełnej krwi oraz As i Cd w moczu Stężenia Pb w pełnej krwi, As i Cd w moczu oraz stężenie kotyniny w surowicy, wraz z uwzględnieniem podziału na ilości wypalanych papierosów dziennie, zostały opublikowane wcześniej [18,19]. Najwyższe stężenia Pb wykazano we krwi palących hutników. Stężenie Cd i As było najwyższe w moczu palących hutników. Stężenie albumin i aktywność β-glukuronidazy w moczu Zaobserwowano 4-krotny wzrost stężenia albumin w moczu palących hutników w stosunku do palących osób z grupy kontrolnej oraz około 5-krotny wzrost stężenia tych białek w moczu niepalących hutników w porównaniu do niepalących osób z grupy kontrolnej. Istotnie statystyczne różnice w stężenia albumin wykazano w moczu palących hutników względem niepalących osób z tej grupy. Podobną zależność zaobserwowano w grupie kontrolnej (Tab. I). Wykazano 2-krotny wzrost aktywności β-glukuronidazy w moczu palących hutników w porównaniu do palących osób z grupy kontrolnej. U niepalących hutników wzrost aktywności tego enzymu był o 1,5-razy wyższy względem niepalących osób z grupy kontrolnej (Tab. I). Wpływ intensywności palenia papierosów na stężenie albumin i aktywność β-glukuronidazy W moczu hutników palących ≥20 papierosów dziennie oraz u palących 20≥ papierosów dziennie osób z grupy kontrolnej wykazano 4-krotny wzrost stężenia albumin w porównaniu do palących <20 papierosów hutników (Tab. II). Taką samą zależność wykazano w przypadku aktywności β-glukuronidazy w moczu palących hutników oraz osób z grupy kontrolnej (Tab. II). U pracowników huty palących ≥20 papierosów dziennie stwierdzono około Tabela I Stężenie albumin i aktywność β-glukuronidazy w moczu hutników i w grupie kontrolnej. Albumin concentration and β-glucuronidase activity in urine of smelters and in control group. Grupy badane n=166 Kontrola Hutnicy niepalący n=25 palący n=40 niepalący n=51 palący n=50 Stężenie albumin [mg/g kreatyniny] 5,00±4,521),3) 7,13±6,452),3) 24,76±24,471),4) 28,26±19,652),4) Aktywność β-glukuronidazy [U/g kreatyniny] 2,92±0,791) 3,10±1,82 4,67±1,881),2),3) 6,26±5,892),3) 1), 2), 3), 4) różnice istotne statystycznie: p<0,05. A. Bizoń i wsp. Tabela II Wpływ palenia papierosów na stężenie albumin i aktywność β-glukuronidazy w moczu hutników i w grupie kontrolnej. The effect of tobacco smoke on albumin concentration and β-glucuronidase activity in urine of smelters and in control group. Grupy badane n=90 Kontrola paląca Hutnicy palący <20 papierosów/ dzień ≥20 papierosów/dzień <20 papierosów/dzień ≥20 papierosów/dzień Stężenie albumin [mg/g kreatyniny] X ± SD 6,77±2,481) 7,30±5,382) 27,56±21,101),3) 30,42±22,852),3) β-glukuronidaza [U/g kreatyniny] X ± SD 3,03±1,481) 3,42±2,182) 5,23±1,761),3) 7,09±4,742),3) 1), 2), 3), 4) różnice istotne statystycznie: p<0,05. 2-krotny wzrost aktywności β-glukuronidazy w stosunku do osób z grupy kontrolnej, palącej ≥20 papierosów dziennie. Wykazano wzrost aktywności β-glukuronidazy w moczu hutników palących ≥20 papierosów dziennie względem pracowników huty w mniejszym stopniu narażonych na dym tytoniowy. W moczu hutników palących <20 papierosów dziennie z grupy kontrolnej (Tab. II). Analiza korelacji Wykazano pozytywne korelacje pomiędzy stężeniem As, Pb i Cd a stężeniem albumin i aktywnością β-glukuronidazy w moczu. Najwyższą pozytywną korelację zaobserwowano pomiędzy stężeniem As w moczu i aktywnością β-glukuronidazy w moczu (r=0,50; p<0,05), następnie pomiędzy stężeniem Cd w moczu a aktywnością tego enzymu (r=0,48; p<0,05). Pozytywną korelację wykazano również pomiędzy stężeniem As w moczu i stężeniem albumin w moczu (r=0,41; p<0,05) oraz stężeniem Cd w moczu i stężeniem tych białek w moczu (r=0,42; p<0,05). Także stężenie Pb we krwi korelowało pozytywnie ze stężeniem albumin (r=0,34; p<0,05) w moczu oraz aktywnością β-glukuronidazy w moczu (r=0,18; p<0,05). Omówienie Zawodowe narażenie na metale ciężkie oraz palenie papierosów to istotne czynniki wpływające negatywnie na zdrowie człowieka. Wykazano wielonarządowe dysfunkcje w wyniku chronicznej ekspozycji na As, Pb i Cd oraz długotrwałego palenia tytoniu. Jednym z głównych narządów toksycznego oddziaływania metali ciężkich są nerki. Oznaczanie specyficznych markerów w moczu, łatwo dostępnym materiale biologicznym, może być kluczowym wskaźnikiem zaburzeń czynności nerek już w początkowym etapie uszkodzenia tego narządu. Oznaczanie stężeń albumin w moczu jest przydatne w ocenie funkcji kłębuszków nerkowych. Stosowane rutynowo metody diagnostyczne wykrywają obecność albumin w moczu dopiero w wysokich stężeniach (150 mg/g kreatyniny). Natomiast wykazano, że znacznie niższe stężenia (około 20 mg/ g kreatyniny) są niebezpieczne dla zdrowia i mogą być czynnikiem predykcyjnym rozwoju nefropatii, retinopatii czy zwiększonej śmiertelności w chorobach sercowo-naczyniowych. Oznaczone stężenia albumin w moczu Przegląd Lekarski 2014 / 71 / 11 hutników, zarówno palących jak i niepalących papierosy, miały wartości powyżej 20 mg/g kreatyniny, co wskazuje na występowanie mikroalbuminurii. U palących pracowników huty stwierdzono najwyższe stężenia albumin wynoszące 28,26±19,65 mg/g kreatyniny, nieznacznie niższe u niepalących hutników (24,76±24,47 mg/g kreatyniny). W moczu osób z grupy kontrolnej odnotowano odpowiednio 7,13±6,45 mg/g kreatyniny u palących i 5,00±4,52 mg/g kreatyniny u niepalących mężczyzn. Różnice średnich stężeń albumin w moczu palących i niepalących osób z badanych grup dowodzą także dodatkowego, toksycznego działania składników dymu tytoniowego na komórki nerek. Podział obu palących grup, ze względu na ilość papierosów wypalanych każdego dnia, także potwierdza istotne statystycznie różnice stężeń albumin w moczu. U hutników wypalających ≥20 papierosów dziennie zanotowano stężenia albumin w granicach 30,42±22,85 mg/g kreatyniny, a u hutników palących <20 papierosów/dziennie wykazano wartość średniego stężenia wynoszące 27,56±21,10 mg/g kreatyniny, co jednoznacznie wskazuje na występowanie mikroalbuminurii. W grupie kontrolnej nie zanotowano istotnych różnic pomiędzy osobami palącymi ≥20 papierosów dziennie a wypalającymi < 20 papierosów dziennie. Otrzymane wyniki świadczą o zależności pomiędzy ekspozycją zawodową na metale ciężkie a występowaniem mikroalbuminurii. Podobne wyniki uzyskali Nordberg i wsp., którzy analizowali wpływ ekspozycji na Cd i As na biomarkery czynności nerek [21]. Wykazali podwyższone stężenie albumin w moczu osób narażonych na Cd i As, natomiast nie stwierdzili wpływu płci na oznaczone stężenie tego białka [21]. Z kolei badania analizujące wpływ pojedynczej ekspozycji na Pb lub Cd nie wykazały mikroalbuminurii [22-24]. Jung i wsp. analizowali wpływ zawodowego narażenia na Pb na markery opisujące funkcję nerek. Wykazali negatywny wpływ ekspozycji na Pb na aktywność N-acetylo-D-glukozamin����������������������� idazy (NAG) i stężenie α-mikroglobuliny w moczu. Natomiast nie zaobserwowali zmian w stężeniu albumin w moczu. U osób, u których stężenie Pb w pełnej krwi wynosiło 74,6±7,8 µg/dl, stężenie albumin w moczu było w zakresie fizjologicznym (9,0±1,9 mg/g kreatyniny). Natomiast u pracowników, u których stężenie Pb wynosiło 46,5±5,9 µg/ dl stężenie albumin miało średnią wartość 8,8±1,9 mg/g kreatyniny. Wykazano, że pomimo znacznego narażenia na Pb i zaburzenia integralności komórek kanalików proksymalnych, kłębuszki nerkowe nie ulegają uszkodzeniu [23]. Wyniki opublikowane przez Bernard i wsp. wykazały również brak istotnego statystycznie wzrostu stężenia albumin w moczu osób narażonych nawet na wysokie stężenia Cd. W moczu osób najbardziej eksponowanych na Cd (≥ 10 µg/g kreatyniny) zaobserwowane średnie stężenie albumin wynosiło 7,6 mg/g kreatyniny, podczas gdy w moczu osób z oznaczonym stężeniem Cd w zakresie od 5 do 10 µg/g kreatyniny stężenie albumin wynosiło 6,3 mg/g kreatyniny [22]. Analogiczne wyniki uzyskali Noonan i wsp., którzy także nie wykazali zależności pomiędzy stężeniem Cd w moczu a stężeniem albumin w moczu oraz nie zaobserwowali liniowej zależności pomiędzy ilością wypalanych paczek papierosów w roku a stężeniem albumin w moczu [24]. W prezentowanej pracy dodatnia korelacja pomiędzy stężeniem Cd i albumin w moczu może wynikać z około 3-krotnie wyższego stężenia Cd w moczu palących hutników. W pracy Noonan i wsp. najwyższe stężenie Cd wynosiło 0,56 µg/g kreatyniny, natomiast najwyższe stężenie Cd w moczu palących ≥20 papierosów dziennie hutników było w zakresie 1,36±0,95 µg/g kreatyniny. Dodatkowo w prezentowanej pracy grupą badaną byli tylko mężczyźni, podczas gdy w badaniach prowadzonych przez Noona i wsp. były uwzględniane również kobiety [24]. Kolejnym markerem oznaczanym w momencie podejrzenia występowania uszkodzenia struktur układu moczowego jest także β-glukuronidaza [25]. Oznaczanie aktywności β-glukuronidazy w moczu jest ważnym markerem oceny stopnia uszkodzenia funkcji nerek, w wyniku ekspozycji na czynniki potencjalnie nefrotoksyczne oraz jest przydatne w diagnostyce wielu chorób, takich jak nowotwory nerek, odmiedniczkowe zapalenie nerek i retinopatia cukrzycowa [16, 17]. Wykazano podwyższoną aktywność β-glukuronidazy w moczu, zarówno palących, jak i niepalących hutników w porównaniu do osób nienarażonych zawodowo na metale ciężkie, co wskazuje, że zawodowa ekspozycja w hucie skutkuje zaburzeniem funkcji nerek. Podwyższona aktywność tego enzymu stwierdzona w grupie palących hutników i osób z grupy kontrolnej w stosunku, odpowiednio, do niepalących hutników i niepalących osób z grupy kontrolnej, potwierdza nefrotoksyczne działanie składników dymu tytoniowego. Zaobserwowano wpływ ilości wypalanych papierosów na wzrost aktywności β-glukuronidazy w moczu oraz wyższą aktywność β-glukuronidazy w moczu hutników palących ≥20 papierosów dziennie w stosunku do hutników palących <20 papierosów dziennie (p<0.05). Wzrost aktywności tego enzymu w moczu hutników oraz dodatkowy wzrost aktywności u hutników palących ≥20 papierosów dziennie wskazuje na nefrotoksyczne oddziaływanie środowiska i przydatność oznaczania aktywności tego enzymu w ocenie uszkodzeń struktury nerek w wyniku ekspozycji na metale ciężkie i dym tytoniowy. W prezentowanej pracy zaobserwowane 583 zmiany w przypadku stężeń albumin oraz aktywności β-glukuronidazy w moczu wynikają najprawdopodobniej z synergistycznego wpływu ekspozycji na As, Pb i Cd oraz ksenobiotyków dymu tytoniowego. Nasze wcześniejsze badania wykazały wzrost aktywności NAG i jej izoformy patologicznej NAG-B w moczu hutników, przy czym najwyższe aktywności NAG zaobserwowano w grupie palących hutników [26]. Podsumowując nasze badania, wykazany wzrost aktywności NAG i β-glukuronidaz oraz wzrost stężenia albumin w moczu osób narażonych zawodowo na metale ciężkie oraz palących papierosy jednoznacznie wskazuje, że ekspozycja środowiskowa na te czynniki skutkuje zaburzeniem w funkcjonowaniu kłębuszków nerkowych i kanalików proksymalnych nerek. Wnioski Występowanie mikroalbuminurii oraz wzrost aktywności β-glukuronidazy w moczu osób narażonych zawodowo na metale ciężkie oraz palących papierosy wskazuje, że ekspozycja środowiskowa na te czynniki skutkuje zaburzeniem w funkcjonowaniu nerek. Piśmiennictwo 1. Fowles J, Dybing B: Application of toxicological risk assessment principles to the chemical constituents of tobacco smoke. Tob Control 2003; 12: 424-430. 2. Paul W, Schapiro A, Gonick H: Studies of human kidney and urinary beta-glucuronidase. Enzymol. Biol Clin. 1967; 8: 47-66. 3. Orth SR: Smoking and the kidney. J Am Soc Nephrol. 2002; 13: 1663-1672. 4. Lhotta K, Rumpelt HJ, König P, Mayer G, Kronen- 584 berg F: Cigarette smoking and vascular pathology in renal biopsies. Kidney Int. 2002; 61: 648-654. 5. Cohen EP, Lemann J: The role of the laboratory in evaluation of kidney function. Clin Chem. 1991; 37: 785-796. 6. Trivin F, Giraudet P: Microalbuminuria or Paucialbuminuria? Clin Chem. 1988; 34: 209-210. 7. Vaidya VS, Ferguson MA: Bonventre JV: Biomarkers of acute kidney injury. Annu Rev Pharmacol Toxicol. 2008; 48: 463-493. 8. Slattery C, Lee A, Zhang Y, Kelly DJ, Thorn P. et al: In vivo visualization of albumin degradation in the proximal tubule. Kidney Int. 2008; 74: 1480-1486. 9. Kessler MA, Meinitzer A, Petek W, Wolfbeis OS: Microalbuminuria and borderline-increased albumin excretion determined with a centrifugal analyzer and the Albumin Blue 580 fluorescence assay. Clin Chem. 1997; 43: 996-1002. 10. Mogensen CE: Microalbuminuria as a predictor of clinical diabetic nephropathy. Kidney Int. 1987; 31: 673-689. 11. Vigstrup J, Mogensen CE: Proliferative diabetic retinopathy: at risk patients identified by early detection of microalbuminuria. Acta Ophtalmol. 1985; 63: 530-534. 12. Wang TJ, Gona P, Larson MG, Tofler GH, Levy D. et al: Multiple biomarkers for the prediction of first major cardiovascular events and death. N Eng J Med. 2006; 355: 2631-2639. 13. Bernard A, Lauwerys R: Epidemiological application of early markers of nephrotoxicity. Toxicol Lett. 1989; 46: 293-306. 14. Elinder CG, Edling C, Lindberg E, Kågedal B, Vesterberg O: Assessment of renal function in workers previously exposed to cadmium. Br J Ind Med.1985; 42: 754-760. 15. Sperker B, Werner U, Mürdter TE, Tekkaya C, Fritz P. et al: Expression and function of β-glucuronidase in pancreatic cancer: potential role in drug targeting. Naunyn-Schmiedeberg’s Arch Pharmacol. 2000; 362: 110-115. 16. Gonick HC, Kramer HJ, Schapiro AE: Urinary β-glucuronidase activity in renal disease. Arch Intern Med. 1973; 132: 63-69. 17. Motomiya Y, Yamada K, Matsushima S, Ijyuin M, Iriya K: Studies on urinary isoenzymes of lactic dehydrogenase and β-glucuronidase in patients with bladder tumors. Urol Res. 1975; 3: 41-48. 18. Bizoń A, Stasiak K, Milnerowicz H: Activity of alanine aminopeptidase in blood and in urine of smoking and non-smoking smelters. Przegl Lek. 2010; 67: 906-909. 19. Milnerowicz H, Bizoń A, Stasiak K: Activity of gamma-glutamyltransferase in blood of smoking and non-smoking smelters. Przegl Lek. 2010; 67: 910-913. 20. Cobben NA, Drent M, De Vries J, Wouters EF, Van Dieijen-Visser MP, Henderson RF: Serum β-glucuronidase activity in a population of excoalminers. Clin Biochem. 1999; 32: 659-664. 21. Nordberg GF, Jin T, Hong F, Zhang A, Buchet JP, Bernard A: Biomarkers of cadmium and arsenic interactions. Toxicol Appl Pharmacol. 2005; 206: 191-197. 22. Bernard A, Thielemans N, Roels H, Lauwerys R: Association between NAG-B and cadmium in urine with no evidence of a threshold. Occup Environ Med. 1995; 52: 177-180. 23. Jung KY, Lee SJ, Kim JY, Hong YS, Kim SR. et al: Renal dysfunction indicators in lead exposed workers. J Occup Health. 1998; 40:103-109. 24. Noonan CW, Sarasua SM, Campagna D, Kathman SJ, Lybarger JA, Mueller PW: Effects of exposure to low levels of environmental cadmium on renal biomarkers. Environ Health Perspect. 2002; 110: 151-155. 25. Jain S, Drendel WB, Chen ZW, Mathews FS, Sly WS, Grubb JH: Structures of human β-glucuronidase reveals candidate lysosomal targeting and active-site motifs. Nature Stacture Biol. 1996; 3: 375-381. 26. Milnerowicz H, Bizoń A, Witt K, AntonowiczJuchniewicz J, Andrzejak R: Urinary N-acetylbeta-D-glucosaminidase and its isoenzymes in smoking and non-smoking workers at copper foundry occupational co-exposed to arsenic cadmium and lead]. Przegl Lek. 2008; 65: 518-521. A. Bizoń i wsp.