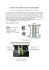Ćwiczenie 21: Membrana do wymiany protonów jako elektrolizer i
Transkrypt
Ćwiczenie 21: Membrana do wymiany protonów jako elektrolizer i
Szkoła z przyszłością szkolenie współfinansowane przez Unię Europejską w ramach Europejskiego Funduszu Społecznego Narodowe Centrum Badań Jądrowych, ul. Andrzeja Sołtana 7, 05-400 Otwock-Świerk ĆWICZENIE L A B O R A T O R I U M F I Z Y K I A T O M O W E J I J Ą D R O W E J Membrana do wymiany protonów jako elektrolizer i ogniwo paliwowe 21 Data pomiaru: ……………..……. Imię i nazwisko: …………………………………………………………...…………………………... Imię i nazwisko: …………………………………………………………...…………………………... 1. CEL ĆWICZENIA Celem ćwiczenia jest zapoznanie się z zasadą działania membrany do wymiany protonów, która może służyć jako elektrolizer lub ogniwo paliwowe. Pomiary wykonane w ćwiczeniu pozwalają także na oszacowanie sprawności zarówno procesu elektrolizy, jak i ponownej przemiany energii zgromadzonej w paliwie wodorowym na elektryczność. 2. UKŁAD DOŚWIADCZALNY Zestaw doświadczalny stanowią: ▪ regulowany zasilacz niskonapięciowy (rys. 1a), ▪ elektrolizer z membraną do wymiany protonów (rys. 1b), ▪ wodorowe ogniwo paliwowe z membraną do wymiany protonów (rys. 1c), ▪ dwie szczelnie zamknięte kolby laboratoryjne z zamocowanymi cylindrami miarowymi (rys. 1d), służące do magazynowania i pomiaru ilości wodoru i tlenu, ▪ zestaw woltomierzy oraz amperomierzy do pomiaru energii dostarczanej do elektrolizera i energii uzyskiwanej z ogniwa paliwowego (rys. 1e), ▪ zestaw oporników z podstawką służący do obciążania wyjścia ogniwa paliwowego (rys. 1f), ▪ zestaw rurek łączących elementy układu i zacisków zamykających przepływ gazów lub wody. Rys. 1 Zestaw pomiarowy a) d) b) c) f) e) „Szkoła z przyszłością” - szkolenie współfinansowane ze środków Europejskiego Funduszu Społecznego R odpływ tlenu odpływ wodoru dopływ tlenu a) dopływ wodoru b) dopływ wody odpływ wody warstwy katalizatora elektron atom wodoru atom tlenu elektrolit warstwy gazodyfuzyjne Rys. 2 Schemat działania membrany do wymiany protonów jako: a) elektrolizera, b) ogniwa paliwowego 3. WSTĘP TEORETYCZNY Membrana do wymiany protonów (ang. proton exchange membrane, w skrócie PEM) ma postać płytki i jest złożona z kilku warstw. Najbardziej wewnętrzna warstwa zrobiona jest elektrolitu, czyli substancji, która przewodzi ładunki elektryczne w postaci jonów dodatnich (tzw. kationów) lub ujemnych (tzw. anionów). W omawianym przypadku chodzi w szczególności o dodatnie jony wodoru, czyli protony. Jednocześnie materiał ten nie powinien przewodzić elektronów, albowiem dla nich przewidziana jest inna droga przepływu. Nie powinien też pozwalać na swobodny przepływ i mieszanie się gazów znajdujących się po obu jego stronach. W membranach PEM często elektrolitem są tanie w produkcji polimery, które są stosunkowo lekkie i można z nich kształtować cienkie elastyczne warstwy (o grubości od kilkudziesięciu do kilkuset µm), a dodatkowo nie grożą wyciekiem (w przeciwieństwie do elektrolitów płynnych). Aby jednak elektrolit ten mógł pracować, niezbędna jest niewielka ilość wody, która tworzy wewnątrz polimeru kanały przewodzące protony. Wynika stąd, że membrany polimerowe nie mogą pracować w temperaturach, w których woda wrze. Często pracują już w temperaturze pokojowej, choć swoją najlepszą wydajność osiągają w temperaturach nieco wyższych. Na elektrolit po obu stronach naniesione są niewielkie warstwy katalizatora reakcji rozkładania wody na wodór i tlen oraz składania jej z powrotem. Katalizatorem najczęściej jest platyna, której dość duży koszt ogranicza powszechne stosowanie ogniw paliwowych na bazie PEM. Warstwa katalizatora musi być oczywiście na tyle cienka, by przepuszczała jony wodoru. Jednocześnie jednak powinna zawierać odpowiednio dużo materiału, by skutecznie katalizować reakcje chemiczne. Jej grubość jest zatem kompromisem pomiędzy przepuszczalnością a zdolnością do katalizowania i wynosi zwykle od 5 do 15 µm. Za każdą warstwą katalityczną znajduje się warstwa gazodyfuzyjna o grubości od ok. 200 do ok. 300 µm, która ma za zadanie równomiernie doprowadzać wodór i tlen do naprzeciwległych stron membrany. Jednocześnie warstwa taka musi zapewnić wydajny odbiór wody, która skrapla się po stronie tlenu jako produkt reakcji z wodorem. Nadmierne gromadzenie się wody może zablokować dostęp gazów do elektrod ogniwa, co uniemożliwi jego działania. Ponadto warstwa gazodyfuzyjna musi dobrze przewodzić elektrony, bowiem to ona stanowi zasadniczą elektrodę ogniwa PEM. Sama warstwa katalizatora (na której faktycznie elektrony są oddzielane lub przyłączane do jonów wodoru) jest zbyt cienka, by efektywnie przewodzić prąd. Dobrym materiałem na warstwy gazodyfuzyjne jest włóknina węglowa lub papier węglowy impregnowane preparatami hydrofobowymi, tj. takimi, które zapobiegają wsiąkaniu wody. Innym rozwiązaniem jest drobna metalowa siateczka, np. ze stali nierdzewnej. Każdy z materiałów ma swoje zalety i wady, niemniej w każdym przypadku dość kosztowne jest uzyskanie odpowiedniej struktury przestrzennej. -2- „Szkoła z przyszłością” - szkolenie współfinansowane ze środków Europejskiego Funduszu Społecznego Warstwy gazodyfuzyjne wraz z warstwami katalizatora tworzą tzw. elektrody gazodyfuzyjne, do których doprowadza się gazy i podłącza obwód prądowy. W celu uzyskania dobrego styku wszystkie wcześniej wymienione warstwy sprasowuje się w podwyższonej temperaturze. Doprowadzanie gazów do obu stron urządzenia zapewniają zwykle odpowiednie płytki z systemem kanalików, choć w przypadku PEM używanej w ćwiczeniu dostęp gazów jest swobodny. Teoretycznie membrana do wymiany protonów może pracować zarówno jako ogniwo elektrolityczne (elektrolizer), które pod wpływem przyłożonego prądu elektrycznego rozkłada wodę na wodór i tlen, jak i jako ogniwo paliwowe, które ze zmagazynowanego wodoru i tlenu produkuje wodę oraz energię elektryczną. W praktycznym zastosowaniu wygodniej jednak zoptymalizować tę konstrukcję w kierunku jednego z wymienionych zastosowań, a wprowadzone zmiany często uniemożliwiają odmienne użycie pod groźbą uszkodzenia urządzenia. Działanie elektrolizera opisują w skrócie następujące reakcje chemiczne: 2H2O → 4H+ + 4e- + O2 2H+ + 2e- → H2 przy czym jony wodoru przechodzą przez elektrolit ogniwa, zaś elektrony poruszają się w zewnętrznym obwodzie elektrycznym pod wpływem przyłożonego napięcia. Pierwsza z reakcji zachodzi na anodzie, zaś druga na katodzie elektrolizera. W rezultacie przy anodzie pozostaje tlen, zaś na katodzie wydziela się wodór, które można łatwo zebrać w oddzielnych pojemnikach. Aby opisać działanie ogniwa paliwowego należy zapisać przeciwne reakcje: H2 → 2H+ + 2e4H + 4e- + O2 → 2H2O + z których pierwsza odbywa się na anodzie, a druga na katodzie. Ponownie protony przechodzą przez elektrolit, zaś elektrony poruszają się w zewnętrznym obwodzie elektrycznym, tym razem wykonując pracę użyteczną. Oczywiście żaden z tych procesów nie ma sprawności 100%, stąd energia elektryczna uzyskana z paliwa wodorowego jest mniejsza niż energia chemiczna zgromadzona w tym paliwie, a ta – mniejsza niż energia włożona w produkcję wodoru. Energia prądu elektrycznego dostarczonego bądź uzyskanego z urządzenia wyposażonego w PEM może być zmierzona przy pomocy woltomierza, amperomierza i zegara. Wyraża się ona wzorem: E = U ⋅ I ⋅t (1) gdzie U to napięcie zmierzone na zaciskach ogniwa, I to natężenie prądu przez nie płynącego, zaś t to czas, w jakim ogniwo jest włączone w obwód elektryczny. W przypadku, gdy napięcie lub natężenie zmienia się podczas pomiaru, lepiej jest notować wartości w odpowiednich przedziałach czasu, a przyrost energii obliczać oddzielnie dla każdego przedziału i na koniec zsumować – uzyskuje się wtedy nieco dokładniejszą (choć nadal przybliżoną) wartość energii po n-tym pomiarze (En). Do obliczenia chwilowego przyrostu energii ∆Ei powinno się w takim przypadku użyć wartości średniej napięcia i natężenia pomiędzy pomiarami: ∆E i = U i + U i +1 I i + I i +1 ⋅ ⋅ ∆ti 2 2 n −1 En = ∑ ∆E (2) i i =1 Ui i Ii oznaczają tu odpowiednio wartości napięcia i natężenia prądu zmierzone w chwili ti, zaś ∆ti = ti+1 – ti i jest to czas pomiędzy dwoma kolejnymi pomiarami. Energię zmagazynowaną w wodorze można obliczyć na podstawie znajomości tzw. ciepła spalania (ang. upper calorific value), które w przypadku wodoru wynosi Ho ≈ 286 kJ/mol. Jest to wartość odmienna od tzw. wartości opałowej (ang. lower calorific value), która dla wodoru wynosi -3- „Szkoła z przyszłością” - szkolenie współfinansowane ze środków Europejskiego Funduszu Społecznego Hu ≈ 242 kJ/mol. Różnica między nimi wynika z tego, że podczas zachodzenia reakcji utleniania część wyzwolonej energii zostaje zużyta na odparowanie wody będącej produktem tej reakcji. Jeśli para skropli się z powrotem jeszcze w obrębie urządzenia, to dodatkowo ogrzewa je, więc można tę energię odzyskać. Sytuacji tej odpowiada wartość ciepła spalania, natomiast jeśli para wodna ulatuje z urządzenia zabierając bezpowrotnie część energii, wtedy mamy do czynienia z energią równą wartości opałowej. W przypadku ogniwa z membraną PEM, które pracuje w niskich temperaturach, para ulega skropleniu, stąd do obliczeń używamy zawsze wartości Ho. Ciepło spalania i wartości opałowa wyrażone są w kJ/mol, czyli odnoszą się do liczności materii w gazie, natomiast w układzie wykorzystanym w tym ćwiczeniu możliwy jest pomiar objętości gazów (zarówno wodoru, jak i tlenu). Zależność pomiędzy licznością a objętością opisuje równanie stanu gazu doskonałego (zwane też równaniem Clapeyrona): p ⋅V = n ⋅ R ⋅T (3) gdzie n to wspomniana liczność materii, V to objętość gazu, p – jego ciśnienie, T – jego temperatura, zaś R to uniwersalna stała gazowa wynosząca 8,314 J/(mol·K). Przekształcając i uzupełniając ten wzór o ciepło spalania można uzyskać równanie na energię zmagazynowaną w wodorze: Ewodoru = Ho ⋅ n = Ho ⋅ p ⋅V R ⋅T R zasilacz A A V V wodór elektrolizer tlen ogniwo paliwowe zaciski Rys. 3 Schemat połączeń aparatury w ćwiczeniu -4- (4) „Szkoła z przyszłością” - szkolenie współfinansowane ze środków Europejskiego Funduszu Społecznego 4. PRZEBIEG DOŚWIADCZENIA A) Przed uruchomieniem urządzeń sprawdzić poprawność połączeń elektrycznych wedle schematu załączonego na rys. 3 oraz czy wszystkie zaciski zamykające przepływ gazów w rurkach są zakręcone. W razie wątpliwości lub nieprawidłowości skonsultować się z obsługą laboratorium. B) Upewnić się, że oba pokrętła zasilacza są ustawione na zero (tj. skręcone maksymalnie w lewo), po czym włączyć zasilacz przyciskiem z tyłu obudowy. Uruchomić także woltomierze ustawiając je na zakres 2000 mV oraz amperomierze ustawiając je na zakres 20 A. C) Otworzyć zaciski odprowadzające gaz z rurek na zewnątrz, po czym nastawić na zasilaczu elektrolizera napięcie równe ok. V oraz prąd równy ok. A. UWAGA: nie przekraczać napięcia 2 V i natężenia 2 A! Na membranie elektrolizera powinna być widoczna produkcja wodoru i tlenu. Odczekać kilka minut, aż wyprodukowane gazy wypełnią rurki. Wyciekający z rurek nadmiar wody wycierać szmatką. Po wypełnieniu rurek gazami wyzerować na zasilaczu napięcie i natężenie prądu oraz zakręcić zaciski zamykające wypływ gazu z rurek. UWAGA: w wypadku, gdy woda zalewa znaczącą część membrany ogniwa paliwowego, poprosić o pomoc obsługę laboratorium. D) Otworzyć zaciski na rurkach prowadzących od ogniwa paliwowego do dwóch kolb służących do magazynowania wodoru. E) Ze znajdujących się w sali laboratoryjnej termometru i barometru odczytać temperaturę i ciśnienie panujące w sali. F) Na zbiorniku wody ponad kolbą zbierającą wodór przyczepić (delikatnie!) skalę objętości tak, by zero na skali pokrywało się z początkowym poziomem wody. G) Upewnić się, że w obwodzie ogniwa paliwowego nie jest wpięty żaden opornik, po czym nastaV oraz prąd Iwe równy ok. A. wić na zasilaczu napięcie Uwe równe ok. H) W odpowiednio dobranych odstępach czasu (np. co minutę) notować w tabeli 2 wartości napięcia Uwe i natężenia Iwe prądu z zasilacza, poziomy wody w obu zbiornikach nad kolbami, a także wartości napięcia Uwy na ogniwie paliwowym i natężenia Iwy prądu przez to ogniwo płynącego. Wykonać w ten sposób przynajmniej 6 pomiarów. I) Podłączyć do obwodu ogniwa paliwowego opornik o wartości więcej pomiarów tak jak w poprzednim punkcie. Ω i wykonać następne 6 lub J) Wyłączyć zasilanie elektrolizera skręcając oba pokrętła w lewo do oporu i wykonać przynajmniej jeszcze 8 pomiarów takich jak w poprzednich punktach. UWAGA: gdyby w kolbach zabrakło któregoś z gazów i w rurkach pojawiła się woda, należy od razu zakręcić zaciski oddzielające ogniwo paliwowe od kolb! K) Po zakończonym pomiarze usunąć opornik z obwodu ogniwa paliwowego i zakręcić zaciski na rurkach. L) Opracować wyniki pomiaru uzupełniając tabelę 2 o wartości energii włożonej w elektrolizer Ewe, energii zgromadzonego w wodorze Ewodoru oraz energii uzyskanej na ogniwie paliwowym Ewy, obliczone zgodnie ze wzorami 1, 2 i 4. M) Wykonać wspólny wykres wartości tych trzech energii w zależności od czasu. N) Na wykonanym wykresie wytyczyć linie proste odpowiadające poszczególnym punktom ćwiczenia. UWAGA: jeśli w obrębie danego przedziału na wykresie widoczne są wyraźne odchyłki od linii prostej, należy ograniczyć się do tych punktów wykresu, które wykazują liniowość. -5- „Szkoła z przyszłością” - szkolenie współfinansowane ze środków Europejskiego Funduszu Społecznego O) Dla każdej z wytyczonych prostych obliczyć współczynniki nachylenia, które odpowiadają średniej mocy danej części układu w wybranych przedziałach czasu. Obliczone współczynniki zanotować w tabeli 1 jako Pwe (dla linii prostych na wykresie Ewe), Pwodoru (dla prostych na wykresie Ewodoru) i Pwy (dla prostych na wykresie Ewy). P) Uzupełnić tabelę 1 o wartości sprawności różnych procesów. Dla pomiarów wykonanych w punkcie H ćwiczenia odpowiedni jest wzór: P η ( H ) = wodoru ( H ) Pwe ( H ) który opisuje sprawność procesu elektrolizy. Dla pomiarów wykonanych w punkcie I odpowiedni jest wzór: Pwy ( I ) η( I ) = Pwodoru ( H ) − Pwodoru ( I ) który opisuje sprawność ogniwa paliwowego (różnica w mianowniku odpowiada tej ilości wodoru, która została wyprodukowana w elektrolizerze, ale nie została zmagazynowana w kolbach, bo została wchłonięta przez ogniwo paliwowe). Dla pomiarów wykonanych w punkcie J ćwiczenia odpowiedni jest wzór: P η ( J ) = wy ( J ) Pwe ( J ) który opisuje sprawność ogniwa paliwowego pracującego tylko podczas zasilania wodorem i tlenem zmagazynowanym wcześniej w kolbach. -6- „Szkoła z przyszłością” - szkolenie współfinansowane ze środków Europejskiego Funduszu Społecznego ĆWICZENIE LABORATORIUM FIZYKI ATOMOWEJ I JĄDROWEJ 21 Membrana do wymiany protonów jako elektrolizer i ogniwo paliwowe Data pomiaru:................................ Imię i nazwisko:.......................................................................................................... Imię i nazwisko:.......................................................................................................... Szkoła, klasa:............................................................................................................. ciepło spalania wodoru: Ho ≈ 286 kJ/mol uniwersalna stała gazowa: R = 8,314 J/(mol·K) energia zmagazynowana w wodorze o objętości V, temperaturze T i ciśnieniu p: H ⋅ p ⋅V E wodoru = o R ⋅T energia (praca) prądu płynącego w obwodzie elektrycznym w czasie t: ∆E = U ⋅ I ⋅t przybliżona energia (praca) prądu w obwodzie w czasie od ti do ti+1 przy napięciu zmieniającym się od Ui do Ui+1 i natężeniu zmieniającym się od Ii do Ii+1: ∆Ei = U i + U i +1 I i + I i+1 ⋅ ⋅ (ti +1 − ti ) 2 2 całkowita energia (praca) prądu w obwodzie w czasie od początku pomiaru do tn: n −1 E n = ∑ ∆E i = ∆E1 + K + ∆ E i + K + ∆E n −1 i =1 TABELA 1 punkt ćwiczenia Pwodoru [W] Pwe [W] Pwy [W] η H ± ± I ± ± ± ± ± ± ± J η(H ) = η( I ) = Pwodoru ( H ) Pwe ( H ) Pwy ( I ) Pwodoru ( H ) − Pwodoru ( I ) η(J) = Pwy ( J ) Pwe ( J ) -7- ± TABELA 2 i,n t [s] ciśnienie atmosferyczne p = ......... ± ...... hPa Iwe [A] Uwe [mV] Vwodoru [ml] temperatura otoczenia T = ......... ± ...... °C Iwy [A] Uwy [mV] ∆Ewe [J] Ewe [J] Ewodoru [J] ∆Ewy [J] Ewy [J] 1 ± ± ± ± ± ± ± ± ± ± ± 2 ± ± ± ± ± ± ± ± ± ± ± 3 ± ± ± ± ± ± ± ± ± ± ± 4 ± ± ± ± ± ± ± ± ± ± ± 5 ± ± ± ± ± ± ± ± ± ± ± 6 ± ± ± ± ± ± ± ± ± ± ± 7 ± ± ± ± ± ± ± ± ± ± ± 8 ± ± ± ± ± ± ± ± ± ± ± 9 ± ± ± ± ± ± ± ± ± ± ± 10 ± ± ± ± ± ± ± ± ± ± ± 11 ± ± ± ± ± ± ± ± ± ± ± 12 ± ± ± ± ± ± ± ± ± ± ± 13 ± ± ± ± ± ± ± ± ± ± ± 14 ± ± ± ± ± ± ± ± ± ± ± 15 ± ± ± ± ± ± ± ± ± ± ± 16 ± ± ± ± ± ± ± ± ± ± ± 17 ± ± ± ± ± ± ± ± ± ± ± 18 ± ± ± ± ± ± ± ± ± ± ± 19 ± ± ± ± ± ± ± ± ± ± ± 20 ± ± ± ± ± ± ± ± ± ± ±