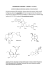Wykład 10
Transkrypt
Wykład 10
Aldehydy i Ketony Grupa karbonylowa: C O Aldehyd R CO H Keton R1 CO R2 1 Aldehyd = „alcohol dehydrogenatus” alkohol odwodorniony Nazewnictwo: 1. alkan + al grupa aldehydowa = lokant 1 propanal CH3CH2CHO 1,3-propanodial (aldehyd malonowy) O O C CH2 C H H 2. aldehyd + nazwa kwasu karboksylowego, który powstaje z aldehydu CH3CHO aldehyd octowy (etanal) 2 3. formylo – grupa aldehydowa jako podstawnik C O H COOH CHO formylocyklopentan kwas o-formylobenzoesowy 3 H C O metanal ( formaldehyd, aldehyd mrówkowy) H CH3 C O etanal ( acetaldehyd, aldehyd octowy ) H CH3CH2CH2 C O butanal ( aldehyd masłowy ) H 4 Aldehydy aromatyczne ArCHO mają końcówkę -esowy C O H 12 aldehyd benzoesowy ( benzaldehyd ) CHO aldehyd 2-naftoesowy 5 Ketony Nazewnictwo: 1. alkan + on O CH3CCH3 R1 CO R2 keton jak najniższy lokant propanon ( aceton , keton dimetylowy ) O CH3CH2CH2CCH3 2-pentanon ; pentan-2-on keton metylowo-propylowy O cykloheksanon O O CH3CH2CCH2CCH3 2,4-heksanodion ; heksano-2,4-dion 6 2. fenony – ketony, których podstawnikiem jest grupa fenylowa O C CH3 O C acetofenon (keton fenylowo-metylowy) benzofenon (keton difenylowy) 7 3. „okso” – grupa ketonowa jako podstawnik O CH3CH2CCH2COOH 5 4 3 2 1 O CH3CH2CCH2CHO kwas 3-oksopentanowy 3-oksopentanal Ważność grup funkcyjnych w nazewnictwie związków: Kwasy > aldehyd > keton > alkohol > fenol > eter > > alken > alkin > halogenek, alkan 8 O grupa acylowa ( acyl ) R C HC O CH3 C grupa formylowa (formyl ) O C O grupa acetylowa ( acetyl ) grupa benzoilowa ( benzoil ) 9 O O CH3CCH2CCH3 2,4-pentanodion O O CH3CCH2CCH3 2,4-pentanodion acetyloaceton O CH3 C CH C CH3 CH3 2 1 5 4 3 4- metylo-3-penten-2-on 4-metylopent-3-en-2-on 10 Otrzymywanie aldehydów 1. Utlenianie alkoholi 1o RCH2OH PCC CH2Cl2 RCHO PCC = CrO3 + chlorowodorek pirydyny 2. Redukcja chlorków kwasowych redukcja Rosenmunda O R C Cl H2 Pd (S) R C O H 3. Ozonoliza 11 Aldehydy aromatyczne - otrzymywanie CH3 CHO 1. O2 / kat 2. H2O CH3 Cl2 CHCl2 CHO H2O hν 12 Otrzymywanie ketonów 1. Utlenianie alkoholi 2o RCHR' OH CrO3 H2SO4 RCR' O 2. Reakcja odczynnika Grignarda z nitrylami R CN + R'MgX RCR' NMgX H 3O RCR' O 13 3. Reakcja Friedel’a-Craftsa O RC Cl O C R AlCl3 4. Z alkinów (reakcja Kuczerowa) R C C R' H3O , Hg 2 H2O R H CC HO R' R C CH2 R' O Ketony metylowe z terminalnych alkinów 5. Ozonoliza 14 Reakcje związków karbonylnych Charakterystycznymi reakcjami grupy karbonylowej są: 1. Addycja nukleofilowa AN 2. Kwasowość wodoru α 15 Addycja nukleofilowa AN δ+ δ− C O C O C O Gdy odczynnik jest silnym nukleofilem: C O CO Nu H-A COH + A Nu Nu Nu = H ( NaBH4 , LiAlH4 ) R ( RMgX ) CN ( HCN ) ROH 16 Często reakcji addycji nukleofilowej towarzyszy reakcja eliminacji wody ( jest to reakcja następcza ): δ+ δ− CO CO CO NuH2 C Nu + H2O NuH2 nukleofil NuH2 = NH3 produkt >C=NH RNH2 >C=NR H2NOH >C=NOH H2NNH2 >C=NNH2 itp 17 Reakcje addycji nukleofilowej są katalizowane przez kwasy i zasady. Słabe nukleofile wymagają katalizy kwasowej: rola kwasu polega na protonowaniu grupy karbonylowej co zwiększa elektrofilowe własności węgla karbonylowego R1 R2 CO + H R1 R2 COH R1 R2 COH + Nu Nu R1 C OH R2 Katalityczne działanie zasad polega na przekształcaniu odczynników nukleofilowych w aniony. 18 Niektóre reakcje addycji nukleofilowej AN do grupy karbonylowej: ROH 2 ROH H+ C O HCN 1. NaBH4 2. H2O 1. RMgX 2. H3O+ OH C OR hemiacetal ; hemiketal OR C OR acetal ; ketal OH C CN cyjanohydryna OH C H OH C R 19 Niektóre reakcje addycji nukleofilowej AN do grupy karbonylowej: RSH OH C SR hemitioacetal; hemitioketal C O 2 RSH H+ SR C SR tioacetal; tioketal 20 Addycja pochodnych amoniaku amina I rz CO RNH2 C NR imina zasada Schiffa amina II rz 2 CH2 1 CO R2NH 2 1 CH C NR2 enamina C NOH oksym hydroksyloamina CO H2N-OH semikarbazyd CO O H2NNHCNH2 O C NNHCNH2 semikarbazon 21 hydrazyna CO H2N-NH2 C N NH2 hydrazon fenylohydrazyna CO H2N-NHC6H5 C N N C6H5 H fenylohydrazon 2,4-dinitrofenylohydrazyna O 2N CO H 2N N H NO2 O 2N CNN H NO2 2,4-dinitrofenylohydrazon 22 Hemiacetale, hemiketale, acetale i ketale Rozpuszczenie aldehydu lub ketonu w alkoholu wytwarza równowagę między nim a produktem reakcji z alkoholem – hemiacetalem lub hemiketalem R H CO R1 R2 CO R'OH OH C OR' R H hemiacetal półacetal R'OH OH C OR' hemiketal półketal R1 R2 23 Równowagowe stężenia półacetali i półketali są zwykle niewielkie i zależą od budowy związków karbonylowych. Ważnym wyjątkiem są hydroksy aldehydy i hydroksy ketony, których budowa umożliwia powstanie cyklicznych półacetali (półketali) przez wewnątrzcząsteczkowe przyłączenie grupy hydroksylowej do grupy karbonylowej. Pierścienie muszą być 5- lub 6-członowe. O CH2CH2CH2CH2C H O H O CH3CH2CH2CH2C H O H CH2 CH2 CH2 CH2 OH C H O OH O OH O 24 Otrzymywanie hemiacetali i hemiketali katalizowane przez zasady: C2H5OH + NaOH C2H5O Na + H2O jon C2H5O- powstaje w bardzo niewielkich ilościach ale wystarczających gdyż jest on bardzo silną zasadą R C O H + OC2H5 O R C OC2H5 + H O C2H5 H OH R C OC2H5 + OC2H5 H W środowisku zasadowym mogą powstać tylko półacetale ( półketale) 25 Otrzymywanie acetali ( przez roztwór związku karbonylowego w bezwodnym alkoholu przepuszcza się gazowy HCl). R O H + H+ C H O R' - H+ R H C O R' + H R OH C H O R' R' O H - H2O R + H2O H H R O R' C H O R' C O R' - H+ + H+ R H C O R' R O R' C H O R' Ketale i acetale powstają tylko w obecności kwasu. 26 Tworzenie się ketali nie zachodzi w przypadku ketonów i prostych alkoholi. Tworzą się natomiast ketale cykliczne: R1 HO CH2 CO + HO CH2 R2 H+ R1 O CH2 C + H2O R2 O CH2 Acetale i cykliczne ketale hydrolizują w obecności wodnych roztworów kwasów, są natomiast trwałe w wodnych roztworach zasad 27 Utlenianie aldehydów Aldehydy są reduktorami i są łatwo utleniane nawet przez słabe utleniacze jak : Ag+ i Cu2+ Odczynnik Tollensa (amoniakalny roztwór AgNO3) RCHO + 2 [Ag(NH3)2]OH RCOO NH4 + 2Ag + H2O + 3NH3 wytrąca się Ag w postaci lustra 28 Utlenianie aldehydów Odczynnik Fehlinga (siarczan VI miedzi II w alkalicznym roztworze winianu sodu) Odczynnik Benedicta (siarczan VI miedzi II w alkalicznym roztworze cytrynianu sodu) oba roztwory niebieskie RCHO + 2Cu2+ + 5OH RCOO + Cu2O + 3H2O wytrąca się czerwony osad Cu2O Ketony nie ulegają w tych warunkach utlenieniu – odczynniki te służą do odróżnienia ketonów od aldehydów. 29 Redukcja aldehydów i ketonów O C H Ni , H2 25oC Ni , H2 100oC NaBH4 O C H CH2OH CH2OH gdy C=O i C=C nie są sprzężone 30 Redukcja Wolffa - Kiżnera C O + H2N NH2 C O C O C N NH2 H2NNH2 , NaOH ∆t H2NNH2 , KOH ∆t NaOH st ∆t CH2 CH2 CH2 Redukcja Clemmensena C O Zn (Hg) HCl CH2 31 Tautomeria keto - enolowa O CCCCCCCC ε δ γ β α α β Związki karbonylowe zawierające 1 lub więcej atomów wodoru przy atomie węgla α do grupy karbonylowej ulegają szybkim wzajemnym przemianom z odpowiadającymi im enolami. Te szybkie przemiany między dwoma odmiennymi strukturalnie związkami stanowią specjalny rodzaj izomerii zwanej tautomerią. O C CH α forma ketonowa OH C C forma enolowa 32 Tautomery – izomery różniące się położeniem atomu H i wiązania wielokrotnego, pozostające ze sobą w łatwo ustalającej się równowadze. 33 amid - imid R O C NH2 OH C R NH laktam - laktim O C NH OH CN fenol - keton OH O N N H 34 nitrozo - oksym R2CH N O R2C N OH nitro - aci R2CH N O O R2CH N odmiana nitro O O R2C N O OH odmiana aci imina - enamina R2CH CR NR R2C CR NHR 35 Kwasowość wodoru α O α β R C C C H H ten jest kwaśny Ka dla Hα to 10-19 – 10-20 Ka dla acetylenu 10-25 Ka dla ROH 10-18 ten już nie jest 36 Kiedy związek karbonylowy straci Hα powstały anion stabilizowany jest rezonansem: O H R C CHR' Z O R C CHR' O R C CHR' A B jon enolanowy A - jest faworyzowane bo C=O mocniejsze niż C=C (ta forma jest bardziej reaktywna) B - jest faworyzowane bo O jest bardziej elektroujemny 37 forma ketonowa OH R C CHR' CH3C O H O CH3CCH3 OO CH3CCCH3 forma enolowa OH R C CHR' CH2 C OH H OH CH3C CH2 OOH CH3CC CH2 10-4 % 10-4 % 10-2 % 38 W związkach β-dikarbonylowych (dwie grupy karbonylowe rozdzielone grupą CH2) ilość enolu jest znacznie większa – dla acetyloacetonu wynosi już 80% O OH CH3 C CH C CH3 O O CH3 C CH2 C CH3 OH O CH3 C CH C CH3 acetyloaceton 39 Większa stabilność formy enolowej w tych związkach wynika z istnienia struktur rezonansowych i wewnątrzcząsteczkowego wiązania wodorowego. O CH3 H O CH2 O CH3 CH3 H O CH3 O CH O CH3 CH3 O CH CH3 H O CH H O CH3 CH3 O CH CH3 40 Nie ulegają tautomerii keto-enolowej a więc nie dają anionu enolanowego te związki karbonylowe, które nie mają wodoru przy węglu α α O C H benzaldehyd C2H5 CH3 C CHO CH3 α O C α benzofenon 2,2-dimetylobutanal 41 Kurkumina –jest składnikiem m.in. przyprawy „Curry”. O O forma ketonowa HO OH OCH3 OCH3 OH O HO OH OCH3 OCH3 O forma enolowa OH HO OH OCH3 OCH3 42 Niektóre chemiczne skutki enolizacji 1. Racemizacja – powstający enol jest achiralny O C C6H5 C2H5 H CH3 OH lub H3O OH C2H5 C C C6H5 CH3 C2H5 CH3 H O C C6H5 R S 2. Deuterowanie w położeniu α O CH3 C CH3 D2O kwas lub zasada O CD3 C CD3 43 3. Halogenowanie w położeniu α O CC H O CC X + X2 + HX X2 = Cl2, Br2, I2 w środowisku kwaśnym HO H C C R + X2 H H+ HO HCCR X + HX w środowisku silnie zasadowym – reakcja haloformowa HO NaOH H C C R + 3 X2 H XO NaOH XCCR X RCOONa + CHX3 haloform 44 4. Reakcja aldolowa O 2 CH3 C H NaOHaq OH O CH3 C CH2 C H H 3-hydroksybutanal „aldol” Reakcji aldolowej bardzo często towarzyszy reakcja eliminacji wody z cząsteczki aldolu lub hydroksyketonu (reakcja kondensacji). OH O CH3 C CH2 C H H ∆t O CH3CH=CHC H α,β – nienasycony aldehyd 45 mechanizm reakcji aldolowej O CC H H O CC H + OH O δ+ R C H δ+ CC HO O R CCC HH H O O R CCC H H O H + O CC H OH ∆t + HOH O R CCC H H 46 Mieszana reakcja aldolowa OH CH3CHCH2CHO + OH CH3CH2CHCH2CHO CH3CHO + CH3CH2CHO NaOHaq + OH CH3CHCHCHO CH3 + OH CH3CH2CHCHCHO CH3 47 CH3CHO O CH3C H O CH3CH2C H NaOHaq + O CH2 C H + O CH2 C H CH2 C O H CH2 C O H OH CH3CHCH2CHO OH CH3CH2CHCH2CHO 48 CH3CH2C CH3CH2C CH3C NaOHaq O H O H O H + + O CH C H CH3 O CH C H CH3 O CH C H CH3 H CH3 C C O H OH CH3CH2CHCHCHO CH3 OH CH3CHCHCHO CH3 49 Reakcja Cannizzaro ( stęż. NaOH : 50 – 60% ) reakcja oksydacyjno-redukcyjna 2 C6H5 C O H 60% NaOH C6H5COOH + C6H5CH2OH Dotyczy tylko aldehydów nie posiadających Hα 50 Aldehydy aromatyczne mają przyjemne zapachy benzaldehyd (aldehyd benzoesowy) migdały CHO wanilina CHO OCH3 OH 51 aldehyd salicylowy zapach łąki CHO OH aldehyd cynamonowy (E) CH=CHCHO E H H CHO 52