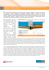BR-1 BR-2 BR-3 BR-4 BR-5 BR-6 BR-7 BR-8 BR-10 BR-11
Transkrypt
BR-1 BR-2 BR-3 BR-4 BR-5 BR-6 BR-7 BR-8 BR-10 BR-11
Nazwisko, imię (DRUKOWANYMI LITERAMI)........................................................................................................................................................................................................................................................................................................................................................................... http://sylwester_stepniak.users.sggw.pl e-mail: [email protected] Ćwiczenia z chemii analitycznej – Analiza kationów Badanie zabarwienia płomienia + Schemat identyfikacji kationów: {Ag , Cu2+, Fe3+, Fe2+, Mn2+, Ca2+, Mg2+, Al3+, Zn2+, Ba2+, NH4+, K+} 1. Zanurzyć drucik platynowy w stężonym HCl BR-1 2. Wyżarzyć w płomieniu palnika Wytrąca się osad: 3. Zanurzyć drucik platynowy Brak osadu: + HClaq w stężonym HCl Cu2+, Fe3+, Fe2+, Mn2+, Ca2+, Mg2+, Al3+, Zn2+, Ba2+, NH4+, K+ AgCl 4. Zanurzyć drucik platynowy Biały osad w roztworze badanym BR-4 5. Wprowadzić drucik do górnej Wytrąca się biały osad: Dekantacja części płomienia palnika Brak osadu: Zn(OH)2, Al(OH)3, Ca(OH)2, Mg(OH)2 2+ + Ba , NH4 , K + NaOH 6. Obserwować zabarwienie płomienia + Kation Wytrąca się kolorowy osad: Fe(OH)2, + NH4OH Fe(OH)3, zielony, brunatnoczerwony, różowy, + KI niebieski BR-9 BR-8 BR-3 Osad Wytrąca się osad: Zn(OH)2 + 2 OH = [Zn(OH)4] nie rozpuszcza się: Mn2[Fe(CN)6] - biały Al(OH)3 + OH- = [Al(OH)4]- Ca(OH)2, Mg(OH)2 Osad rozpuszcza się: - + KI BR-5 2 Ag+ + 2 OH- = Ag2O + H2O 2- BR-7 + NH4OH (nadmiar) żółty osad Wytrąca się biały osad: BaSO4 BR-12 + HClO4 (zwilżony papierek uniwersalny barwi się na niebiesko) + K4[Fe(CN)6] Osad rozpuszcza się: + H2C2O4 + NaOH płomienia Wytrąca się biały osad: - Zn(OH)2 + 6 NH4OH = [Zn(NH3)6] + 2 OH + 6 H2O Wytrąca się żółty osad: Osad nie rozpuszcza się: 3+ Ceglastoczerwone Różowofioletowe BR-11 Wydziela się NH3 Badanie zabarwienia 2+ Ceglastoczerwone + H2SO4 Fe4[Fe(CN)6]3 - niebieski BR-6 Ag+ + I- = AgI szary osad Ca żółty osad BR-10 + NaOH Jasnozielone 2+ + K4[Fe(CN)6] AgCl + 2 NH4OH = [Ag(NH3)2]+ + 2 H2O BR-2 Ba K+ Cu2+ + 2 I- = CuI2 + NaOH (nadmiar) Biały osad rozpuszcza się: Niebieskozielone 2+ Cu Mn(OH)2, Cu(OH)2 Barwa płomienia 2+ Al + 3 NH4OH= Al(OH)3 + 3 2 Zn2+ + K4[Fe(CN)6] = Zn2[Fe(CN)6] + 4 K+ KClO4 Ceglastoczerwona barwa Wytrąca się biały osad: płomienia: Ca2+ CaC2O4 NH4+ W badanym roztworze znajduje się kation – Symbol:………………, Nazwa:…………………………………………..