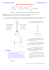+ załącznik ćwiczenie 3
Transkrypt
+ załącznik ćwiczenie 3
IMIĘ NAZWISKO ………………………………… ……………………………..GRUPA …………….. ĆWICZENIE NR 3 Oznaczanie kwasu acetylosalicylowego metodą spektrofotometrii w nadfiolecie Substancją farmakologicznie czynną w tabletce polopiryny jest kwas acetylosalicylowy, którego wzór strukturalny podano poniżej: Kwas acetylosalicylowy w środowisku alkalicznym ulega hydrolizie do: CEL ĆWICZENIA Oznaczanie kwasu acetylosalicylowego w tabletkach metodą spektrofotometrii w nadfiolecie WYKONANIE 1. Przygotowanie roztworów krzywej wzorcowej Do 5 kolbek poj. 100 cm3 odmierzono kolejno 1, 2, 3, 4 i 5 cm3 roztworu podstawowego kwasu salicylowego o stężeniu …... mg/100 cm3 oraz po 1 cm3 roztworu NaOH 0,1 mol/dm3. Po uzupełnieniu wodą destylowaną do kreski (objętości 100 cm3) roztwory wymieszano. Sposób obliczenia stężenia kwasu salicylowego w przygotowanych roztworach wzorcowych przedstawiono poniżej: 2. Wyznaczenie analitycznej długości fali (λmax ) kwasu salicylowego Analityczną długość fali, kwasu salicylowego, wyznaczono z przebiegu widma UV w zakresie 200 nm do 400 nm , dla roztworu wzorcowego o stężeniu 3mg/100 cm3 mierzonego wobec wody destylowanej jako odnośnika (ryc. 1.). za λmax przyjęto nm Zmierzono absorpcję przygotowanych roztworów wzorcowych przy λmax , a wyniki zamieszczono w tabeli 1. Absorpcjometria – protokół opracowała dr B. Szafran-Urbaniak 1 Tabela 1. ………………………………………………………………………………………... ROZTWORY WZORCOWE KWASU SALICYLOWEGO c[mg/100cm3] A 3. Wyznaczenie zależności A = f( c ) metodą najmniejszych kwadratów Parametry równania (A = ac + b) zależności absorbancji (A) od stężenia kwasu salicylowego (c) w roztworach wzorcowych w [mg/100cm3] wyznaczono metodą najmniejszych kwadratów, korzystając z następujących wzorów: a= b= r= n xy n x 2 y x y x a x n n x 2 a= b= n xy x y 2 x 2 n y 2 y 2 r= Równanie krzywej wzorcowej przyjmuje postać:.............................................................. krzywą wzorcową poprowadzono przez dwa teoretyczne punkty c1 = ................., A1 = ................. c2 = ................., A2 = ................. Wykres krzywej wzorcowej do oznaczania stężenia kwasu salicylowego metodą spektrofotometrii w nadfiolecie przedstawiono poniżej na ryc. 2. Ryc. 2. ………………………………………………………………………………………… Absorpcjometria – protokół opracowała dr B. Szafran-Urbaniak 2 4. Oznaczenie kwasu salicylowego w tabletce Tabletkę …………………………………………………………………….. rozkruszono bagietką w zlewce, do której dodano 10 cm3 NaOH 0,1 mol/dm3. Po dokładnym rozdrobnieniu masy tabletki dodano jeszcze 20 cm3 NaOH 0,1 mol/dm3. Zawartość zlewki wymieszano i przeniesiono ilościowo po przez bibułowy sączek do kolby poj. 250 cm 3. Zlewkę kilka razy przepłukano małymi porcjami NaOH i przesączono do kolby miarowej. Po uzupełnieniu kolby roztworem NaOH do objętości 250 cm3 pobrano 2 cm3 przygotowanego roztworu i przeniesiono do kolby poj. 100 cm3 uzupełniając wodą destylowaną. Wykreślono widmo UV badanego roztworu oraz zmierzono pięciokrotnie absorbancję analizy przy λmax = nm a wyniki zamieszczono w tabeli 2. Tabela 2. ……………………………………………………………………………………… POMIAR A 1 2 3 4 5 WARTOŚĆ ŚREDNIA 5. Obliczenie zawartości kwasu acetylosalicylowego w …………………………………….. Z równania krzywej wzorcowej obliczono stężenie kwasu salicylowego w analizowanej próbie. ....................................................................................................................................................... Stężenie kwasu salicylowego w próbie wynosi CSA = mg/100 cm3 Przeliczono stężenie kwasu salicylowego (CSA) w próbie na zawartość kwasu acetylosalicylowego (CASA) według następującego wzoru: c ASA CASA = cSA M ASA M SA MASA = 180,17 g; MSA = 138,2 g mg/100cm3 Absorpcjometria – protokół opracowała dr B. Szafran-Urbaniak 3 Zawartość kwasu acetylosalicylowego w tabletce wynosi Ryc. 1. Widmo elektronowe UV roztworów wzorcowych kwasu salicylowego oraz kwasu wyizolowanego z tabletki polopiryny WNIOSKI ………………………………………………………………………………………………… ………………………………………………………………………………………………… ………………………………………………………………………………………………… ………………………………………………………………………………………………… ………………………………………………………………………………………………… ………………………………………………………………………………………………… ………………………………………………………………………………………………… ………………………………………………………………………………………………… ………………………………………………………………………………………………… …………………………………………………………………………………………………... ....................................................................................................................................................... ....................................................................................................................................................... ....................................................................................................................................................... ĆWICZENIE ZALICZONO W DNIU: Absorpcjometria – protokół opracowała dr B. Szafran-Urbaniak 4