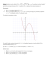pobierz - Konkurs Chemiczny im. prof. Antoniego Swinarskiego
Transkrypt
pobierz - Konkurs Chemiczny im. prof. Antoniego Swinarskiego
51 Ogólnopolski Konkurs Chemiczny im. prof. A. Swinarskiego I Etap 17.01.2015 r. ZADANIE A (20 pkt) 1. W którym zestawie cząsteczki są ułożone w kolejności ze wzrastającym kątem między wiązaniami: a) H2O, CH4, NH3 b) CH4, NH3, H2O c) H2O, NH3, CH4 d) NH3, CH4, H2O 2. Próbka białego ciała stałego jest jednym z następujących związków: NaHCO 3, AgNO3, Na2S lub CaBr2. 0,1 M roztwór jakiego związku można użyć do zidentyfikowania badanej próbki? a) NH3 (aq) b) HCl (aq) c) NaOH (aq) d) KCl (aq) 3. CaF2 ma iloczyn rozpuszczalności Ksp = 3,9·10–11 w 25°C. Jakie jest stężenie [F–] w nasyconym roztworze tej soli w temperaturze 25°C? a) 2,1·10-4 b) 3,4·10-4 c) 4,3·10-4 d) 6,8·10-4 4. Etanol reaguje z jonami Cr2O72– w środowisku kwaśnym zgodnie z równaniem: C2H5OH(c) + Cr2O72–(aq) + H+(aq) CO2(g) + Cr3+(aq) + H2O(c) Ile będzie wynosił współczynnik stechiometryczny przy H +(aq) po zbilansowaniu tego równania tak, aby uzyskać jak najmniejsze liczby całkowite? a) 10 b) 12 c) 14 d) 16 5. W którym z podanych związków grupa –OH ma najbardziej kwasowy charakter? a) b) c) CH3CH2CH2OH d) (CH3)3COH 6. W przemyśle chemicznym metanol, CH3OH, syntetyzuje się za pomocą reakcji tlenku węgla (II) z wodorem w obecności miedzi, tlenku cynku i glinu jako katalizatorów. Reakcja ta jest odwracalna: CO(g) + 2H2(g) CH3OH(g) ΔH = –91 kJ mol–1 W celu uzyskania jak największej wydajności reakcję należy prowadzić a) b) c) d) przy zmniejszonym ciśnieniu i w niskiej temperaturze przy zwiększonym ciśnieniu i w niskiej temperaturze przy zmniejszonym ciśnieniu i w wysokiej temperaturze przy zwiększonym ciśnieniu i w wysokiej temperaturze 7. Który z polimerów otrzymuj się przez reakcję polikondensacji? a) polipropylen b) poli(tereftalan etylenu) c) poli(chlorek winylu) d) polistyren 8. Magnetyt, Fe3O4, można zredukować do żelaza ogrzewając Fe3O4 z tlenkiem węgla (II): Fe3O4 + 4CO 3Fe + 4CO2 Jaka masa Fe3O4 jest potrzebna do otrzymania 5,0 kg żelaza, jeśli proces zachodzi z wydajnością 88%? a) 6.1 kg b) 6.9 kg c) 7.9 kg d) 18 kg 9. W reakcji opisanej równaniem 2A + B C przebiegającej zgodnie z równaniem kinetycznym 2 v = k·cA ·cB stężenia substratów zwiększyły się dwukrotnie. Szybkość tej reakcji a) zwiększy się 3-krotnie, b) zwiększy się 6-krotnie c) zwiększy się 8-krotnie, d) zmniejszy się 6-krotnie 10. Trzy metale, A, B i C, zanurzone w roztworach soli tych metali zostały przetestowane w ogniwach galwanicznych. Zaobserwowano, że dla A i B: A jest katodą, dla B i C: C jest katodą, dla A i C: A jest anodą. Jaka jest kolejność potencjałów elektrochemicznych kationów tych metali od najwyższego do najniższego? a) A > B > C b) B > C > A c) C> A > B d) B > A > C ZADANIE B (20 pkt) Analizowany związek chemiczny X jest białą substancją zwęglająca się podczas ogrzewania. Dane dotyczące tego związku uzyskane na drodze analizy klasycznej i instrumentalnej zestawiono poniżej. 1 2 3 4 5 6 7 8 Brak węgla asymetrycznego. Grupy funkcyjne położone obok siebie (grupy wicynalne). Analiza elementarna - 61,31% C; 5,11% H; 10,22% N. Nierozpuszczalny w wodzie. Rozpuszczalny w etanolu. Roztwarza się w roztworach wodorotlenku sodu i potasu, roztworze amoniaku oraz roztworach węglanów sodu i potasu. W trakcie ogrzewania z 30% roztworem NaOH wydziela gaz o ostrym przenikliwym zapachu, który zabarwia na zielono-niebiesko zwilżony uniwersalny papierek wskaźnikowy. W wyniku reakcji z wodą bromową otrzymuje się białą substancję A zawierającą 28,47% C; 1,69% H; 4,75% N i 54,24% Br. Roztwór alkoholowy substancji X z 10% roztworem FeCl3 daje fioletowe zabarwienie. Po ogrzaniu z rozcieńczonym kwasem solnym i ochłodzeniu wydziela się biała krystaliczna substancja B odbarwiająca rozcieńczony roztwór wodorotlenku sodu z dodatkiem fenoloftaleiny. Na zmiareczkowanie 0,276 g substancji B roztworem NaOH o stężeniu 0,100 mol/dm3 wobec fenoloftaleiny zużywa się 20,00 cm3 roztworu wodorotlenku. Na podstawie podanych wyżej informacji i po przeprowadzeniu stosownych obliczeń: 1. Podać wzór sumaryczny, wzór strukturalny i nazwę substancji X. 2. Określić przynależność tego związku do jednej z grup związków organicznych. 3. Wyjaśnić roztwarzanie się substancji X w podanych roztworach (tabela punkt 3) pisząc odpowiednie jonowe skrócone równania reakcji. 4. Zapisać równanie reakcji substancji X ze stężonym roztworem wodorotlenku sodu (tabela punkt 4). 5. Obliczyć wzór sumaryczny oraz podać wzór strukturalny i nazwę systematyczną substancji A oraz zapisać równanie reakcji tworzenia tej substancji ze związku X. 6. Podać jonowe skrócone równanie reakcji substancji X z chlorkiem żelaza(III). 7. Zapisać równanie reakcji otrzymywania substancji B oraz podać jej wzór strukturalny i nazwę. 8. Zapisać równanie reakcji substancji B z bezwodnikiem kwasu octowego, nazwać produkt i podać jego zastosowanie. ZADANIE C (15 pkt) Żyletki są produkowane ze stopu żelaza z chromem. Kawałek żyletki o masie 0,1331 g poddano reakcji z nadmiarem rozcieńczonego kwasu siarkowego (VI). Powstały roztwór o zielonkawym zabarwieniu, zawierający jony Fe2+, miareczkowano zakwaszonym roztworem nadmanganianu potasu o nieznanym stężeniu. W miareczkowaniu zużyto 20,08 cm3 roztworu KMnO4. Jony Cr3+, powstałe w reakcji z kwasem siarkowym nie reagują z KMnO4 w tych warunkach. 10 cm3 roztworu kwasu szczawiowego o stężeniu 0,0500 mol/dm3 zakwaszono kwasem siarkowym i roztwór ten miareczkowano tym samym roztworem KMnO4. Na zmiareczkowanie tej ilości kwasu szczawiowego zużyto 9,76 cm3 roztworu KMnO4. a) Napisz zbilansowane równania reakcji: i) pomiędzy żelazem z żyletki i kwasem siarkowym (VI) ii) miareczkowania roztworu Fe2+ nadmanganianem potasu iii) pomiędzy kwasem szczawiowym a nadmanganianem potasu. b) Oblicz stężenie roztworu KMnO4, użytego w obu miareczkowaniach. c) Oblicz zawartość procentową żelaza w żyletce. ZADANIE D (15 pkt) Podgrzany powyżej 100 ºC chlorek nitrozylu (NOCl) ulega częściowemu rozkładowi z wytworzeniem tlenku azotu (II) i gazowego chloru. Reakcja ta jest odwracalna. a) Napisz równanie reakcji rozkładu chlorku nitrozylu. b) 2,50 mola NOCl podgrzano w zamkniętym reaktorze. Po osiągnięciu równowagi mieszanina zawierała 0,80 mola tlenku azotu (II). Oblicz (w molach) ilość chloru i pozostałego NOCl. c) Inna mieszanina NOCl, NO i Cl2 osiągnęła stan równowagi w zamkniętym zbiorniku o pojemności 15,00 dm3 w pewnej temperaturze T. Mieszanina równowagowa zawierała 1,90 mola NOCl i 0,86 mola NO. W tej temperaturze stężeniowa stała równowagi tej reakcji, K c = 7,4 10-3 mol/dm3. Napisz wyrażenie na stałą równowagi tej reakcji, Kc. Oblicz liczbę moli Cl2 w mieszaninie w stanie równowagi. d) Jak wpłynie na wydajność procesu dwukrotne podwyższenie ciśnienia w układzie? ZADANIE E (15 pkt) Do grupy związków możliwych do otrzymania z kwasów karboksylowych (RCOOH) należą miedzy innymi: estry - RC(O)OR’, halogenki kwasowe – RC(O)X, amidy kwasowe – RC(O)NH2, RC(O)NHR’, RC(O)NR’R” oraz bezwodniki kwasowe RC(O)O(O)CR’, gdzie R, R’, R” to dowolna grupa węglowodorowa a X najczęściej Cl, Br lub I. Wszystkie z tych pochodnych ulegają, w odpowiednich warunkach, hydrolizie do wyjściowych kwasów karboksylowych. Pewien 1,2-podstawiony związek aromatyczny A wykorzystywany w farmacji, jak wykazała analiza elementarna, zawiera 61,31% węgla, 5,11% wodoru oraz 10,22% azotu. W odpowiednich warunkach ulega on hydrolizie do słabo rozpuszczalnej w wodzie substancji B, która w postaci rozcieńczonego roztworu wodno-etanolowego daje w reakcji z roztworem soli żelaza(III) fioletoworóżowy roztwór. Dodatkowo substancja B reaguje z roztworem wodorowęglanu sodu z wydzieleniem bezbarwnego, bezwonnego gazu. 1. Obliczyć wzór sumaryczny związku A. 2. Podać wzór strukturalny związku A wraz z krótkim uzasadnieniem. 3. Nazwać związek A. 4. Podać równanie hydrolizy związku A stosując wzory strukturalne. 5. Nazwać substancję B. 6. Podać równanie reakcji substancji B z wodorowęglanem sodu. 7. Podać przykład handlowego produktu zawierającego substancję B. 8. Na podstawie budowy związku B zaproponować dowolną reakcję, której może on ulegać i krótko to uzasadnić. 9. Podać równanie reakcji związku B z bezwodnikiem kwasu octowego i nazwać produkty.