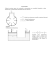a–22 wyznaczanie entalpii parowania wody
Transkrypt
a–22 wyznaczanie entalpii parowania wody
A–22 WYZNACZANIE ENTALPII PAROWANIA WODY Cel ćwiczenia: Celem ćwiczenia jest wyznaczanie entalpii parowania wody na podstawie zależności prężności pary nasyconej od temperatury wrzenia, korzystając z prawa Clausiusa-Clapeyrona. Zagadnienia: Entalpia. Przemiany fazowe ciecz – gaz w układzie jednoskładnikowym. Ciepło przemiany fazowej, entalpia parowania. Prężność pary cieczy. Równanie Clausiusa-Clapeyrona. Równanie Antoine’a. Reguła Troutona. Wpływ ciśnienia zewnętrznego na prężność pary nasyconej nad cieczą. Sprzęt: Odczynniki: elektroniczny miernik ciśnienia APAR tensometryczny woda destylowana czujnik ciśnienia, termometr 50-100 °C z podziałką 0,2 °C płaszcz grzejny, autotransformator, podciśnieniowa aparatura szklana, pompa próżniowa (ssak), pipety jednomiarowe 50 cm3, 10 cm3, 5 cm3 UWAGA: Celem prawidłowego wykonania ćwiczenia należy zapewnić szczelność każdego połączenia w podciśnieniowej aparaturze szklanej. Przy pierwszym pomiarze należy regulować ciśnienie przy pomocy pompy, tak by otrzymać wartość maksymalną ciśnienia. Pierwsze uruchomienie podciśnieniowego układu szklanego należy wykonać w asyście prowadzącego zajęcia. Wykonanie ćwiczenia: 1. Dokładnie zapoznać się z podciśnieniową aparaturą szklaną oraz wszystkimi połączeniami w niej występującymi. 2. Do kolby pomiarowej układu szklanego wlać 50 cm3 wody destylowanej. Termometr umieszczony w kolbie nie może być zanurzony w wodzie. M.Ch./E.Z. 1 3. Zamknąć kran łączący układ szklany z atmosferą, otworzyć kran łączący układ z pompą próżniową (ssakiem). Włączyć miernik ciśnienia. 4. Odpompować powietrze z układu szklanego, tak by osiągnąć najniższe ciśnienie wewnątrz układu. Zamknąć kran łączący układ z pompą próżniową i wyłączyć pompę. 5. Włączyć płaszcz grzejny kolby pomiarowej i obieg wody w chłodnicy. 6. Po osiągnięciu temperatury wrzenia w kolbie pomiarowej i ustabilizowaniu się wskazań termometru oraz manometru odczytać jednocześnie temperaturę i ciśnienie w układzie szklanym. 7. Delikatnie otworzyć kran łączący układ z atmosfera, wpuścić do układu nieco powietrza, tak by ciśnienie wewnątrz układu szklanego wzrosło o około 0,05 V. Wykonać pomiar temperatury wrzenia według p.5. 8. Wykonać ok. 20 - 30 pomiarów (wpuszczając powietrze do układu szklanego, tak aby ciśnienie wzrastało za każdym razem o około 0,05 V) pod coraz wyższym ciśnieniem, a ostatni pomiar wykonać pod ciśnieniem atmosferycznym (tj. kran łączący układ szklany z atmosferą otwarty). 9. Pomiary powtórzyć trzykrotnie. 10. Wartość ciśnienia atmosferycznego w danym dniu pomiarowym odczytać na barometrze. Opracowanie wyników: 1. Wyniki pomiarów przedstawić w tabeli zawierającej następujące dane: temperatura, ciśnienie, logarytm ciśnienia. 2. Wykonać wykres zależności ciśnienia zredukowanego od temperatury, p~ = f (T), oraz logarytm ciśnienia zredukowanego od odwrotności temperatury, ln p~ = f (1/T), gdzie ciśnienie zredukowane, p~ , opisane jest zależnością: p ~ p= p0 p - prężność pary nasyconej, p0 - ciśnienie standardowe (1013 hPa) 3. Wyznaczyć równanie prostej ln p~ = f (1/T) metodą najmniejszych kwadratów. 4. W oparciu o równanie Clausiusa-Clapeyrona – prostoliniową zależność ln p~ = f (1/T), obliczyć entalpię parowania wody. 4. Wyznaczyć błąd obliczonej entalpii parowania wody oraz przeprowadzić dyskusję błędów. M.Ch./E.Z. 2 Równanie kalibracyjne manometru elektronicznego APAR, czujnik 0,05 MPa, kanał pomiarowy 2: p = 1013 + U [mV] − 11,6 [hPa] 1.983 Literatura: 1. L.Sobczyk, A.Kisza, K.Gatner, A.Koll, „Eksperymentalna chemia fizyczna” PWN Warszawa 1992. 2. L.Komorowski, A.Olszowski, Chemia Fizyczna, tom 4, Laboratorium Fizykochemiczne, PWN Warszawa 2013. 3. J.Bryłka, „Ćwiczenia laboratoryjne z chemii fizycznej”, Skrypt Wyższej Szkoły Inżynieryjnej w Radomiu, Radom 1983. 4. E.Dutkiewicz, „Ćwiczenia laboratoryjne z chemii fizycznej”, Wydawnictwo Naukowe UAM, Poznań 1997. M.Ch./E.Z. 3