Białka cytoszkieletu i motory molekularne
Transkrypt
Białka cytoszkieletu i motory molekularne
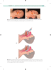
Część II · OD GENETYKI MOLEKULARNEJ DO BIOCHEMII CZŁOWIEKA · Aktyna jest białkiem mikrofilamentarnym wykazującym aktywność ATPazową Ryc. 10.3. Wrodzona erytrodermia z rybią łuską spowodowana mutacją keratyny. (Dzięki uprzejmości Wellcome Medical Photographic Library, nr N0004663C). Podwyższoną ekspresję K6 i K16 obserwuje się w uszkodzeniach skóry z hiperprloliferacją, jak np. pęcherzyca albo łuszczyca. Ekspresja tych keratyn ułatwia migrację keratynocytów w obrębie zranienia. Filamenty pośrednie odrywają także pewną rolę w niektórych chorobach nowotworowych. Komórki Reed-Sternberga (cytologiczny marker chłoniaka Hodgkina) dokonują nadekspresji restyny, podczas gdy rozwój raka jelita grubego jest związany z mutacją MCC (mutated in colorectal carcinoma). Niektóre przypadki stwardnienia zanikowego bocznego (amyotrophic lateral sclerosis) mogą być spowodowane mutacjami dotyczącymi neurofilamentów. Mikrofilamenty aktynowe są najlepiej znane jako tworzywo cienkich miofilamentów. W rzeczywistości białko to występuje powszechnie. Spolimeryzowane makromolekuły aktynowe tworzą około 10-20% białek. Większość ważnych molekuł odpowiedzialnych za kształtowanie architektury komórek jest wiązana przez aktynę, co sprawia, że ta ostatnia jest niezwykle ważna w kontekście determinacji morfologii komórkowej (ryc. 10.4). Produkt genu beta aktyny ze względu na jego wszechobecną ekspresję traktowany jest jako tzw. gen odnośnikowy w trakcie wykonywania eksperymentów genetycznych. Tak jak tubulina jest główną białkową składową rzęski, aktyna stanowi kluczowy element budulcowy kosmków jelitowych. Niemniej jednak obydwa typy białek różnią się znacznie pod wieloma względami. Po pierwsze – stabilizacja filamentów aktynowych jest zależna raczej od ATP, a nie GTP. Po drugie – mikrofilamenty istnieją jako gmatwanina krzyżowo powiązanych białek, a nie dyskretna struktura tubularna. Polimeryzacja aktyny odbywa się w dwóch etapach: pierwszy to nukleacja (etap limitujący szybkość procesu polimeryzacji), kolejny to elongacja – ten etap prowadzi do zaangażowania w polimeryzację rozmaitych izoform aktyny. Ryc. 10.4. Koordynacja zdarzeń wewnątrzkomórkowych prowadzona przez białka cytoszkieletu. 250 Rozdział 10 · BIAŁKA CYTOSZKIELETU I MOTORY MOLEKULARNE · 1. Nukleacja rozpoczyna się jako zależna od wysokiego stężenia soli zmiana konfiguracji (konformacji) globularnej (monomerycznej) formy G-aktyny. Ta odmiana aktyny to około 50% aktyny komórkowej. 2. W drugim etapie aktyna G jest konwertowana do spolimeryzowanej formy aktyny. Istnieje przynajmniej 6 izoform aktyny kodowanych przez odrębne geny. Polimery mikrofilamentów aktyny F są stabilizowane przez jony wapnia i ADP, podczas gdy forma niespolimeryzowana jest stabilizowana przez jony magnezu i ATP. Stopień konwersji zależny jest od aktywności ATPazowej molekuł aktynowych, występujących wokół i w obrębie określonego mikrofilamentu. W związku z tym, że aktyna połączona z ATP wykazuje wyższe powinowactwo do zakończeń filamentów, elongacja polimerów aktyny jest ATP-zależna (ryc. 10.5). W niektórych systemach eksperymentalnych deformacja komórkowa jest związana z defosforylacją tyrozyn występujących w obrębie aktyn. Zachowania aktyny są regulowane przez białka wiążące aktynę. Monomeryczne formy G aktyny są wiązane poprzez małe białko o masie cząsteczkowej około 15 kDa, nazywane profiliną. Profilina stabilizuje aktynę w formie monomerycznej. Spolimeryzowane filamenty aktynowe ulegają rozdziałowi pod wpływem żelzoliny. Inne białko wiążące się z aktyną to wilina, która uczestniczy zarówno w katalizowaniu polimeryzacji F-aktyny, jak i rozrywaniu polimerów aktyny, przyczyniając się w ten sposób do utrzymania dynamicznej architektury mikrokosmków w komórkach jelit. W niemięśniowych typach komórek aktyna jest rozdzielona pod wpływem żelzoliny i wiliny, i wpływa na relaksacyjną zmianę kształtu komórki, umożliwiając w ten sposób fagocytozę i mobilność komórki. Wpływ żelzoliny wynika przede wszystkim z możliwości tzw. czapeczkowania (capping) – wiązania tego białka do tzw. rosnącego końca filemantu aktynowego, czemu towarzyszy terminacja polimeryzacji. Tymozyna beta 4 to inne biało wiążące aktynę. Tymozyna porządkuje komórkowe za- Ryc. 10.5. Transformowanie aktyny w wyniku fosforyla- cji i polimeryzacji. Katalizowana przez ATPazę hydroliza ATP inicjuje polimeryzację monomerycznej formy aktyny (aktyny F). soby monomerów aktynowych w sposób precyzyjny, zapobiegając spontanicznej polimeryzacji aktyny. ASPEKTY KLINICZNE Aktyna w chorobach człowieka Aktyna jest produktem tzw. genu metabolizmu podstawowego (housekeeping gene) a jej udział zaobserwowano w kilku chorobach człowieka. 1. W wyniku masywnych uszkodzeń tkanek dochodzi do uwolnienia dużych ilości aktyny F i aktyny G do krążenia, co prowadzi do indukowanych mikrofilamentami zatorów naczyniowych. Zatory te mogą prowadzić nawet do stanów zagrożenia życia w przypadku szoku septycznego, malarii, piorunującej martwicy wątroby. 2. Powstanie krążących autoprzeciwciał w przypadku przewlekłego zapalenia wątroby (przeciwciała przeciwko mięśniom gładkim) lub zespołu pourazowego serca (przeciwciała przeciwko komórkom mięśnia sercowego) może być związane z uwolnieniem do krążenia dużych ilości aktyny występującym po uszkodzeniu tkanek. 3. Nieprawidłowe rozrywanie filamentów aktynowych w związku z mutacją punktową żelzoliny występuje w przypadku rodzinnej amyloidozy typu fińskiego. 4. Zdolność żelzoliny do rozrywania filamentów aktynowych może mieć znaczenie terapeutyczne w mukowiscydozie, gdzie wysoki poziom filamentów aktynowych wydzielanych w trakcie trawienia powoduje niewydolność trzustki. Zależny od aktyny ruch komórkowy jest zazwyczaj osiągnięty w wyniku formowania kolca (spike, równoległe filamenty, filopodia) albo kartki (ortogonalne filamenty: lamelliopodia). Wydłużanie lameliopodiów jest przyśpieszane za pośrednictwem tymozyny beta 4 (patrz powyżej), przez co dochodzi do ułatwienia migracji komórkowej. W odniesieniu do tego aspektu, nadekspresja tymozyny beta 4 jest związana z metastazą komórek nowotworowych. W przypadku bakterii Yersinia pestis – czynnika zakaźnego dżumy, zdolność do kolonizowania narządów układu odpornościowego jest osiągana w wyniku wyrzutu zewnątrzkomórkowych białek Yop bakterii Yersinia, w tym białka YopE, będącego cytotoskyną depolimeryzującą mikrofilamenty aktynowe. Białko YopE ulega nadekspresji w wyniku kontaktu bakterii z komórkami gospodarza (ryc. 10.6). Wrodzone zaburzenia w rozwoju układu nerwowego określone mianem zespołu Williamsa powstają wielokrotnie w konsekwencji niedoboru enzymu powodującego fosforylację kofiliny (patrz poniżej). 251 Część II · OD GENETYKI MOLEKULARNEJ DO BIOCHEMII CZŁOWIEKA · Ryc. 10.7. W zespole Wiskotta-Aldricha obserwuje się Ryc. 10.6. Uszkodzenie cytoszkieletu aktynowego wywo- łane przez zewnątrzkomórkowe białka Yop bakterii dżumy. Białko to jest wprowadzane do komórek gospodarza za pomocą białka transmembranowego Ysc. ASPEKTY MOLEKULARNE WASP Autosomalny recesywny zespół Wiskotta-Aldricha (WAS; ryc. 10.7) jest spowodowany poprzez mutacje utraty funkcji (loss of function) dotyczące białka WASP, które ulega selektywnej ekspresji w komórkach linii hematopoetycznych. WASP jest białkiem wiążącym aktynę i indukującym tworzenie ognisk adhezyjnych w makrofagach, limfocytach i płytkach krwi. W przypadku komórek wykazujących zdolności chemotaktyczne to działanie białka WASP związane jest ze stymulacją kompleksu aktyno-pokrewnego białka Arp2/3. Komórki zdolne do ekspresji białka WASP syntetyzują podosomosomy w odpowiedzi na bakteryjne chemoatraktanty. Te struktury adhezyjne nie występują u pacjentów z WAS, powodując defekty w chemotaksji, a co za tym idzie – uogólniony niedobór immunologiczny. W komórkach neuronalnych kombinacja PIP2 (fosfatydyloinozytolobisfosforan) i małego białka G Cdc42 indukuje formowanie wypustek w konsekwencji wiązania do N-WASP, czyli białka wiążącego profilinę i będącego homologiem białka WASP, występującego głównie w komórkach układu nerwowego. Po związaniu do Cdc42, N-WASP indukuje depolimeryzację – odkrywając wolne, rosnące końce mikrofilamentu, co w końcowym efekcie umożliwia utworzenie długich aktynowych mikrokolców (microspikes). Inna fosfoproteina, kofilina, mediuje błonowe marszczenie (rufflling) i lamoliopodialne efekty małego białka G Rac. Zmiany te umożliwiają wytworzenie kompleksu ze spokrewnionym z WASP białkiem WAVE. [Ruffling umożliwia tworzenie 252 częste infekcje spowodowane defektami adhezji i chemotaksji komórek układu odpornościowego. (Dzięki uprzejmości wellcome Medical Photographic Library, nr N0005090C). zmarszczek (ruffles) kompartmentów błony komórkowej, umożliwiających tworzenie kompleksów białek adhezyjnych w obrębie lameliopodiów – przyp. red.]. ASPEKTY KLINICZNE VASP i listerioza Zjadliwość wewnątrzkomórkowej bakterii Listeria monocytogenes jest zależna od jej zdolności do inwazji tkanek. Listeria porusza się wewnątrz komórek, osiągając prędkość około 5 mikrometrów (jest to połowa średnicy komórki bakteryjnej) na minutę. Ruch bakterii odbywa się dzięki aktynowemu „ogonowi rakietowemu” (rocket tail) napędzanemu przez białka gospodarza. W momencie kiedy bakteria dociera do błony komórkowej, formowane są filopodia. W jaki sposób Listeria podporządkowuje sobie maszynerię gospodarza? Białko wiążące aktynę, profilina, ulega koncentracji w tych częściach komórki, gdzie filamenty aktynowe ulegają rekrutacji do bogatego w prolinę białka wiążącego profilinę VASP (vasodilator-stimulated phosphoprotein). Kluczowe dla zjadliwości bekterii Listeria jest białko ActA, wiążące VASP i ulegające ekspresji na tych częściach powierzchni bakteryjnej, gdzie formułowany jest aktynowy ogon. Poprzez wiązanie do VASP profilina ulega rekrutacji do tej części ściany bakterii, które zawiera ActA. To z kolei umożliwia rozpoczęcie formowania siedliska dla aktynowego ogona. Odpowiednie domeny białka ActA są homologiczne do WASP, a inne do białek cytoszkieletu zyksyny i winkuliny. To tłumaczy wiązanie ActA do kompleksu sygnalizacyjnego Arp2/3 (który włącza demontaż aktynowego filamentu) i VASP (ryc. 10.8).