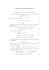ADSORPCJA
Transkrypt
ADSORPCJA
ADSORPCJA Adsorpcja — proces zmiany stężenia substancji na granicy pomiędzy dwiema fazami - gazową i ciekłą (gaz-roztwór), ciekłą i stałą (roztwór-ciało stałe) oraz pomiędzy nie mieszającymi się cieczami (ciecz-ciecz). Stężenie substancji w obszarze międzyfazowym (na granicy faz i/lub w jej pobliżu jest inne niż w głębi fazy). Adsorpcja ma charakter powierzchniowy, czym różni się od absorpcji polegającej na pochłanianiu w całej objętości (mechanizm podziałowy - opisywany prawem Nernsta). Często procesy adsorpcji oraz absorpcji występują równocześnie i mówimy wtedy o sorpcji. Termin sorpcja stosujemy również wtedy gdy nie możemy sprecyzować mechanizmu zjawiska. Granica faz gaz-ciało stałe z adsorbat ρ(z) faza zaadsorbowana adsorbent Energia potencjalna chemisorpcja fizysorpcja odległość z Energia potencjalna Fizysorpcja → Chemisorpcja Fizysorpcja może poprzedzać chemisorpcję. odległość z Adsorpcja może być czuła na - początkową orientację cząsteczki - zmiany w wiązaniach wewnątrzcząsteczkowych - punkt zbliżenia (miejsce adsorpcyjne) Adsorpcja fizyczna (Fizysorpcja) Adsorpcja chemiczna (Chemisorpcja) - brak bariery energetycznej (nie wymaga aktywacji) - może występować bariera energetyczna - wymaga aktywacji - proces szybki - różnorodna kinetyka procesu - oddziaływania vdW słabe (<0.4 eV ≈ 10 kcal/mol ) - powstawanie wiązań jonowych/ metalicznych/kowalencyjnych silnych (>0.4 eV) - zawsze atomowa lub cząsteczkowa - może być dysocjatywna - proces odwracalny - często nieodwracalna - może powstawać wielowarstwa - ograniczona do monowarstwy Physical Adsorption (Physiorption) Chemical Adsorption (Chemisorption) - no barrier (not activated) - may have barrier - fast - variable uptake kinetics - vdW/dipole interactions - covalent/metallic/ionic - weak (<0.4 eV) - strong (>0.4 eV) - always atomic/molecular - may be dissociative - reversible - often irreversible - surface symmetry insensitive - surface symmetry specific - may form multilayers - limited to monolayer - surface T < condensation T - wide range surface T Adsorpcja zlokalizowana i mobilna energia translacje x,y,z 3 kT 2 q gaz = qtr . x qtr . y qtr . z qwew. V – bariera dla dyfuzji q ads. = e − ε a / kT q tr .x q tr . y q osc.z q wew . V MOBILNA kT~ V oscylacje x,y,z energia ZLOKALIZOWANA kT<< V translacje x,y,z 3 kT 2 translacje x,y q ads. = e − ε a / kT q osc.x q osc. y q osc.z q wew . V oscylacje z MODEL LANGMUIRA - Zespół kanoniczny, N,T,V, B - const. •Równocenne energetycznie centra adsorpcyjne •Adsorpcja zlokalizowana, monowarstwowa – co najwyżej jedna molekuła na jednym centrum adsorpcyjnym. •Brak oddziaływań w fazie gazowej i zaadsorbowanej. V,T N-M - liczba molekuł w fazie gazowej M –liczba molekuł zaadsorbowanych B – liczba miejsc adsorpcyjnych Ec = Eads. + E gaz - brak oddziaływań międzycząsteczkowych Z c = Z ads. Z gaz Z ads. B! M = qads. M !( B − M )! Z gaz = W stanie równowagi dF=0 (F w minimum) lub dlnZc=0 (Zc-maksymalne) q N −M gaz ( N − M )! F=-kTlnZc lnZc = BlnB − B + M lnqads. − M lnM + M − (B − M)ln(B − M) + (B − M) (N − M) lnqgaz − (N − M)ln(N − M) + (N − M) d ln Z c = ln qads. − ln M + 1 + ln( B − M ) − 1 dM − ln q gaz + ln ( N − M ) + 1 − 1 = 0 B − M qads. ln (N − M ) = 0 M q gaz Z równania stanu gazu doskonałego: pV (N − M ) = kT q gaz = q V ' gaz =1 Ostatecznie mamy: q ads. θ M = = K L ( T ) p K L (T ) = ' q gaz kT B − M 1− θ localized Izoterma Langmuira lub K Lp θ= 1 + K Lp po raz pierwszy wprowadzona w 1916 r. przez Irvinga Langmuira, laureata Nagrody Nobla w 1932 r. Klasyfikacja izoterm wg Brunauera Liniowa postać izotermy Langmuira a θ= am am - pojemność monowarstwy mol/g lub mol/m2 p 1 p = + a am K L am a p p a tg α = a = K La m − K La p 1 am K La m 1 a mK L p tg α = − K L a IZOTERMA LANGMUIRA - Wielki zespół kanoniczny T,µ,B układ otwarty M =B Ξ ads. (T , µ , B ) = ∑ λM Z ads. ( B, M , T ) M =0 B M Ξ ads. (T , µ , B) = ∑ λ qads. M =0 M M =B B! M B−M ( ) ( ) λqads. 1 = ∑ M = 0 M !( B − M )! M =B = (1 + λqads. ) B M ln Ξ ads. ( B, µ , T ) = B ln(1 + λqads. ) Obliczamy średnią liczbę cząsteczek w układzie (zaadsorbowanych): Bλqads. ∂ ln Ξ ads. M = λ = ∂λ T , µ 1 + λqads. W stanie równowagi: µ gaz µ gaz = µ ads. λ gaz = λads. q gaz N p = −kT ln = kT ln ' = kT ln ' N q gaz (T )V q gaz (T )kT p λ= ' q gaz (T )kT M K Lp =θ= B 1 + K Lp q ads. K L (T ) = ' q gaz kT ADSORPCJA MOBILNA •Cząsteczki poruszają się swobodnie po powierzchni w polu potencjału powierzchniowego - dwuwymiarowy gaz doskonały. •Adsorpcja mobilna, monowarstwowa. •Brak oddziaływań w fazie gazowej i zaadsorbowanej. A q ads. = e − ε a / kT q tr .x q tr . y q osc.z q wew . tr. = post. M M q ( λ q ) ads. Ξ ads. (A, T, µ) = ∑ λM ads. = ∑ = e λq ads . M =0 M! M =0 M! ∂ ln Ξ ads. M=λ = λq ads ∂λ ' ads. M q θ= = ' p = KMp A q gaz kT mobile Izoterma Henry’ego p λ= ' q gaz (T )kT q ads. = q ' ads . A ADSORPCJA WIELOWARSTWOWA - MODEL BET W modelu zakłada się, że cząsteczki adsorbatu adsorbują się na powierzchni adsorbentu w sposób zlokalizowany (tzn. cząsteczki nie mogą się przemieszczać po powierzchni) dzięki oddziaływaniom adsorbat-adsorbent, na zaadsorbowanych cząsteczkach dzięki oddziaływaniom adsorbatadsorbat (określonym poprzez wielkość ciepła skraplania adsorbatu) mogą się "pionowo" adsorbować kolejne cząsteczki adsorbatu itd., nie występują oddziaływania poziome między zaadsorbowanymi cząsteczkami, faza gazowa jest doskonała. B - liczba miejsc adsorpcyjnych, M - liczba molekuł w jednym słupku Zakładając, że ilość warstw adsorpcyjnych nie jest niczym ograniczona, otrzymujemy 2-parametrowe klasyczne równanie BET. Ξ ads. = (Ξ słup. ) B Ξ słup. = 1 + λq a + λ2 q a q l + λ3q a q l2 + ..... = 1 k 1 + λq a ∑ (λq l ) = 1 + λq a 1 − λq l k =0 szereg geometryczny Ξ słup. 1 − λq l + λq a = 1 − λq l p λ= ' q gaz (T )kT ∂ ln Ξ słup. ∂ ln Ξ ads. M=λ = Bλ ∂λ ∂λ Bλq a M= (1 − λq l )(1 − λq l + λq a ) p C ps M = B p p 1 − 1 + (C − 1) ps p s p λ= ' q gaz (T )kT p λq l = ps qa C= ql Model 2-parametrowy. Parametry modelu: B,C ps - prężność pary nasyconej Zamiast parametru B wprowadza się parametr am (mol/g) nazywany pojemnością monowarstwy. Adsorpcję oznacza się wtedy symbolem a i wyraża się w molach na gram adsorbentu. Tak sformułowany model z reguły przewiduje adsorpcję wyższą niż obserwowana doświadczalnie. Równanie BET jest powszechnie stosowane do wyznaczania pola powierzchni właściwej adsorbentów w oparciu o niskotemperaturową adsorpcję azotu (77-78 K temperatura ciekłego azotu). x 1 (C − 1) = + x a (1 − x ) a m C a m C x a (1 − x ) tg α = S = a m ωN 2 ωN 2 = 16,2 A2 (C − 1) a mC 1 a mC x= p ps Otrzymaną pojemność monowarstwy przelicza się na powierzchnię właściwą adsorbentu przy wykorzystaniu tzw. powierzchni siadania cząsteczki azotu (σ = 0.162 nm2=16.2 A2). Tak określoną powierzchnię właściwą często nazywa się też skrótowo powierzchnią BET adsorbentu. W przypadku założenia ograniczonej liczby warstw otrzymujemy równanie 3-parametrowe: am,C, n (ograniczenie grubości warstwy adsorpcyjnej do n-warstw, może wynikać z wielkości porów lub rozmiaru przestrzeni międzyziarnowych). [ a 1 Cx 1 − (n + 1) x n + nx n +1 θ= = a m 1 − x 1 + (C − 1) x − Cx n +1 ] ADSORPCJA NA POWIERZCHNIACH HETEROGENICZNYCH energia Powierzchnie heterogeniczne charakteryzują się centrami adsorpcyjnymi o różnej energii adsorpcji. Rozkład przypadkowy (random distribution) Rozkład płatowy (patchwise distribution) Równanie izotermy adsorpcji na powierzchni heterogenicznej - gdy na powierzchni występuje kilka rodzajów centrów adsorpcyjnych o energiach adsorpcji εi, i=1,2,3...... θ t = ∑ α iθ i i - gdy zbiór różnych wartości energii jest bardzo duży (rozkład ciągły χ(ε)) θ t ( p) = ∫ θ l ( p, ε )χ (ε )dε Ω local - lokalna total - całkowita ( ) χ ε d ε = 1 ∫ Ω Ω -energy domain przedział zmienności energii adsorpcji (εmin, εmax), (0,∞) normalization condition warunek unormowania energy distribution function –funkcja rozkładu energii adsorpcji Z równania całkowego możemy wyznaczyć: •izotermę globalną gdy znana jest izoterma lokalna i funkcja rozkładu energii adsorpcji, θ t ( p) = ∫ θ l ( p, ε )χ (ε )dε szukane Ω znane znane •funkcję rozkładu energii adsorpcji dla założonego modelu adsorpcji lokalnej gdy znana jest izoterma globalna. θ t ( p) = ∫ θ l ( p, ε )χ (ε )dε znane Ω znane szukane funkcja rozkładu energii adsorpcji χ(ε) 1 ε max − ε min rozkład prostokątny εmin εmax ε ' K L = exp K L kT 1 dla ε min < ε < ε max χ (ε ) = ε max − ε min 0 dla ε < ε min lub ε > ε max izoterma lokalna ε ' exp K L p kT θ L (ε , p ) = ε ' 1 + exp K L p kT ε max Całkujemy: ∫ε θ L (ε , p ) χ (ε )dε = min ε max 1 − ε min ε max ' ε ' K L p K L p ε max exp 1 + exp kT kT kT d ln = ε ∫ε ε max − ε min ε ' ε min ' min 1 + exp K p 1 exp + L K L p kT kT Przybliżenie kondensacyjne: polega na zastąpieniu izotermy lokalnej izotermą kondensacyjną, zdefiniowaną następująco: 0 θ c (ε , p) = 1 gdy gdy ε < ε c ( p) ε ≥ ε c ( p) χ ∞ θχ ∫ε χ (ε )dε c 0 θ c (ε , p) = 1 gdy p < p c (ε ) gdy p ≥ p c (ε ) równanie całkowe przyjmuje wtedy postać: ∞ ∞ 0 εc θ t ( p ) = ∫ θ c (ε , p )χ (ε )dε = ∫ χ (ε )dε εc ∞ ∫ θχdε 0 ε Wyznaczanie εc . 1 θ (ε , p c ) = 2 kryterium Cerofoliniego Wyznaczanie kondensacyjnej funkcji rozkładu energii adsorpcji: ∂θ t ( p ) ∂p χ c (ε ) = − ∂p ∂ε p = pc Wyznaczanie kondensacyjnej izotermy całkowitej(globalnej): θ t ( p ) = − Χ c (ε c ) Χ c = ∫ χ (ε )dε Przykład 1: Wyznaczanie funkcji rozkładu energii adsorpcji gdy znana jest izoterma: lokalna całkowita ε ' exp K L p kT θ L (ε , p ) = ε 1 + exp K L' p kT θt = KF p 1/ n Freundlich Langmuir 1 0 < <1 n 1) wyznaczanie energii kondensacji εc ' exp K L p 1 kT = θ c (ε c , p) = 2 εc ' 1 + exp K L p kT ε c ( p ) = −kT ln K L' − kT ln p p c (ε ) = 1 ε K L' exp kT 2) wyznaczanie funkcji rozkładu energii adsorpcji ∂θ t ( p ) ∂p χ c (ε ) = − ∂p ∂ε χ c (ε ) = KF ( ) nkT K ' 1/ n L θt = KF p K F 1 / n −1 p = − p − n kT p = pc ε exp − nkT χ c (ε ) ε 1/ n Przykład 2: Obliczanie całkowitej izotermy adsorpcji gdy: izotermą lokalną jest równanie Langmuira p c (ε ) = 1 ε K exp kT ' L funkcja rozkładu energii adsorpcji ma postać χ (ε ) = χ (ε ) 1 ε − ε0 exp c c ε − ε0 1 + exp c 2 ε 1 ε − ε0 exp c 1 c dε = − Χ c (ε ) = ∫ χ (ε )dε = ∫ 2 ε − ε0 ε − ε 0 1 + exp 1 + exp c c θ t ( p ) = − Χ c (ε c ) = 1 − kT ln K L' − kT ln p − ε 0 1 + exp c kT c parametr heterogeniczności ' ε0 K L exp p kT / c kT kT ( Kp ) 0< <1 = θ t ( p) = c kT kT / c 1 + (Kp ) c ' ε0 1 + K L exp p kT izoterma Langmuira-Freundlicha LF izoterma Bradley’a-Sipsa TERMODYNAMIKA ADSORPCJI f. zaadsorbowana adsorbent układ autonomiczny (można zaniedbać efekty oddziaływania z fazą gazową) dU = TdS − pdV + µ a dn a + µ s dn s dla całego układu dU 0,a = TdS 0,a − pdV 0,a + µ 0,a dn a dla samego adsorbentu Gdy założymy, że adsorbent jest inertny, to różnicę tych energii można uważać za energię wewnętrzną ns moli fazy zaadsorbowanej: dU − dU 0,a = T (dS − dS 0,a ) − p (dV − dV 0,a ) + ( µ a − µ 0,a )dn a + µ s dn s Wprowadzając oznaczenia: dS = dS − dS s 0, a dV = dV − dV s 0, a dU s = TdS s − pdV s + µ s dn s − ϕdn a − ϕ = µ a − µ 0,a Z równania na dUs wynika, że ∂U s ϕ = − a ∂n S s ,V s ,n s reprezentuje zmianę energii przy przyroście ilości adsorbentu o jednostkę, a więc także przyroście pola powierzchni adsorbentu. Zakładając, że pole powierzchni i liczba miejsc adsorpcyjnych są proporcjonalne do na ϕdn = π dAs = π dB a dn = C dAs = C dB a A B A ciśnienie rozprężania (spreading pressure) G s = U s + pV s − TS s dG = − S dT + V dp − πdAs + µ dn s Gdy s T = const. s i B s s p = const. to całkując powyższe równanie otrzymamy G = −πAs + µ n s s s Różniczkując to ostatnie równanie dG s = −πdA s − As dπ + µ s dn s + n s dµ s i porównując różniczki dGs dostaniemy n dµ = − S dT + V dp + As dπ s s s s 1 dµ = − s dT + v dp + dπ Γ s s s :n s Γ = n s / As średnie wielkości molowe dµ g = − s g dT + v g dp W stanie równowagi dµ s = dµ g Dla T=const. i vg>>vs otrzymamy 1 dπ = ( s s − s g )dT + (v g − v s )dp = v g dp Γ (mol / m 2 ) Z równania stanu gazu doskonałego RT v = p g dπ = RTΓd ln p p Aby wyznaczyć π należy dokładnie zmierzyć izotermę Γ(p) poczynając od bardzo niskich ciśnień. π = RT ∫ Γd ln p 0 W stanie równowagi (s s −s g ( h )= s ( − hg T ) ) s g 1 h − h − v g dp + dπ = ( s s − s g )dT = dT Γ T ( s g ∂ ln p h − h =− 2 ∂ T RT π ) Aby z tego równania obliczyć zmianę entalpii (efekt cieplny) należy wyznaczyć zależność π(p). Izosteryczne ciepło adsorpcji (efekt cieplny przy stałym pokryciu) µ s ( p, T , Γ) ∂µ s dµ = ∂T s ∂µ s ∂T ∂µ s ∂µ s dT + dp + p ,Γ ∂p T ,Γ ∂Γ ∂ ∂G s = s p ,Γ ∂T ∂n ∂ = s p ,T ∂n ∂G s ∂T dΓ p ,T ∂S s = − s p ,Γ ∂n = − s s T , p różniczkowa molowa entropia ∂µ s ∂p ∂ ∂G s = s T ,Γ ∂p ∂n ∂ = s T , p ∂n ∂G s ∂p ∂V s = s T ,Γ ∂n = v s T , p różniczkowa molowa objętość dµ = − s dT + v dp s s s Γ = const. dµ = − s dT + v dp g g g Zakładając, że gaz jest doskonały i porównując potencjały otrzymamy ( ) q st h s − hg ∂ ln p = =− 2 RT RT 2 ∂T Γ bo w stanie równowagi adsorpcyjnej (s s − sg ) = (h s − hg T ) WYZNACZANIE qst Aby wyznaczyć qst trzeba znać zależność p(T) przy stałym Γ. lnp ∂ ln p q st = − R ∂ (1 / T ) Γ 1/T Γ T1<T2<T3 p1<p2<p3 Γ=const. p MODEL LANGMUIRA – powierzchnia homogeniczna θ ε ' ln p = − − ln K L + ln 1−θ RT ' K ∂ ln ∂ p ln 2 L q st = RT 2 = ε − RT ∂T θ ∂T ciepło adsorpcji niezależne od pokrycia MODEL LANGMUIRA - FREUNDLICHA – powierzchnia heterogeniczna RT c ε0 θt ' ln K L + RT + ln p = 1 − θ t θt ε0 c ln p = ln − − ln K L' RT 1 − θ t RT ' ∂ ln K ∂ ln p 2 L q st = RT 2 = ε − RT ∂T θ ∂T θ − c ln t 1−θt ciepło adsorpcji zależne od pokrycia MODEL FOWLERA-GUGGENHEIMA (BRAGGA WILLIAMSA) Energia oddziaływań bocznych w przybliżeniu Bragga-Williamsa jest dla każdej konfiguracji (rozmieszczenia molekuł między centra adsorpcyjne) taka sama i wynosi ε ωθ K L' exp exp p RT RT θ FG (ε , p, ω ) = ε ωθ 1 + K L' exp exp p RT RT 2 U oddz . M zu = 2B ω = − zu ω >0 ω <0 izoterma FG przyciąganie odpychanie ε ln p = − ln K L' − RT ωθ − RT θ + ln 1−θ ' ∂ K ln ∂ p ln 2 L q st = RT 2 RT = ε + ωθ − ∂T θ ∂T ciepło adsorpcji zależne od pokrycia PODSUMOWANIE qst q st = ωθ ω>0 ∂ ln K L' q st = ε − RT ∂T 2 1 q st = ωθ ω<0 θ θt q st = −c ln 1−θt