Lasery w endodoncji - Dental Tribune International
Transkrypt
Lasery w endodoncji - Dental Tribune International
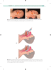
Praktyka _ Standardy postępowania Lasery w endodoncji Lasers in endodontics Autorzy_Enrico DiVito, Rolando Crippa, Giuseppe Iaria, Vasilios Kaitsas, Stefano Benedicenti i Giovanni Olivi Streszczenie: W niniejszym artykule przeanalizowano grupę najważniejszych badań oraz nowe wytyczne dla zastosowania lasera jako aktywatora substancji płuczących. Summary: This article will analyze some of the most important research in the international literature today and the new guidelines for the use of the laser as a source of activation of chemical irrigants. Słowa kluczowe: lasery, nowe wytyczne, aktywator substancji płuczących. Key words: lasers, new guidelines, source of activation of chemical irrigants. Ryc. 1 _Endodoncja wspomagana laserowo _Przygotowanie otworu dostępu Przygotowanie otworu dostępu może być przeprowadzone bezpośrednio z laserami Erbium, dzięki którym można usunąć szkliwo i zębinę. W tym przypadku zaleca się użycie krótkiej końcówki (4-6 mm), o średnicy 600-800 µm, wykonanej z kwarcu, aby można było wykorzystać większą energię i moc. Nie należy zapominać o znaczeniu tej techniki. Ze względu na szczególne dostosowanie do tkanek bogatych w wodę (miazga i tkanka próchniczna), laser umożliwia minimalnie 14 laser 2_2014 inwazyjny dostęp (ponieważ jest wybiórczy) do komory miazgi zęba i jednocześnie pozwala na odkażenie i usunięcie pozostałości bakterii i miazgi. Dostęp do otworów kanałowych można skutecznie uzyskać po uprzednim zmniejszeniu liczby bakterii, zapobiegając tym samym przemieszczaniu się bakterii, toksyn i resztek w kierunku wierzchołka podczas zabiegu. Chen et al. wykazali, że podczas przygotowania otworu bakterie niszczone są do głębokości 300-400 µm poniżej naświetlanej powierzchni. Co więcej, lasery Erbium są użyteczne w usuwaniu kamieni miazgi oraz w poszukiwaniu zwapnionych kanałów. Praktyka _ Standardy postępowania Ryc. 2 _Przygotowanie i kształtowanie kanałów Przygotowanie kanałów przy pomocy narzędzi NiTi wciąż jest kluczowym standardem w dzisiejszej endodoncji. Pomimo stwierdzonego działania ablacyjnego laserów Erbium (2,780 i 2,940 nm) na twardych tkankach, ich skuteczność w przygotowaniu kanałów w korzeniu wydaje się być obecnie ograniczona i nie odpowiada standardom endodontycznym osiąganym w technologii NiTi21-23. Niemniej jednak, lasery Erbium, Chromium: YSGG (Er, Cr: YSGG) oraz Erbium: YAG (Er: YAG) otrzymały zgodę FDA (Agencji Żywności i Leków) dla stosowania w czyszczeniu, kształtowaniu i powiększaniu kanałów. W kilku badaniach potwierdzono skuteczność tych systemów w kształtowaniu i powiększaniu kanałów korzeniowych. Shoji et al. zastosowali system laserowy Er: YAG ze stożkową końcówką, emisją boczną wynoszącą 80% oraz emisją przy końcówce wynoszącą 20% w celu powiększenia i oczyszczenia kanałów, przy wykorzystaniu 10-40 mJ dla 10 Hz. Otrzymali czystsze powierzchnie zębiny w porównaniu do technik obrotowych.24 Ryc. 3 patent FDA dla całej procedury endodontycznej (powiększanie, czyszczenie oraz odkażanie), z końcówkami 400, 320 i 200 μm, po kolei i od korony ku dołowi, przy 1.5 W oraz 20 Hz (z powietrzem/wodą w sprayu 35/25%).26,27 Stabholz et al. przedstawili pozytywne wyniki leczenia przeprowadzonego całościowo z wykorzystaniem lasera Er: YAG oraz endodontycznych mikrosond do emisji bocznej.28,29 Ali et al., Matsouka et al. oraz Jahan et al. wykorzystali laser Er, Cr: YSGG do przygotowania prostych i zakrzywionych kanałów, ale w tym przypadku wyniki grupy eksperymentalnej były gorsze od wyników grupy kontrolnej. Stosując laser Er, CR: YSGG o końcówkach 200-320 μm przy 2 W i 20 Hz na prostych i zakrzywionych kanałach, doszli do wniosku, że promieniowanie laserowe może przygotować proste i zakrzywione kanały (poniżej 10°), podczas gdy bardziej zakrzywione kana- We wstępnym badaniu skuteczności lasera Er: YAG wyposażonego w mikrosondę z emisją promieniową wynoszącą 200-400 μm, Kesler et al. przekonali się, że laser pozwala na szybsze i lepsze powiększanie i kształtowanie w porównaniu z metodami tradycyjnymi. Obserwacje SEM wykazały jednolicie czystą powierzchnię zębiny na wierzchołku fragmentu korony, bez resztek miazgi, a także dobrze wyczyszczone kanaliki zębinowe.25 Chen przedstawił badania kliniczne przeprowadzone z wykorzystaniem lasera Er, Cr: YSGG – pierwszego lasera, który otrzymał Ryc. 4 laser 2_2014 15 Praktyka _ Standardy postępowania Ryc. 5 Ryc. 6 ły wykazały skutki uboczne takie, jak: perforacje, wypalenie i przesunięcie kanału.21-23 Inamoto et al. zbadali umiejętność cięcia i morfologiczne skutki promieniowania lasera Er:YAG in vitro, stosując 30 mJ przy 10 i 25 Hz i przy prędkości ekstrakcji włókna wynoszącej 1 i 2 mm/s, również uzyskując pozytywne wyniki.30 Minas et al. zaobserwowali pozytywne wyniki, stosując laser Er, Cr: YSGG przy 1,5; 1,75 i 2,0 W oraz 20 Hz, ze sprayem wodnym.31 Powierzchnie przygotowane przy pomocy lasera Erbium są dobrze oczyszczone, bez warstwy mazi, ale często pojawiają się krawędzie, nierówności i osmolenia, niosące za sobą ryzyko perforacji czy przesunięcia wierzchołkowego. Podsumowując, kształtowanie kanałów przy pomocy lasera Erbium do dziś pozostaje skomplikowaną procedurą, którą można przeprowadzać jedynie na dużych i prostych kanałach, bez szczególnych korzyści. _Odkażanie układu endodontycznego Badania dotyczące odkażania kanałów odnoszą się do działania chemicznych substancji Ryc. 7 16 Ryc. 8 laser 2_2014 płuczących (NaClO), powszechnie stosowanych w endodoncji, w połączeniu z substancjami chelatującymi dla lepszego oczyszczenia kanalików zębinowych (kwas cytrynowy i kwas edetynowy). Jednym z takich badań jest badanie Berutti et al., którzy zaobserwowali odkażające właściwości NaClO do głębokości 130 μm na ścianie korzenia.32 Lasery początkowo zostały wprowadzone do endodoncji w celu zwiększenia poziomu odkażania układu endodontycznego. Wszystkie długości fali mają silne właściwości przeciwbakteryjne ze względu na ich termiczne oddziaływanie, które przy różnej mocy oraz przy zmiennej zdolności do penetrowania ścianek zębiny wywołuje ważne zmiany strukturalne w ściankach komórkowych bakterii. Początkowe uszkodzenie następuje w ściankach komórkowych, wywołując zmiany w gradiencie osmotycznym, prowadzące do pęcznienia i obumarcia komórki.16,34 _Odkażanie laserem w bliskiej podczerwieni Odkażanie kanałów wspomagane laserem w bliskiej podczerwieni wymaga tradycyjnego przygotowania kanałów (wierzchołkowe przygotowanie z ISO 25/30), jako że długość fali nie wykazuje skłonności wobec twardych tkanek i tym samym nie wywołuje efektu ablacyjnego. Promieniowanie stosowane jest pod koniec tradycyjnego przygotowania endodontycznego jako końcowy środek do odkażania układu endodontycznego przed zatkaniem. Włókno optyczne o średnicy 200 μm umieszczane jest Praktyka _ Standardy postępowania w odległości 1 mm od wierzchołka i wycofywane ruchem spiralnym na powierzchni korony (w ciągu 5-10 s zgodnie z różnymi procedurami). Obecnie zaleca się przeprowadzanie tej procedury w kanale wypełnionym endodontyczną substancją płuczącą (najlepiej EDTA lub kwas cytrynowy; ewentualnie NaClO), aby zredukować niepożądane skutki morfologiczne.9,35-38 Wykorzystując model eksperymentalny, Schoop et al. wykazali sposób, w jaki lasery rozprowadzają swoją energię i wnikają w głąb ściany zębiny, podkreślając ich większą skuteczność w porównaniu z tradycyjnymi płuczącymi systemami chemicznymi w odkażaniu ścian zębinowych.8 Laser Neodymium: YAG (Nd:YAG; 1,064 nm) dokonał redukcji bakterii na poziomie 85% przy 1 mm, w porównaniu z laserem diodowym (810 nm), pozwalającym na 63% redukcję przy 750 μm lub mniej. Ta znacząca różnica w penetracji wynika z niskiej i zmiennej skłonności do tkanek twardych, wykazywanej przez podane długości fali. Zdolność dyfuzyjna, która nie jest jednakowa, pozwala światłu dotrzeć i zniszczyć bakterie poprzez penetrację opartą na oddziaływaniu termicznym (Ryc. 1). Wiele innych badań mikrobiologicznych potwierdziło silne działanie przeciwbakteryjne laserów diodowych i Nd: YAG. Stopień odkażania obciążenia bakteryjnego w kanale głównym sięgał 100%.39-43 Badanie in vitro przeprowadzone przez Benedicenti et al. wykazało, że użycie lasera diodowego 810 nm w połączeniu z chelatującymi substancjami płuczącymi, takimi jak kwas cytrynowy czy EDTA, zaowocowało niemalże całkowitą re- Ryc. 9 dukcją obciążenia bakteryjnego (99,9%) E. faecalis w układzie endodontycznym.9 _Odkażanie za pomocą lasera o średniej podczerwieni Biorąc pod uwagę niewielką skuteczność w penetracji kanałowej i kształtowaniu, użycie lasera Erbium do odkażania endodontycznego wymaga zastosowania tradycyjnych technik w przygotowaniu kanału. Wierzchołek kanału powinien zostać przygotowany za pomocą przyrządów ISO 25/20. Końcowe przejście z użyciem lasera możliwe jest dzięki zastosowaniu długich, cienkich końcówek (200 i 300 μm), dostępnych dla licznych przyrządów Erbium, co pozwoli z większą łatwością osiągnąć długość roboczą (1 mm od wierzchołka). W tej metodologii tradycyjna technika polega na wykonywaniu sferycznych ruchów w czasie wyciągania końcówki (przerwy powyżej 5-10 s), z 3 lub 4 powtórzeniami, w zależności od procedury, przeplatając napromieniowywanie z płukaniem przy wykorzystaniu tradycyjnych substancji płuczących i utrzymaniem wilgotności kanału podczas wykonywania procedury (NAClO i/lub EDTA) ze zintegrowanym sprayem. Trójwymiarowego odkażania układu endodontycznego przy pomocy lasera Erbium nie można jeszcze porównać z odkażaniem przy pomocy laserów o bliskiej podczerwieni. Energia termiczna wytworzona przez te lasery jest początkowo pochłaniana na powierzchni (duża skłonność wobec tkanki zębinowej bogatej w wodę), gdzie laser wykazuje największe właściwości przeciwbakteryjne dla E. coli (bakteria Gram-ujemna) i E. faecalis (bakteria Gram-dodatnia). Przy mocy 1,5 W Mortiz et al. uzyskali prawie Ryc. 10 laser 2_2014 17 Praktyka _ Standardy postępowania Celem trwających badań jest ocena skuteczności nowej techniki laserowej, która wykorzystuje nowozaprojektowaną, zarówno promieniową, jak i tulejkowatą końcówkę do usuwania nie tylko warstwy mazi, ale również bakteryjnego bioilmu.13 Wyniki są bardzo obiecujące. Ryc. 11 Ryc. 12 całkowity poziom usunięcia tych bakterii (99,64%).44 Jednakże, systemy te nie mają właściwości przeciwbakteryjnych głęboko w kanałach bocznych, jako że sięgają jedynie 300 μm głębokości podczas testowania na szerokości ściany korzenia.8 Późniejsze badania skupiły się na zdolności lasera Er, Cr: YSGG do odkażania tradycyjnie przygotowanych kanałów. Wykorzystując niewielką moc (0,5 W, 10 Hz, 50 mJ, z 20% powietrzem/wodą w sprayu), nie uzyskano całkowitej redukcji bakterii. Niemniej jednak, lepsze rezultaty dla lasera Er, Cr: YSGG osiągnięto przy redukcji wynoszącej 77% dla 1W i 96% dla 1,5 W.42 Inny obszar badawczy został poświęcony zdolności lasera Erbium do usuwania bioilmu bakteryjnego z wierzchołkowej tercji,46 a ostatnie badanie in vitro potwierdziło zdolność lasera Er: YAG do usuwania endodontycznego bioilmu wielu gatunków bakterii (np. A. naeslundii, E. faecalis, L. casei, P. acnes, F. nucleatum, P. gingivalis czy P. nigrescens), przy znaczącej redukcji komórek bakteryjnych i rozpadzie bioilmu. Wyjątek stanowi bioilm utworzony przez L. casei.47 Ryc. 13 18 laser 2_2014 Lasery Erbium z końcówkami „end-iring” – czołowa emisja na czubku końcówki – cechują się niewielką boczną penetracją ściany zębiny. Promieniowa końcówka została zaproponowana w 2007 r. dla Er, Cr: YSGG, a Gordon et al. oraz Schoop et al. zbadali morfologiczne i odkażające efekty stosowania tego systemu laserowego (Ryc. 2).48-50 W pierwszym badaniu wykorzystano końcówkę 200 μm z emisją promieniową dla 20 Hz, przy użyciu powietrza/wody w sprayu (43 i 28%) i z osuszaniem w warunkach 10 i 20 mJ i 20 Hz (0,2 i 0,4 W odpowiednio). Czas promieniowania wahał się od 15 s do 2 min. Największe właściwości przeciwbakteryjne osiągnięto przy maksymalnej mocy (0,4 W), przy dłuższym czasie wystawienia na promieniowanie, bez wody w trybie suszenia – redukcja bakterii wyniosła 99,71%. Minimalny czas naświetlana (15 s) przy minimalnej mocy (0,2 W) i z wodą pozwoliło na redukcję bakterii na poziomie 94,7%.48 W drugim badaniu użyto końcówki o średnicy 300 μm i 2 różnych parametrach emisji (1 i 1,5 W, 20 Hz), z promieniowaniem 5 razy przez 5 s oraz z czasem chłodzenia wynoszącym 20 s na każde przejście. Uzyskany poziom odkażania był znacząco wysoki. Zaobserwowano ważne różnice pomiędzy 1 a 1,5 W, a wzrost temperatury zawarł się pomiędzy 2,7 i 3,2° C.49 Ta sama grupa z Wiednia przebadała inne parametry (0,6 i 0,9 W), które spowodowały bardzo zwarty wzrost temperatury wynoszący odpowiednio 1,3 i 1,6° C, wykazując silne działanie przeciwbakteryjne wobec E. coli i E. faecalis.50 Potrzeba wykorzystania efektów termalnych do niszczenia komórek bakteryjnych skutkuje zmianami na poziomie zębiny i okołozębowym. Istotna jest ocena najlepszych parametrów i zgłębianie nowych technik, które zredukują do minimum niepożądany wpływ termalny, jaki lasery wywierają na twarde i miękkie struktury tkanek. Praktyka _ Standardy postępowania Ryc. 15 Ryc. 14 _Skutki morfologiczne na powierzchni zębiny Liczne badania skupiły się na morfologicznych skutkach promieniowania laserowego wywieranych na ściany korzenia jako uboczne skutki odkażania kanału korzeniowego i czyszczenia przeprowadzonego przy pomocy różnych laserów. Przy działaniu na sucho lasery bliskiej i średniej podczerwieni powodują charakterystyczne efekty termiczne (Ryc. 3 i 4).51 Lasery bliskiej podczerwieni wywołują charakterystyczne zmiany morfologiczne w ścianie zębiny: warstwa mazi jest tylko częściowo usunięta, a kanaliki zębinowe są pierwotnie zamykane w wyniku topnienia nieorganicznych struktur zębiny. Rekrystalizacyjne pęcherzyki i pęknięcia są wyraźne (Ryc 5-8).52-55 Ryc. 16 oczyszczona z mazi, kanaliki zębinowe otwarte, a uszkodzenia termiczne mniej widoczne.35-38 W podsumowaniu swojego badania nad laserem Erbium, Yamazaki et Woda obecna w roztworach płuczących ogranicza termiczną interakcję wiązki lasera ze ścianą zębiny i jednocześnie oddziałuje aktywowana termicznie przez laser o bliskiej podczerwieni (docelowy chromofor) o szczególnym działaniu (dezynfekcja i chelatacja). Promieniowanie lasera o bliskiej podczerwieni – diodowego (2,5 W, 15 Hz) oraz Nd: YAG (1,5 W, 100 mJ, 15 Hz) – przeprowadzone po zastosowaniu roztworu płuczącego pozwala na otrzymanie lepszej formy zębiny, porównywalnej do otrzymanej jedynie przy pomocy środka płuczącego. Napromieniowanie z NaClO lub chlorheksydyną tworzy morfologię o zamkniętych kanalikach zębinowych i obecności niewielkiej warstwy mazi, ale o ograniczonym obszarze topnienia w porównaniu z karbonizacją zaobserwowaną w czasie suchego napromieniowania. Najlepsze rezultaty otrzymano, gdy promieniowanie nastąpiło po płukaniu EDTA. Powierzchnia była Ryc. 17 Ryc. 18 laser 2_2014 19 Praktyka _ Standardy postępowania Ryc. 19 Ryc. 20 al. oraz Kimura et al. potwierdzili, że woda jest potrzebna do uniknięcia niepożądanych cech morfologicznych, wyraźnie obecnych podczas przeprowadzania napromieniowania laserem Erbium na sucho.56,57 Lasery Erbium używane w ten sposób powodują oznaki ablacji i uszkodzenia termicznego w wyniku zastosowanej mocy. Dowiedziono występowania pęknięć na krawędziach, obszarów powierzchniowego topnienia i odparowania warstwy mazi. Typowa forma pojawia się, gdy zębina płukana jest przy pomocy lasera Erbium z wykorzystaniem wody. Uszkodzenie termiczne jest zredukowane, a kanaliki zębinowe są otwarte na górze bardziej zwapnionych i poddanych ablacji obszarów okołokanalikowych. Wewnątrzkanalikowa zębina, bardziej bogata w wodę jest w większym stopniu poddana ablacji. Warstwa mazi ulega odparowaniu dzięki działaniu promieniowania lasera Erbium i właściwie nie występuje.58-64 Shoop et al., badając wahania temperatury na powierzchni korzeniowej in vitro odkryli, że standardowa energia (100 mJ, 15 Hz, 1,5 W) powodowała wzrost temperatury o 3,5° C na powierzchni przyzębia. Moritz zaproponował, by te parametry zostały uznane za międzynarodowe standardy dla stosowania laserów Erbium w endodoncji, postrzegając je jako skuteczny sposób na czyszczenie i odkażanie kanałów (Ryc. 9-12).14,16 Nawet z laserami Erbium zaleca się stosowanie roztworów płuczących. NaClO i EDTA mogą być stosowane zamiennie podczas termicznej fazy leczenia endodontycznego wspomaganego laserowo, w konsekwencji czego forma zębiny przejawia mniej skutków termicznych. Stanowi to nowy obszar badań 20 laser 2_2014 w dziedzinie endodoncji wspomaganej laserowo. Zaproponowanych zostało wiele technik, takich jak płukanie aktywowane laserowo (LAI) czy strumień fotoakustyczny aktywowany przez foton (PIPS). _Fototermiczne i fotomechaniczne zjawiska w usuwaniu warstwy mazi George et al. opublikowali pierwsze badanie poświęcone zdolności lasera do aktywowania płuczącej cieczy wewnątrz kanału korzeniowego w celu zwiększenia jej działania. W badaniu tym końcówki 2 systemów laserowych – Er:YAG i Er. Cr: YSGG (400 μm średnicy, zarówno płaskie, jak i cylindryczne) z usuniętą chemicznie zewnętrzną powłoką zostały wykorzystane do bocznego rozprowadzania energii. Badanie zostało tak zaprojektowane, aby wypłukać kanały korzeniowe przygotowane wcześniej z grubą warstwą mazi wyhodowanej doświadczalnie. Po porównaniu wyników 2 grup naświetlanych laserowo z grupami, które nie były poddane działaniu lasera, badanie wykazało, że laserowa aktywacja substancji płuczących (zwłaszcza EDTAC) przyczyniła się do lepszego oczyszczenia i usunięcia warstwy mazi z powierzchni zębiny.65 W późniejszym badaniu autorzy zauważyli, że procedura ta, wykorzystująca moc 1 i 0,75 W, powoduje wzrost temperatury jedynie o 2,5° C, nie uszkadzając struktur przyzębia.66 Blanken i De Moor również zbadali skutki aktywacji laserowej substancji płuczących w porównaniu w konwencjonalnym płuka- Praktyka _ Standardy postępowania niem (CI) i biernym płukaniem ultradźwiękowym (PUI). W badaniu tym, 2,5% NaClO oraz laser Er, Cr: YSGG użyte zostały 4 razy po 5 s przy parametrach: 75 mJ, 20 Hz, 1,5 W z końcówką endodontyczną (200 μm średnicy, płaska końcówka), trzymaną prosto 5 mm od wierzchołka. Usuwanie warstwy mazi w trakcie tej procedury przyniosło znacznie lepsze rezultaty niż w przypadku 2 poprzednich metod.67 Fotomikrograiczne badanie eksperymentu sugeruje, że laser powoduje ruch płynów o dużej prędkości poprzez efekt kawitacji. Rozprzestrzenianie się i sukcesywna implozja substancji płuczących (na skutek efektu termicznego) powodują uzupełniające działanie kawitacyjne na płyny wewnątrz kanału. Nie było konieczne przesuwanie włókna w górę i w dół kanału. Wystarczyło utrzymać je prosto w środkowej tercji, 5 mm od wierzchołka.68 Koncepcja ta znacznie ułatwia technikę laserową bez potrzeby sięgania do wierzchołka i pokonywania zakrzywień korzenia (Ryc. 13). De Moor et al. porównali technikę LAI z PUI i doszli do wniosku, że technika laserowa, wykorzystująca krótszy czas płukania (4 razy po 5 s) daje wyniki porównywalne do techniki ultradźwiękowej, która zakłada dłuższy czas płukania (3 razy po 20 s).69 De Groot et al. również potwierdzili skuteczność techniki LAI oraz lepsze wyniki w porównaniu z PUI. Autorzy podkreślili koncepcję strumienia w wyniku opadania cząsteczek wody w zastosowanych roztworach płuczących.70 Hmud et al. zbadali możliwość wykorzystania laserów o bliskiej podczerwieni (940 i 980 nm) z włóknem 200 μm do aktywowania substancji płuczących przy parametrach, odpowiednio 4 W i 10 Hz oraz 2,5 W i 25 Hz. Biorąc pod uwagę brak kojarzenia pomiędzy tymi długościami fali a wodą, potrzebne były wyższe wartości mocy, które poprzez kawitację i efekt termiczny wywołały ruch płynów w kanale korzeniowym, prowadząc do zwiększonej zdolności do usuwania resztek i warstwy mazi.71 W późniejszym badaniu autorzy zweryikowali także bezpieczeństwo zastosowania wyższych mocy, co spowodowało wzrost temperatury o 30° C w wewnątrzkanałowym roztworze płuczącym, ale jedynie o 4° C na zewnętrznej powierzchni korzeniowej. Badanie wykazało, że płukanie aktywowane przez lasery o bliskiej podczerwieni jest bardzo skuteczne pod względem minimalizowania wpływu termicznego na zębinę i spoiwo korzenia.72 W niedawno przeprowadzonym badaniu Macedo et al. nawiązali do kluczowej roli aktywacji jako silnego modulatora wskaźnika reakcji NaOCl. Podczas 3-minutowej przerwy pochłanianie dostępnej chloryny znacznie wzrosło po LAI w porównaniu z PUI czy Cl.73 _Strumień fotoakustyczny aktywowany przez foton (PIPS) Technika PIPS wykorzystuje laser Erbium (Powerlase AT/HT i LightWalker AT, oba Fotona) oraz ich interakcję z roztworami płuczącymi (EDTA, NaOCl lub woda de- Ryc. 21 Ryc. 22 laser 2_2014 21 Praktyka _ Standardy postępowania strzenianie się i kolejne „fale wstrząsowe”, prowadzące do powstania silnego strumienia płynów wewnątrz kanału, nie powodując przy tym niepożądanych skutków termicznych, obserwowanych w innych metodologiach. Ryc. 23 Ryc. 24 Ryc. 25 stylowana).13 Technika ta wykorzystuje inny mechanizm niż poprzedni LAI. Bazuje wyłącznie na zjawisku fotoakustycznym i fotomechanicznym, wynikających z zastosowania subablacyjnej energii 20 mJ przy 15 Hz, z impulsami trwającymi 50 mikrosekund. Ze średnią mocą wynoszącą zaledwie 0,3 W każdy impuls reaguje z cząsteczkami wody przy szczytowej mocy 400 W, powodując rozprze- 22 laser 2_2014 Badanie z termoogniwami, zastosowane jedynie wobec wierzchołkowej tercji korzenia wykazało wzrost termiczny wynoszący zaledwie 1,2° C po 20 s i 1,5° C po 40 s ciągłego naświetlania. Inna znacząca przewaga wynika z umieszczenia końcówki w komorze miazgi zęba przy wejściu do kanału korzeniowego, bez problematycznego umieszczania końcówki w kanale i 1 mm od wierzchołka, czego wymagają inne techniki (LAI i Cl). Stosowane są nowo zaprojektowane końcówki – 9 mm długości, 600 μm średnicy, z „promieniową lub prążkowaną końcówką”. Ostatnie 3 mm pozbawione są powłoki, co pozwala na większą boczną emisję energii w porównaniu z frontalną końcówką. Taki tryb emisji energii pozwala na lepsze wykorzystanie energii lasera, kiedy na poziomach subablatywnych doprowadzanie z wysoką mocą szczytową dla każdego pulsu 50 mikrosekund (400 W) powoduje silne „fale wstrząsowe” w substancjach płuczących, wywierając wyraźny i znaczący wpływ mechaniczny na ścianę zębiny (Ryc. 1416). Powstały strumień akustyczny pozwala na trójwymiarowe ruchy w obrębie systemu kanału korzenia, dzięki czemu lekarz praktyk ma lepszy dostęp do złożonej anatomii, często widocznej w jednej tercji wierzchołka. Badania pokazują, że usunięcie warstwy mazi jest wyższe w porównaniu z grupą kontrolną, w której zastosowano jedynie EDTA lub wodę destylowaną. Próbki poddane działaniu lasera i EDTA przez 20-40 s wykazują całkowite usunięcie warstwy mazi przy otwartych kanalikach zębinowych (punktacja 1 wg Hulsmanna) oraz brak niepożądanych zjawisk termicznych, co jest charakterystyczne dla ścian zębinowych poddanych działaniu tradycyjnych technik laserowych. Przy dużym powiększeniu struktura kolagenowa jest nienaruszona, co sugeruje możliwość przeprowadzenia minimalnie inwazyjnego zabiegu endodontycznego (Ryc. 17-19). Grupa medyczna zajmująca się zawansowanymi technologiami w dziedzinie stomatologii (Medical Dental Advanced Technologies Group) we współpracy z Uniwersytetem Paciic Arthur A. Dugoni School of Dentistry, Uniwersytetem w Genui, Uniwersytetem Praktyka _ Standardy postępowania Loma Linda School of Dentistry, Uniwersytetem w Tennessee, Uniwersytetem w Bostonie, Uniwersytetem Stanu Luizjana oraz Arizona School of Dentistry and Oral Health prowadzi obecnie badania nad skutkami zastosowania techniki odkażania kanału korzeniowego i usuwania bioilmu bakteryjnego w kanale korzeniowym. Wyniki, które mają być opublikowane są bardzo obiecujące (Ryc. 20-25). _Dyskusja i wnioski Technologia laserowa stosowana w endodoncji przszła ważną ewolucję w ciągu ostatnich 20 lat. Ulepszona technologia pozwoliła na wprowadzenie włókien endodontycznych i końcówek o kalibrze i elastyczności, które pozwalają na insercję do 1 mm od wierzchołka. Badania w ostatnich latach ukierunkowane były na technologie wytwarzania (impulsy o zredukowanej długości, końcówki prążkowane czy końcówki typu radial iring) oraz techniki (LAI i PIPS), które ułatwiają ich zastosowanie w endodoncji i minimalizują niepożądane efekty termiczne na ściankach zębiny, wykorzystując mniejszą energię w obecności chemicznych substancji płuczących. EDTA okazała się najlepszym rozwiązaniem dla techniki LAI, ponieważ aktywuje płyn, zwiększa jego właściwości chelatujące oraz stopień czyszczenia warstwy mazi. Wykorzystanie NAClO zwiększa działanie odkażające. Wreszcie, technika PIPS redukuje skutki termiczne i wykazuje silne działanie czyszczące i przeciwbakteryjne dzięki trójwymiarowemu strumieniowi płynów, zainicjowanemu przez energię fotoniczną lasera. Celem przyszłych badań jest ocena tych technik (LAI i PIPS) jako innowacyjnych technologii dostępnych w endodoncji. _ Piśmiennictwo dostępne u wydawcy. Niniejszy artykuł w wersji oryginalnej został opublikowany w międzynarodowym wydaniu „Laser” nr 2/2011. _autor Enrico DiVito, DDS – główny autor niniejszego artykułu rozpoczął swą praktykę stomatologiczną w Scottsdale, Arizona, w 1900 r. Jest założycielem i dyrektorem akredytowanej Arizona School of Dental Assisting. Oprócz wykładowcy, DiVito jest także instruktorem klinicznym w Arizona School of Dentistry and Oral Health. Jest odpowiedzialny za pomoc w utworzeniu Wydziału Stomatologii Laserowej. Zdobył tytuł pierwszego stopnia w Arizona State University oraz z wyróżnieniem ukończył Dental School przy University of Paciic w San Francisco, otrzymując liczne nagrody za wybitne osiągnięcia. Z autorem można się skontaktować, pisząc na adres: [email protected] laser 2_2014 23