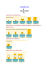BUDOWA I WŁAŚCIWOŚCI AMINOKWASÓW
Transkrypt
BUDOWA I WŁAŚCIWOŚCI AMINOKWASÓW
1 Ć WICZENIE 1 BUDOWA I WŁAŚCIWOŚCI AMINOKWASÓW 1.1. AMINOKWASY BIAŁKOWE Aminokwasy są związkami organicznymi zawierającymi co najmniej jedną grupę karboksylową -COOH oraz co najmniej jedną grupę aminową -NH2. W zależności od położenia grupy aminowej względem karboksylowej wyróżniamy α-, β- i γ-aminokwasy. W przyrodzie występuje ponad 300 różnych aminokwasów, ale tylko 20 z nich wchodzi w skład białek (tzn. są kodowane w kodzie genetycznym). Wszystkie aminokwasy białkowe są α-aminokwasami, w których grupa aminowa znajduje się przy atomie węgla bezpośrednio sąsiadującym z grupą karboksylową (tzw. atomie węgla α). Wyjątek stanowi prolina, która posiada grupę aminową wbudowaną w pierścień. Aminokwasy niebiałkowe także często pełnią istotne funkcje biologiczne np. β-alanina wchodzi w skład koenzymu A, a kwas γ-aminomasłowy jest neuroprzekaźnikiem. Ciekawym aminokwasem niebiałkowym, który powstaje w wyniku modyfikacji istniejącego łańcucha polipeptydowego jest hydroksyprolina występująca w niektórych białkach (np. w kolagenie). Ogólna struktura α-aminokwasów oraz przykładowe β- i γ-aminokwasy zostały przedstawione na rys 1.1. Rys. 1.1 Aminokwasy Wśród białkowych aminokwasów tylko glicyna (R = H) jest achiralna. Wszystkie pozostałe aminokwasy mają cztery różne podstawniki przy węglu α (asymetrycznym), są zatem cząsteczkami chiralnymi, mogącymi występować jako enancjomery określane umownie jako L i D (projekcja Fischera). Wszystkie chiralne aminokwasy białkowe należą do szeregu L (wyjątek stanowi prolina). Z punktu widzenia konfiguracji absolutnej (projekcja Newmana wg zasady Cahna, Ingolda i Preloga) wszystkie aminokwasy mają konfigurację (S) (z wyjątkiem (R)-cysteiny) (rys. 1.2). Chiralne aminokwasy wykazują czynność optyczną, czyli skręcają płaszczyznę światła spolaryzowanego o pewien Laboratorium Biochemii, Wydział Chemiczny PW 2 kąt, charakterystyczny dla danego aminokwasu. Znak skręcalności ((+) lub (-)) jest jedyną wielkością, która pozwala rozróżnić enancjomery danego aminokwasu, ponieważ wszystkie pozostałe właściwości fizyczne i chemiczne są identyczne. Rys. 1.2. Konfiguracja aminokwasów na przykładzie alaniny L-aminokwasy, zależnie od zdolności organizmu do syntezy, dzieli się na endogenne oraz egzogenne. Człowiek może syntezować jedynie część podstawowego zestawu aminokwasów, które są nazywane aminokwasami endogennymi. Pozostałe (egzogenne) muszą być dostarczane z pożywieniem. Są to walina, leucyna, izoleucyna (o rozgałęzionych łańcuchach bocznych), fenyloalanina, tryptofan (zawierające pierścień aromatyczny), lizyna, treonina i metionina, a u dzieci także histydyna i arginina. D-aminokwasy występują w stanie wolnym, ścianie komórkowej bakterii oraz w antybiotykach peptydowych i są nieprzyswajalne przez zwierzęta i człowieka. Właściwości chemiczne aminokwasów wynikają z jednoczesnej obecności dwóch grup funkcyjnych – aminowej i karboksylowej. Powoduje to, że aminokwasy są związkami amfoterycznymi, czyli mogą reagować zarówno jak kwasy i jak zasady. W roztworach wodnych cząsteczki aminokwasów występują w formie niezjonizowanej tylko w ilości 0,1%, natomiast reszta cząsteczek to jony. Sumaryczny ładunek cząsteczki aminokwasu zależy od pH środowiska. W roztworach wodnych występuje równowaga kwasowo–zasadowa pomiędzy kationem i anionem oraz jonem obojnaczym (zwitterionem) powstałym w wyniku oddziaływania grup funkcyjnych w obrębie tej samej cząsteczki (rys. 1.3). Rys. 1.3. Równowaga kwasowo-zasadowa Laboratorium Biochemii, Wydział Chemiczny PW 3 W środowisku silnie kwasowym aminokwasy występują jako kationy, w środowisku silnie zasadowym – jako aniony. Stałe równowagi (pKa) tych przemian są charakterystyczne dla poszczególnych aminokwasów. Dodatkowo aminokwasy zasadowe i kwasowe określa się także pKa grup bocznych. Istnieje także takie pH roztworu w którym ładunek sumaryczny cząsteczki jest równy zeru, a aminokwas występuje w formie jonu obojnaczego. Takie pH nosi nazwę punktu izoelektrycznego (pI). Wartości pI dla większości aminokwasów białkowych są bliskie 6. W przypadku aminokwasów posiadających dodatkowe grupy aminowe lub karboksylowe punkt izoelektryczny ulega przesunięciu z uwagi na dodatkową jonizację tych grup (tabela 1.1). Stałe dysocjacji i wartość punktu izoelektrycznego wyznacza się przez miareczkowanie roztworami silnych kwasów i zasad. Tabela 1.1. Przykładowe wartości pI i pKa aminokwasów aminokwas Ala Leu Ser His Arg Lys Asp Glu pI 6,02 5,98 5,68 7,74 10,76 9,74 2,87 3,22 pKa2 9,87 9,74 9,21 9,33 8,99 9,06 9,90 9,47 pKa1 2,35 2,33 2,19 1,80 1,82 2,16 1,99 2,10 pKa gr. bocz. 6,04 12,48 10,54 3,90 4,07 Stosuje się różne kryteria klasyfikacji aminokwasów. Biorąc pod uwagę budowę łańcuchów bocznych aminokwasy możemy podzielić na: alifatyczne obojętne, alifatyczne hydroksyaminokwasy, siarkowe, zasadowe, kwasowe i ich monoamidy oraz aminokwasy z pierścieniem aromatycznym. Poza wymienionymi grupami podziału znajduje się pozbawiona łańcucha bocznego glicyna. 1.1.1. Aminokwasy alifatyczne obojętne Do tej grupy należą: alanina, walina, leucyna, izoleucyna oraz prolina, których wzory strukturalne przedstawione są na rys. 1.4. Aminokwasy te zawierają alifatyczny, niepolarny, a zatem hydrofobowy łańcuch boczny (R). Laboratorium Biochemii, Wydział Chemiczny PW 4 Rys. 1.4. Aminokwasy alifatyczne obojętne 1.1.2. Alifatyczne hydroksyaminokwasy Alifatyczne hydroksyaminokwasy to seryna i treonina (rys. 1.5.). Ich łańcuchy boczne są neutralne (pozbawione ładunku) i polarne dzięki obecności grupy hydroksylowej. Rys. 1.5. Alifatyczne hydroksyaminokwasy 1.1.3. Aminokwasy siarkowe Do aminokwasów siarkowych (rys. 1.6.) należą: cysteina (zawierająca grupę tiolową SH) i metionina (zawierająca grupę tiometylową SCH3). Cysteina pod wpływem łagodnych czynników utleniających dimeryzuje do cystyny (Cys)2 z utworzeniem wiązania disiarczkowego. Laboratorium Biochemii, Wydział Chemiczny PW 5 Rys. 1.6. Aminokwasy siarkowe 1.1.4. Aminokwasy zasadowe Aminokwasami zasadowymi (rys. 1.7) są: lizyna (zawierająca na końcu łańcucha bocznego grupę aminową), arginina (zawierająca grupę guanidynową) oraz histydyna (posiadająca silnie zasadowy pierścień imidazolowy). Rys. 1.7. Aminokwasy zasadowe 1.1.5. Aminokwasy kwasowe i ich amidy Do aminokwasów kwasowych (rys 1.8.) zalicza się kwas asparaginowy i kwas glutaminowy. W łańcuchach bocznych tych aminokwasów znajduje się dodatkowa grupa karboksylowa. Amidami kwasów asparaginowego i glutaminowego są asparagina i glutamina. Laboratorium Biochemii, Wydział Chemiczny PW 6 Rys. 1.8. Aminokwasy kwasowe i ich amidy 1.1.6. Aminokwasy z pierścieniem aromatycznym Do tej grupy należą aminokwasy zawierające podstawnik aromatyczny (rys. 1.9) czyli: fenyloalanina, tyrozyna i tryptofan. Obecność pierścienia aromatycznego warunkuje zdolność do pochłaniania promieniowania UV w zakresie 260 – 290 nm (właściwość ta jest wykorzystywana w metodach ilościowego oznaczania białka). Tyrozyna zawiera dodatkowo grupę hydroksylową w pierścieniu. Tryptofan jest aminokwasem heteroaromatycznym. Rys. 1.9. Aminokwasy aromatyczne Laboratorium Biochemii, Wydział Chemiczny PW 7 1.2. WYKONANIE ĆWICZENIA Najbardziej charakterystyczną reakcją barwną α-aminokwasów jest reakcja z ninhydryną. Jest ona uwarunkowana równoczesną obecnością wolnej grupy aminowej i karboksylowej przy tym samym atomie węgla. W reakcjach barwnych uwarunkowanych budową łańcucha bocznego aminokwasu, pozytywne wyniki dają również związki nie będące aminokwasami, których cząsteczki zawierają takie same lub podobne grupy funkcyjne. Białka, zawierające z reguły wszystkie rodzaje aminokwasów, dają również pozytywne odczyny w reakcjach na łańcuchy boczne poszczególnych aminokwasów. Istnieje ponadto szereg reakcji związanych z charakterystycznymi cechami budowy białek. Do reakcji wykorzystujących obecność wiązań peptydowych lub specyficzną budowę przestrzenna cząsteczki należą: reakcja biuretowa i reakcje oparte na wytracaniu białka z roztworu za pomocą różnych czynników denaturujących. Schemat postępowania w celu identyfikacji aminokwasów przy wykorzystaniu barwnych reakcji wskaźnikowych przedstawia rysunek 1.10. Odczynniki: 1. 1% roztwory aminokwasów: glicyny (Gly), cystyny ([Cys]2), fenyloalaniny (Phe), tyrozyny (Tyr), tryptofanu (Trp), histydyny (His), argininy (Arg) 2. 1% roztwór białka (albuminy lub kazeiny) 3. 0,2M bufor fosforanowy pH 6,0 4. 6M NaOH 5. 10% NaOH 6. 1% α-naftol w etanolu 7. 1% NaBrO 8. HNO3 stężony 9. H2SO4 stężony 10. 0,5% roztwór CuSO4 11. 20% kwas trichlorooctowy (TCA) 12. 2% roztwór octanu ołowiu(II) (Uwaga! Silna trucizna!) 13. odczynnik Millona: 10 g rtęci metalicznej rozpuścić w 14 ml stężonego HNO3 i rozcieńczyć dwukrotną objętością wody (Uwaga! Silna trucizna!) 14. roztwór kwasu glioksalowego: roztwór a – 1 g pyłu magnezowego zalać 20 ml wody; roztwór b – 2,5 g kwasu szczawiowego rozpuścić w 25 ml wody; w celu sporządzenia roztworu kwasu glioksalowego należy do roztworu b wlać roztwór a, po czym ochłodzić, przesączyć, dodać 2,5 ml lodowatego kwasu octowego i dopełnić wodą do 100 ml 15. 36% aldehyd mrówkowy 16. 10% roztwór NaNO2 17. 1% roztwór kwasu sulfanilowego w 1M HCl 18. 10% roztwór Na2CO3 19. 1% roztwór ninhydryny w etanolu (96%) Laboratorium Biochemii, Wydział Chemiczny PW 8 Rys. 1.10. Schemat identyfikacji aminokwasów za pomocą reakcji barwnych Laboratorium Biochemii, Wydział Chemiczny PW 9 1.2.1. REAKCJE OGÓLNE AMINOKWASÓW I BIAŁEK A. Reakcja z ninhydryną Aminokwasy pod wpływem ninhydryny ulegają utlenieniu do amoniaku, dwutlenku węgla i aldehydu uboższego o jeden atom węgla. W przypadku reakcji z α-aminokwasami istotną rolę odgrywa grupa karboksylowa. Kondensacja dwóch cząsteczek ninhydryny (zredukowanej i utlenionej) z amoniakiem w środowisku o pH wyższym niż 4 daje związki o barwie fioletowoniebieskiej (purpura Rühemana), której natężenie jest proporcjonalne do zawartości azotu aminowego aminokwasu (rysunek 1.11). Rys. 1.11. Reakcja aminokwasu z ninhydryną Reakcja ta znalazła liczne zastosowania zarówno w próbach jakościowych jak i w metodach ilościowego oznaczania aminokwasów. Dodatni wynik reakcji z ninhydryną (oprócz aminokwasów, peptydów i białek) dają także sole amonowe, aminocukry i amoniak. Z tego względu oznaczana próba musi być wolna od tych związków. Wykonanie Do czterech ponumerowanych próbówek odpipetować po 1 ml buforu fosforanowego o pH 6 i dodać po 5 kropli roztworów: 1 – badany; 2 – dowolny aminokwas; 3 – białko; 4 – woda. Następnie dodać po 2 krople roztworu ninhydryny i ogrzewać przez kilka minut we wrzącej łaźni wodnej. Zanotować wyniki. B. Reakcja z kwasem azotowym(III) Aminokwasy wydzielają azot cząsteczkowy w reakcji z kwasem azotowym(III) w wyniku deaminacji (rysunek 1.12). Reakcję tę wykorzystuje się w gazometrycznej metodzie ilościowego oznaczania α-aminokwasów metodą Van Slyke’a. Laboratorium Biochemii, Wydział Chemiczny PW 10 Rys. 1.12. Schemat reakcji aminokwasów z kwasem azotowym(III) Wykonanie Do trzech ponumerowanych próbówek odpipetować po 2 ml 10% NaNO2 i 1 ml 2M CH3COOH. Następnie dodać po 0,5 ml roztworów: 1 – badanego, 2 – glicyny, 3 – wody. Dokładnie zamieszać. Wydzielanie się pęcherzyków gazu świadczy o powstawaniu azotu cząsteczkowego. C. Reakcja biuretowa (reakcja Piotrowskiego) Białka i peptydy zawierające co najmniej 2 wiązania peptydowe tworzą z jonami miedzi(II) w środowisku zasadowym połączenia kompleksowe o barwie fioletowej (Rys.1.13.), natomiast produkty kompleksowego powiązania jonów miedzi(II) z aminokwasami są niebieskie. Wyjątkiem jest histydyna, która ze względu na budowę swego łańcucha bocznego, daje produkt o barwie fioletowo-niebieskiej. Reakcja biuretowa znalazła zastosowanie w wielu metodach ilościowego oznaczania białek. Nazwa reakcji pochodzi od biuretu – najmniejszego związku dającego pozytywny wynik w tej próbie (rys. 1.14.). Rys 1.13. Kompleks jonów miedzi z białkami Rys.1.14. Biuret Wykonanie Do 0,5 ml badanego roztworu dodać 10 kropli 6 M NaOH i 2 krople 0,5% roztworu CuSO4. Przeprowadzić próby z wodą oraz roztworami histydyny, glicyny i albuminy. Zanotować wyniki. D. Wytrącanie białka za pomocą kwasu trichlorooctowego Jednym z powszechniej stosowanych odczynników odbiałczających jest kwas trichlorooctowy (TCA), który w stężeniu 2-10% powoduje wytrącenie większości białek z roztworu. Wykonanie Do 0,5 ml badanego roztworu dodać 3 krople 20% roztworu TCA. Przeprowadzić próby z roztworem albuminy i dowolnego aminokwasu. Zanotować wyniki. Laboratorium Biochemii, Wydział Chemiczny PW 11 1.2.2. REAKCJE CHARAKTERYSTYCZNE NIEKTÓRYCH AMINOKWASÓW A. Reakcja na obecność aminokwasów siarkowych Związki posiadające grupy sulfhydrylowe (utlenione lub zredukowane), jak cysteina i cystyna, ogrzewane w środowisku zasadowym ulegają rozkładowi, a powstały anion siarczkowy daje z solami ołowiu(II) czarny lub szary osad siarczku ołowiu(II). Metionina, której atom siarki uczestniczy w utworzeniu wiązania tioeterowego, nie daje tej reakcji. Schematyczny przebieg reakcji cysteiny z jonami ołowiu(II) przedstawia rysunek 1.15. Rys. 1.15. Schemat przebiegu reakcji cysteiny z jonami ołowiu(II) Wykonanie Do czterech ponumerowanych próbówek odmierzyć po 5 kropli roztworów: 1 – badanego, 2 – cystyny, 3 – dowolnego aminokwasu, 4 – białka. Następnie dodać po 10 kropli 6M NaOH i 5 kropli roztworu (CH3COO)2Pb. Próbkę ogrzewać przez kilka minut we wrzącej łaźni wodnej. Zanotować wyniki. B. Reakcja ksantoproteinowa na obecność pierścienia benzenowego Pierścienie benzenowe różnych związków ulegają nitrowaniu (rysunek 1.16) pod wpływem tzw. mieszaniny nitrującej (stężony kwas azotowy i stężony kwas siarkowy w stosunku 1:3). Produkty nitrowania mają barwę od jasnożółtej do brązowej, znacznie intensywniejszą po zalkalizowaniu próby. Reakcja zachodzi z różną szybkością i wydajnością w zależności od budowy związku i warunków reakcji. Tyrozyna, tryptofan i białka zawierające te aminokwasy nitrują się łatwo, natomiast do nitrowania fenyloalaniny niezbędne jest intensywne ogrzewanie próbki. Rys. 1.16. Schemat reakcji ksantoproteinowej z udziałem tyrozyny Laboratorium Biochemii, Wydział Chemiczny PW 12 Wykonanie Ponumerować 6 próbówek i odpipetować po 0,5 ml roztworów: 1 – badanego, 2 – tyrozyny, 3 – tryptofanu, 4 – fenyloalaniny, 5 – białka, 6 – glicyny. Dodać 2 krople stężonego kwasu azotowego i 6 kropli stężonego kwasu siarkowego. Mieszaninę ogrzewać przez kilka minut we wrzącej łaźni wodnej, a następnie ostudzić i ostrożnie dodać 2 ml 6M roztworu NaOH (wlot probówki skierować pod wyciąg). Gdyby zabarwienie nie wystąpiło, reakcję powtórzyć, ogrzewając próbę w płomieniu mikropalnika do momentu pojawienia się brązowych par tlenków azotu (kilka minut). Zanotować wyniki. C. Reakcja Millona na obecność fenoli Związki zawierające grupy fenolowe tworzą w środowisku kwasu azotowego w temperaturze 40°C czerwone kompleksy nitrofenoli z jonami rtęci(II) i rtęci(I). Jest to reakcja charakterystyczna dla monofenoli, a więc spośród aminokwasów tylko dla tyrozyny. Służy do ilościowego oznaczania tyrozyny metodą fotometryczną. Wykonanie Ponumerować cztery próbówki i dodać po 10 kropli roztworów: 1 – badanego, 2 –tyrozyny, 3 – dowolnego aminokwasu, 4 – białka. Następnie dodać po 5 kropli odczynnika Millona i ogrzać kilka minut we wrzącej łaźni wodnej. Zanotować wyniki. D. Wykrywanie układu indolowego w tryptofanie W środowisku kwaśnym tryptofan reaguje z aldehydami, między innymi z kwasem glioksalowym HOOC-CHO (rekcja Adamkiewicza-Hopkinsa (inna nazwa reakcja Hopkinsa-Colé)) lub aldehydem mrówkowym (reakcja Voisseneta), dając barwne produkty kondensacji (Rys.1.17). Wykonanie Ponumerować cztery próbówki i dodać po 10 kropli roztworów: 1 – badanego, 2 – tryptofanu, 3 – dowolnego aminokwasu, 4 – białka oraz po 4 krople roztworu kwasu glioksalowego lub aldehydu mrówkowego. Następnie wprowadzić ostrożnie po wewnętrznej ściance probówki około 0,5 ml stężonego kwasu siarkowego tak, aby nie wymieszać kwasu z roztworem wodnym. W obecności pochodnych indolu na granicy faz powstanie fioletowe zabarwienie. Zanotować wyniki. Laboratorium Biochemii, Wydział Chemiczny PW 13 Rys. 1.17. Schemat kondensacji tryptofanu z kwasem glioksalowym i aldehydem mrówkowym E. Reakcja Pauly’ego na obecność histydyny Pochodne imidazolu, jak również fenole i aminy aromatyczne, dają z solami diazoniowymi w środowisku zasadowym barwne produkty sprzęgania. Pauly zastosował w tym celu kwas diazobenzenosulfonowy, który przygotowuje się bezpośrednio przed użyciem przez diazowanie kwasu sulfanilowego kwasem azotowym(III) na zimno. Histydyna, tyrozyna i białka dają w reakcji Pauly’ego jednakowe, krwistoczerwone zabarwienie. Wykonanie Zmieszać w probówce po 2 ml roztworów kwasu sulfanilowego i azotanu(III) sodu i zawartość probówki wytrząsać przez kilka minut chłodząc ją jednocześnie pod bieżącą wodą. Następnie ponumerować pięć próbówek i odmierzyć do każdej po 5 kropli odczynnika diazowanego i kolejno po 5 kropli roztworów: 1 – badanego, 2 – histydyny, 3 – tyrozyny, 4 – dowolnego aminokwasu, 5 – białka oraz po 10 kropli roztworu Na2CO3. Zanotować wyniki. F. Reakcja na obecność argininy (Sakaguchi) Grupa guanidynowa argininy z α-naftolem w obecności utleniacza bromianu(I) sodu w środowisku zasadowym tworzy czerwono-pomarańczowy kompleks (Rys. 1.18). W razie dłuższego działania bromianu(I) sodu następuje odbarwienie roztworu, ponieważ barwny produkt ulega dalszym przemianom. Dodatek mocznika może stabilizować utworzony barwnik. Laboratorium Biochemii, Wydział Chemiczny PW 14 Rys. 1.18. Schemat reakcji argininy z α-naftolem Wykonanie Ponumerować 4 próbówki i odpipetować po 1 ml roztworów: 1 – badanego, 2 – argininy, 3dowolnego aminokwasu, 4 – białka. Następnie dodać kolejno po 0,5 ml 10% NaOH, 2 krople 1% etanolowego roztworu α-naftolu oraz 2 krople roztworu NaBrO. Wymieszać zawartość i zanotować wyniki. 1.3. PRZEDSTAWIENIE WYNIKÓW Uzyskane podczas wykonanych doświadczeń wyniki należy przedstawić w formie zestawienia (tabela 1.2). Uwaga! Wszystkie reakcje należy wykonywać dla roztworu badanego (otrzymanego od prowadzących zajęcia) oraz dla odpowiednich roztworów wzorcowych. Tabela 1.2 Reakcja Gly (Cys)2 Phe … … Badana próbka Z ninhydryną … … 1.4. PYTANIA I ZADANIA 2. Dokonaj klasyfikacji aminokwasów w oparciu o różne kryteria ich podziału: (np. białkowe/niebiałkowe, egzogenne/endogenne, budowa łańcucha bocznego). 3. Narysuj formę L i D wskazanego aminokwasu. 4. Wyjaśnij co to jest punkt izoelektryczny. Podaj przykłady aminokwasów znacznie różniących się od siebie wartościami pI. 5. Narysuj wzory aminokwasów: chiralnego i achiralnego. Podaj ich nazwy i skróty trzyliterowe. 6. Opisz reakcję wykorzystywaną w ilościowym oznaczaniu aminokwasów metodą Van Slyke’a. 7. Wyjaśnij na czym polega reakcja Pauly’ego i jakie aminokwasy można przy jej użyciu wykrywać. 8. Zaproponuj schemat postępowania służący do wykrycia tryptofanu w próbie badanej. Laboratorium Biochemii, Wydział Chemiczny PW