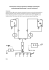TECHNIKI NISKOTEMPERATUROWE W MEDYCYNIE SEMINARIUM
Transkrypt
TECHNIKI NISKOTEMPERATUROWE W MEDYCYNIE SEMINARIUM
TECHNIKI NISKOTEMPERATUROWE W MEDYCYNIE SEMINARIUM Medyczne zastosowanie kriotechniki – do przechowywania preparatów biologicznych, w urządzeniach diagnostycznych i w kriochirurgii. Dorota Lisowska Inżynieria Mechaniczno-Medyczna II stopień, II semestr Gdańsk 2011 Spis treści 1. Wstęp ..............................................................................................................................3 2. Zastosowanie kriotechniki w urządzeniach diagnostycznych ...........................................3 3. Zastosowanie kriotechniki w kriochirurgii .......................................................................5 4. Zastosowanie kriotechniki do przechowywania preparatów biologicznych ......................9 5. Podsumowanie .............................................................................................................. 11 2 1. Wstęp Kriotechnika jest dziedziną zajmująca się zastosowaniem niskich temperatur. Wykorzystuje się ją m.in. w przemyśle, technice, nauce, ale także i w medycynie. Rozwój kriotechniki pozwolił na uzyskanie bardzo niskich temperatur, a co za tym idzie rozszerzył się zakres wykorzystania zimna i właściwości materiałów, które zmieniają się po schłodzeniu. Już 2500 lat p.n.e. Egipcjanie byli świadomi uśmierzającego działania zimna. W dzisiejszych czasach w medycynie techniki niskotemperaturowe wykorzystuje się w leczeniu operacyjnym (kriochirurgia), rehabilitacji (krioterapia), transporcie preparatów biologicznych, a także pośrednio w diagnostyce medycznej. Zimno niszczy komórki chorobowe, spowalnia reakcje biochemiczne komórek w czasie transportu narządów do transplantacji, a nawet staje się pomocny w funkcjonowaniu tomografów NMR, wywołując efekt nadprzewodnictwa. 2. Zastosowanie kriotechniki w urządzeniach diagnostycznych Urządzenia diagnostyczne pozwalają określić stan zdrowia pacjenta i ocenić zmiany chorobowe postępujące w jego organizmie. W dzisiejszych czasach aparatura jest niezbędnym elementem pracy lekarza pozwalającym na nieinwazyjne oglądanie wnętrza ciała badanej osoby. Wśród szerokiej gamy aparatury diagnostycznej znajduje się tomograf NMR. Urządzenie to przeprowadza badanie, którego wynikiem jest obraz MRI (magnetic resonance imaging) powstały za pomocą rezonansu magnetycznego (rys. 1). Zjawisko to polega na wykrywaniu protonów w badanym narządzie. Silne pole elektromagnetyczne generowane przez magnes pobudza protony do wysyłania promieniowania elektromagnetycznego. Badanie przeprowadza się w celu rozpoznania i oceny zmian rakowych, a także u osób z chorobą Alzheimera. 3 Rys. 1 Zdjęcie MRI powstałe przy użyciu tomografu NMR Źródło: Chorowski M., „Pożytki z niskich temperatur”, Dolnośląski Festiwal Nauki, Wrocław, 2005 Podstawowymi elektromagnes elementami wytwarzający budowy pole tomografu magnetyczne, są: NMR nadajnik i nadprzewodzący odbiornik fal o częstotliwościach radiowych i elektromagnesy gradientowe, ułożone wzdłuż trzech prostopadłych do siebie kierunków (rys. 2). Pacjenta umieszcza się na stole aparatu i wsuwa do komory urządzenia w stałe pole magnetyczne o wysokiej energii. Rys. 2 Schemat budowy rezonansu magnetycznego Źródło: Coyne K., „MRI: A Guided Tour”, dostępne w Internecie: http://www.magnet.fsu.edu/education/tutorials/magnetacademy/mri/ 4 Za powstanie pola magnetycznego odpowiedzialny jest elektromagnes stały lub znacznie częściej stosowany elektromagnes nadprzewodzący. Jego zadaniem jest wytwarzanie jednorodnego, silnego i stałego w czasie pola magnetycznego. Elektromagnesy nadprzewodzące wykonywane są z niobku tytanu i umieszczane w kriostacie wypełnionym ciekłym helem o temperaturze wrzenia ok. 4K. Chłodzenie elektromagnesu do tak niskiej temperatury wywołuje zjawisko nadprzewodnictwa, czyli wypchnięcie z objętości nadprzewodnika pola magnetycznego (efekt Meissnera) i zaniknięcie oporu elektrycznego. Dzięki temu otrzymuje się znacznie większe natężenie i stabilność pola magnetycznego, niż w przypadku elektromagnesu stałego. Zużycie energii na wytworzenie pola jest stosunkowo niewielkie ze względu na zerową rezystancję. Wysoka cena ciekłego helu stanowi główną wadę tego typu urządzeń. 3. Zastosowanie kriotechniki w kriochirurgii Kriochirurgia jest zabiegiem polegającym na miejscowym, kontrolowanym niszczeniu tkanek zmienionych chorobowo poprzez działanie na nie temperaturami kriogenicznymi. Za początek kriochirurgii wykorzystującej prawdziwie niskie temperatury można uznać rok 1950. W tym czasie Allington wprowadził ciekły azot do lecznictwa dermatologicznego. Mroził on zmiany skórne (brodawki, leukoplaki, naczyniaki) za pomocą bawełnianego wacika zanurzonego w roztworze ciekłego azotu. Technika ta stosowana jest w niezmieniony sposób do dnia dzisiejszego. Kriochirurgia znajduje coraz większe zastosowanie w leczeniu pacjentów. Jest alternatywą dla chirurgii klasycznej (z użyciem skalpela), a także dla zabiegów elektrokoagulacji. Wskazania do zabiegu: choroby nowotworowe – nowotwory łagodne i mało zaawansowane nowotwory złośliwe skóry, warg i błon śluzowych jamy ustnej, nowotwory złośliwe i trudnodostępne do leczenia chirurgicznego ze względu na swą lokalizację (jama ustna, gardło, noc zatoki przynosowe), guzy przysadki i szyszynki, choroby oczu – krioekstrakcja soczewki w zaćmie, przewlekłe owrzodzenie rogówki o wirusowej etiologii, 5 choroby nosa, gardła i krtani – polipy, naczyniaki nosa, jamy ustnej i krtani, brodawczaki, żylaki przegrody nosa, gardła i przełyku, choroby dróg oddechowych – wczesne okresy nowotworu złośliwego tchawicy i oskrzeli, choroby ginekologiczne – nadżerki szyjki macicy, choroby układu moczowego – brodawczaki, nowotwory złośliwe pęcherza moczowego. Wśród przeciwwskazań do operacji kriochirurgicznych znajdują się m.in.: obecność innych chorób, których zaostrzenie może być spowodowane miejscowym obniżeniem temperatury, schorzenia terapeutyczne uniemożliwiające wygojenie odczynu po zamrożeniu. W zależności od rodzaju ogniska chorobowego, operację przeprowadza się jedną z trzech powszechnie stosowanych metod. Zmiany płytkie i łagodne zamraża się przy użyciu wacika zanurzanego w ciekłym azocie o temperaturze wrzenia ok. 77K (rys. 3). Rys. 3 Metoda kriochirurgii z użyciem wacika bawełnianego. Źródło: Chorowski M., „Pożytki z niskich temperatur”, Dolnośląski Festiwal Nauki, Wrocław, 2005 Metoda ta jest prosta i tania. Nie pozwala jednak na wywołanie głębokiego mrożenia ze względu na brak możliwości utrzymania szybkiego spadku temperatury przez dłuższy okres. Istnieje ryzyko spływania ciekłego azotu na skórę, co prowadzi do uszkodzenia zdrowych tkanek i powstania mało estetycznych blizn. Niesamowicie ważny w tej metodzie jest aspekt higieniczny. Waciki powinny być wymieniane podczas leczenia każdego nowego pacjenta, a naczynia, do których odlewany jest azot powinny poddawać 6 się sterylizacji lub być przeznaczone do jednorazowego użytku. Nieprzestrzeganie ww. zasad może prowadzić do zakażeń bakteryjnych i wirusowych (m.in. wirusem HIV). Kolejnym sposobem zamrażania tkanek jest natryskiwanie ich z odległości 1cm. Metoda stosowana jest do zmian chorobowych o średnicy do 2cm. W przypadku większych ognisk, należy je podzielić na części, o średnicy nie większej od maksymalnie dopuszczalnej. W celu otrzymania lepszego efektu mrożenia, strefy sąsiadujące ze sobą powinny na siebie częściowo nachodzić. Czynnikiem chłodzącym w tym przypadku jest ciekły azot (ok. 77K) lub podtlenek azotu (184K). Kriociecz rozpyla się na zmianę chorobową, z której następnie czynnik odparowuje powodując tym samym zamrożenie komórek. Rys. 4 Krioaplikator stosowany w metodzie natryskowej. Źródło: Chorowski M., „Pożytki z niskich temperatur”, Dolnośląski Festiwal Nauki, Wrocław, 2005 W przypadku opisywanej metody istnieje duża trudność w ocenie głębokości i rzeczywistej strefy zamrożenia. Istotnym parametrem przeprowadzanego zabiegu jest natężenie strumienia gazu. Duże natężenie zwiększa głębokość zamrożenia, ale również poszerza pole mrożenia. W efekcie może dojść do niepożądanego zniszczenia tkanek zdrowych otaczających zmianę chorobową. Na skuteczność leczenia wpływa także ciągłość zabiegu. Ważne jest, aby możliwy był stały dopływ czynnika chłodzącego do krioaplikatora natryskującego (rys. 4). Kolejną znaną metodą kriochirurgii jest technika kontaktowa. Polega ona na mrożeniu zmian skórnych za pomocą krioaplikatorów zamkniętych, schładzanych przepływającym w ich wnętrzu ciągłym strumieniem gazu (rys. 5). Jako czynnik chłodzący stosuje się podtlenek azotu lub dwutlenek węgla. Metoda ta jest przeznaczona dla zmian chorobowych o różnych wielkościach – od punktowych do kilkucentymetrowych ognisk. 7 Metoda ta przewyższa metodę natryskową ze względu na lepszą możliwość oceny strefy mrożenia i jego zakres. Również precyzyjność zabiegu jest znacznie większa, dlatego zalecany jest on do zamian guzowatych, naciekających i głębokich. Wprawdzie zabieg trwa dłużej jednak charakteryzuje się większą efektywnością. Rys. 5 Krioaplikator stosowany w metodzie kontaktowej. Źródło: Chorowski M., „Pożytki z niskich temperatur”, Dolnośląski Festiwal Nauki, Wrocław, 2005 Zabieg kriochirurgiczny składa się z 3 głównych etapów: szybkie zamrażanie, podczas którego zachodzi zmiana konsystencji ogniska chorobowego do twardego lodu, odpowiednio długi czas krioaplikacji, w który narasta „kula lodowa”, powolne rozmrażanie. Szybkie zamrażanie, a następnie rozmrażanie powoduje nieodwracalne zmiany w komórce, które prowadzą do martwicy nieprawidłowej tkanki. W przeciwieństwie do innych sposobów leczenia – po rozmrożeniu tkanka swym wyglądem może wręcz nie różnić się od tkanki zdrowej, mimo że została zniszczona w sposób nieodwracalny. Ilość powtórzonych cykli zamrażanie/rozmrażanie znacząco wpływa na efektywność zabiegu. Po rozmrożeniu tkanek, w miejscu przeprowadzanego zabiegu, pojawia się zaczerwienienie związane z przekrwieniem oraz obrzęk. Po kilku godzinach pojawia się wysięk lub pęcherz utrzymujący się na powierzchni skóry prze 7-10 dni. Następnie w jego miejsce powstaje strup, który odpada samoistnie po okresie 2-3 tygodni. Kriochirurgia odznacza się szeregiem zalet dzięki czemu stała się alternatywą dla innych metod operacyjnych. Przede wszystkim jest bezbolesna (pacjent może odczuwać delikatne pieczenie), czego nie można powiedzieć o elektrokoagulacji, która wymaga 8 stosowanie miejscowego znieczulenia. Ponadto leczenie zimnem jest bezkrwawe, a blizny powstające po zabiegu są elastyczne, mniejsze i samoistnie zanikają. Metoda ta przeznaczona jest dla pacjentów bez ograniczenia wiekowego. Zabieg trwa krótko, dlatego też kriochirurgia zaliczana jest do medycyny jednego dnia. 4. Zastosowanie kriotechniki do przechowywania preparatów biologicznych Preparaty biologiczne takie jak tkanka, krew, czy narząd często podlegają transplantacji. Ratują życie ludziom z pewnymi dysfunkcjami organów, bądź uzupełniają braki krwi jakie powstały w trakcie operacji, czy też na skutek wypadku, w którym pacjent odniósł obrażenia. Odległość między dawcą a biorcą może być bardzo duża. W związku z tym preparaty biologiczne należy przetransportować w taki sposób, aby nie straciły swoich właściwości, nie doszło do niedotlenienia i zahamowania produkcji ATP przez narządy, a także nie powinny one ulec procesom biochemicznym. W celu spełnienia ww. wymagań powstały specjalne pojemniki chłodzone ciekłym azotem lub suchym lodem. Pod pojęciem suchego lodu kryje się zestalony dwutlenek węgla, otrzymywany przez rozprężanie ciekłego dwutlenku węgla i jego prasowanie. W warunkach normalnych suchy lód sublimuje (temperatura sublimacji ok. 194K), czyli przechodzi bezpośrednio ze stanu stałego do stanu gazowego. Sublimacja 1dm3 suchego lodu, w warunkach normalnych trwa około 2-3 godziny. Utrzymanie stałej niskiej temperatury otoczenia, w której byłby przechowywany pojemnik z suchym lodem dodatkowo spowolni proces przemiany fazowej. Suchy lód charakteryzuje się właściwościami bakteriostatycznymi. Obniżenie temperatury tkanek powoduje zmniejszenie ich potrzeb energetycznych. Udowodniono, że w temperaturze 5°C zapotrzebowanie na tlen stanowi nie więcej niż 5% zapotrzebowania w temperaturze 37°C. Metabolizm komórkowy w niskiej temperaturze nie zostaje całkowicie zatrzymany, mimo niedokrwienia narządu. Spowolniona zostaje szybkość reakcji chemicznych i opóźnienie śmierci komórki. Następstwa niedokrwienia łagodzone są poprzez działanie wielu różnych molekuł wchodzących w skład płynów stosowanych do schłodzenia narządów. Obniżenie temperatury poniżej -5°C negatywnie wpływa na narządy ludzkie, dlatego pojemniki do 9 ich przechowywania powinny utrzymywać temperaturę na poziomie 0-4°C lub 2-6°C w przypadku krwi pełnej konserwowanej i koncentratów krwinek czerwonych. Wyróżnia się dwa sposoby przechowywania i transportu narządów przeznaczonych do przeszczepu: metoda termostabilna – polega na zanurzeniu narządu w płynie o temperaturze pomiędzy 0 a 4°C, a następnie umieszczeniu go w naczyniu o odpowiednim rozmiarze. Naczynie zabezpiecza się podwójnym plastikowym workiem, po czym wkłada się je do izotermicznego pojemnika utrzymującego pożądaną temperaturę. Taki sposób transportu narządów jest najbardziej popularny, ze względu na niski koszt i dużą skuteczność. Przechowywanie preparatów biologicznych tą metodą nie może przekroczyć 48 godzin. Transport narządów możliwy jest dzięki pojemnikom izotermicznym typu A (przechowywanie wątroby, trzustki) lub typu B (przechowywanie palców, języka, małżowiny) Rys. 6 Pojemnik izotermiczny typu A firmy Medic Supplies Co. Rys. 7 Pojemnik izotermiczny klasy B firmy Med Technologies Źródło: http://www.dometic.com Źródło: www.medtech.com 10 metoda ciągłej perfuzji hipotermicznej – stosowana podczas transportu nerek lub serca. Wymagana jest obecność specjalnej aparatury chłodniczo-medycznej wydłużającej czas przechowywania do 72 godzin. Do transportu tego typu narządów wykorzystuje się pojemniki izotermiczno-elektroniczne, które pozwalają na stałą kontrolę parametrów. Rys. 6 Pojemnik izotermiczno-elektroniczny firmy Dometic Systems Źródło: http://www.dometic.com/enlu/Europe/Luxembourg/Medical-Systems/Cold-Chain/Transport-Boxes/ 5. Podsumowanie Kriotechnika w medycynie odnalazła szereg zastosowań. Wypiera tradycyjne metody operacji, a także wprowadza innowacyjność w tą dziedzinę nauki. Ułatwia proces diagnostyczny, etap leczenia, przeprowadzenie operacji, ale także okres rekonwalescencji staje się mniej bolesny i dokuczliwy. Zastosowanie technik niskotemperaturowych w medycynie przyniosło wiele korzyści zarówno dla pacjentów, jak i lekarzy. Możliwy stał się nawet kilkunastogodzinny transport pobranych do przeszczepu naczyń, bez naruszania ich funkcjonalności. Być może realny stanie się znany z filmów science fiction proces zamrażania człowieka w celu wprowadzenia go w stan hibernacji i powrót do życia po kilkuset latach. Pierwsze próby spełnienia tego typu wizji zostały już wprowadzone w życie, właśnie dzięki możliwości utrzymywania niskich temperatur. 11 Bibliografia: 1. Coyne K., „MRI: A Guided Tour”, dostępne w Internecie: http://www.magnet.fsu.edu/education/tutorials/magnetacademy/mri/ 2. Maj J., „Kriokoagulacja”, artykuł dostępny w Internecie: http://www.medic.hg.pl/Kriokoagulacja.pdf 3. Tobała J., Witkowska A., Olsztyński A., „Praktyczne uwagi na temat wybranych aspektów kriochirurgii zmian skórnych”, Dermatologia Kliniczna 6/2004: 29-35 4. Waszkiewicz Ł., „Przechowywanie i transport narządów ludzkich przeznaczonych do przeszczepu”, Technika Chłodnicza i Klimatyzacyjna 5/2007: 205-210 5. M. Chorowski: „Pożytki z niskich temperatur czyli dlaczego „za zimno” widzimy lepiej”, Dolnośląski Festiwal Nauki, Wrocław, 2005 6. M. Chorowski: Technologie kriogeniczne „Kriogenika w medycynie”, artykuł dostępny w Internecie: http://www.instytut22.pwr.wroc.pl/uploads/File/Kriogenika%20w%20medycynie.pdf 7. M. Jakubiak, D. Wojnowska: „Kriochirurgia i jej zastosowanie w dermatologii”, artykuł dostępny w Internecie: http://www.czytelniamedyczna.pl/1370,kriochirurgia-i-jej-zastosowanie-wdermatologii.html 8. M. Chorowski: „Kriogenika w zastosowaniach przemysłowych, medycznych i badawczych”, Chłodnictwo i Klimatyzacja 1/2005 12