Leki stosowane w chorobach układu pokarmowego
Transkrypt
Leki stosowane w chorobach układu pokarmowego
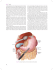
ROZDZIAŁ Leki stosowane w chorobach układu pokarmowego 62 Kenneth R. McQuaid, MD Opis przypadku Kobieta, lat 21, zgłasza się ze zdiagnozowaną chorobą Crohna. Choroba została wykryta 2 lata temu i obejmuje końcową część jelita krętego oraz część proksymalną okrężnicy, co zostało potwierdzone w kolonoskopii oraz na zdjęciu RTG jelita cienkiego. Początkowo kobieta była leczona, z dobrym skutkiem, mesalazyną oraz budezonidem, jednakże w ostatnich dwóch miesiącach nastąpił u niej nawrót choroby. Zgłasza występujące skurcze, zmęczenie, bóle brzucha, bezkrawawą biegunkę, do 10 stolców dziennie. Zaobserwowała także spadek masy ciała prawie o 7 kg. Kobieta wcześniej nie chorowała i nie Wprowadzenie Wiele grup leków omawianych w tej książce ma ogromne zastosowanie w leczeniu chorób układu pokarmowego oraz innych narządów ciała. Grupy leków stosowane prawie wyłącznie w leczeniu chorób jelit zostały omówione w poniższym rozdziale zgodnie z ich terapeutycznym zastosowaniem. Leki stosowane w zaburzeniach kwasowo-peptycznych Do schorzeń układu pokarmowego zalicza się chorobę refluksową przełyku, chorobę wrzodową (żołądka 1234 przechodziła poważnych zabiegów chirurgicznych. Obecnie przyjmowane przez nią leki to mesalazyna w dawce 2,4 g/d oraz budezonid w dawce 9 mg/d. Wygląda na wychudzoną i wycieńczoną. Badanie brzucha wykazuje tkliwość bez obrony mięśniowej w prawej dolnej części brzucha; bez wyczuwalnych oporów patologicznych. Badanie per rectum bezbolesne, nie stwierdzono szczelin ani przetok. Wyniki badań laboratoryjnych wskazują na anemię oraz podwyższony poziom białka C-reaktywnego (CRP). Jakie są możliwości szybkiego opanowania objawów choroby? Jakie są możliwości długoterminowego leczenia? i dwunastnicy) oraz związane ze stresem uszkodzenie błony śluzowej. We wszystkich tych przypadkach nadżerki błony śluzowej oraz owrzodzenia powstają, kiedy substancje żrące, takie jak kwas, pepsyna czy żółć, biorą górę nad mechanizmami obronnymi błony śluzowej przewodu pokarmowego, takimi jak: wydzielanie śluzu i wodorowęglanów, prostaglandyn, przepływ krwi oraz procesy naprawy i regeneracji uszkodzonych komórek. Ponad 90% przypadków choroby wrzodowej żołądka jest związanych z infekcją Helicobacter pylori oraz przyjmowaniem niesteroidowych leków przeciwzapalnych (NLPZ). Leki stosowane w leczeniu zaburzeń trawiennych dzielą się na dwie grupy: środki zmniejszające kwasowość soku żołądkowego oraz wspomagające ochronę błony śluzowej. Rozdział 62 • Leki stosowane w chorobach układu pokarmowego 1235 Wpust żołądka Dno żołądka Komórka przedzwojowa nerwu błędnego Naczynie krwionośne dna żołądka Gastryna + Komórka przedzwojowa nerwu błędnego G/CCK-B-R + M3-R Histamina Komórka ECL Naczynie krwionośne wpustu żołądka ACh + – + ACh-R Histamina + Gastryna + M3-R H2-R G/CCK-B-R GRP-R Gastryna Komórka okładzinowa Somatostatyna-R Somatostatyna – H+/K+ Komórka G Komórka D + K+ K+ H+ H + H + H+ + Peptydy trawienne ATP-aza Kwas solny światła żołądka H+ H+ Kwas solny światła żołądka Światło żołądka okolicy wpustu Światło żołądka okolicy dna RYCINA 62-1. Schematyczny model fizjologicznej kontroli wydzielania jonów wodorowych (kwasu) przez komórki okładzinowe gruczołów dna żołądka. Komórki okładzinowe są pobudzane do wydzielania kwasów (H+) przez gastrynę (czynną na receptorze gastryny CCK-B), acetylocholinę (receptor M3) oraz histaminę (receptor H2). Kwas wydzielany jest poprzez błonę kanalików wydzielniczych komórki okładzinowej za pomocą pompy protonowej adenozynotrifosfatazy (ATP-azy) do światła żołądka. Gastryna wydzielana jest przez komórki G do naczyń krwionośnych w odpowiedzi na peptydy w świetle naczynia. Wewnątrz trzonu żołądka gastryna przemieszcza się z naczyń krwionośnych do tkanki podśluzówkowej gruczołów właściwych żołądka, gdzie wiąże się z receptorami CCK-B na komórkach okładzinowych oraz komórkach ECL żołądka. Nerw błędny pobudza neurony zazwojowe jelitowego układu nerwowego do wydzielania acetylocholiny (receptor M3), która wiąże się z receptorami M3 na komórkach okładzinowych i komórkach ECL. Komórki ECL pobudzone przez gastrynę (receptor CCK-B) bądź acetylocholinę (receptor M3) stymulują uwalnianie histaminy. Wewnątrz jamy odźwiernikowej pobudzanie nerwu błędnego zazwojowych neuronów jelitowych zwiększa wydzielanie gastryny bezpośrednio poprzez stymulację komórek G (za pomocą peptydu GRP), a bezpośrednio poprzez zatrzymanie wydzielania somatostatyny z komórek D. Wydzielanie kwasu musi zostać w końcu zatrzymane. Komórki D są pobudzane do uwalniania somatostatyny poprzez wzrost stężenia H+ w świetle naczyń oraz poprzez CCK uwalniany do krwiobiegu przez dwunastnicze komórki I w odpowiedzi na proteiny i tłuszcze (niepokazane). Wiązanie somatostatyny z receptorami na przyległych komórkach G zatrzymuje dalsze wydzielanie gastryny, ATP-azy, pompy protonowej H+/K+-ATP-azy, CCK, cholecystokininy, M3 oraz receptorów muskarynowych. ŚRODKI REDUKUJĄCE KWASOWOŚĆ SOKU ŻOŁĄDKOWEGO Fizjologia wydzielania kwasu żołądkowego Komórka okładzinowa zawiera receptory gastryny (CCK-B), histaminy (H2) oraz acetylocholiny (receptory muskarynowe, M3) (ryc. 62-1). Wiązanie acetylocholiny (z nerwów błędnych zazwojowych) lub gastryny (uwalniana do krwi przez zatokowe komórki G) z receptorami komórki okładzinowej powoduje wzrost wapnia cytozolowego, co z kolei pobudza kinazy proteinowe, które to stymulują wydzielanie kwasu z H+/ K+-adenozynotrifosfatazy – ATP-azy) (pompa protonowa) na powierzchni kanalikowej. W bliskim sąsiedztwie z komórkami okładzinowymi znajdują się komórki wewnątrzwydzielnicze jelita zwane komórkami chromochłonnymi [enterochromaffin-like (ECL) cells]. Komórki ECL również mają receptory 1236 gastryny i acetylocholiny pobudzające wydzielanie histaminy. Histamina wiąże się z receptorem H2 na komórce okładzinowej, co skutkuje aktywacją cyklazy adenylanowej, a co za tym idzie – wzrostem komórkowego cyklicznego adenozynomonofosforanu (cyclic adenosine monophosphate – cAMP) oraz aktywacją kinaz białkowych, które to pobudzają wydzielanie kwasu poprzez H+/K+-ATP-azy. Uważa się, że u ludzi największy wpływ gastryny na wydzielanie kwasu uwidacznia się pośrednio poprzez uwalnianie histaminy z komórek ECL, bardziej niż poprzez bezpośrednią stymulację komórek okładzinowych. Acetylocholina natomiast pomaga w skutecznej bezpośredniej stymulacji komórek okładzinowych. Środki zobojętniające kwas Środki zobojętniające kwas były stosowane przez wieki w leczeniu pacjentów z dyspepsją i zaburzeniami trawiennymi. Były one podstawą leczenia zaburzeń trawiennych do czasu pojawienia się blokerów receptora H2 oraz czynników spowalniających pompę protonową. Są one nadal powszechnie stosowane przez pacjentów jako środki dostępne bez recepty w leczeniu powracającej zgagi i dyspepsji. Środki zobojętniające kwas są słabymi zasadami, które wchodzą w reakcję z kwasem solnym w celu utworzenia soli i wody. Ich głównym mechanizmem działania jest redukcja kwasowości soków żołądkowych. Po posiłku wydziela się około 45 mEq/godz. kwasu solnego. Pojedyncza dawka wielkości 156 mEq środka zobojętniającego kwas podana 1 godzinę po posiłku skutecznie neutralizuje kwas na 2 godziny. Jednakże zdolność do neutralizacji kwasu różni się znacznie w zależności od postaci leku. Zależy ona od tempa jego rozpuszczania (tabletka vs płynny środek), rozpuszczalności w wodzie, tempa reakcji z kwasami, a także tempa opróżniania żołądka. Wodorowęglan sodu (np. soda oczyszczona, Alka Seltzer) wchodzi gwałtownie w reakcje z kwasem solnym, tworząc dwutlenek węgla i chlorek sodu. Powstawanie dwutlenku węgla powoduje wzdęcia oraz odbijanie. Nieprzereagowana zasada jest łatwo wchłaniana, co może potencjalnie spowodować zasadowicę metaboliczną w przypadku podania dużej dawki lub kiedy pacjent cierpi na niewydolność nerek. Wchłanianie chlorku sodu może zaostrzyć zatrzymywanie płynów u pacjentów z niewydolnością serca, nadciśnieniem tętniczym i niewydolnością nerek. Węglan wapnia (np. Tum, Os-Cal) jest słabiej rozpuszczalny i wolniej niż wodorowęglan sodu wchodzi w reakcję z HCl, formując dwutlenek węgla i chlorek wapnia (CaCl2). Tak jak wodorowęglan sodu, chlorek wapnia może powodować odbijanie i zasadowicę metaboliczną. Węglan wapnia stosowany jest przy wielu innych schorzeniach ze względu na jego właściwości zobojętniające kwas (rozdz. 42). Zbyt duże dawki zarówno wodorowęglanu sodu, jak i węglanu wapnia w połączeniu z produktami mlecznymi zawierającymi wapń mogą CZĘŚĆ X • Zagadnienia wybrane spowodować hiperkalcemię, niewydolność nerek oraz zasadowicę metaboliczną (zespół Burnetta). Związki zawierające wodorotlenek magnezu lub wodorotlenek glinu powoli wchodzą w reakcję z HCl, tworząc chlorek magnezu lub chlorek glinu oraz wodę. Ponieważ nie są przy tym wytwarzane żadne gazy, nie ma efektu w postaci odbijania. W tym przypadku również zasadowica metaboliczna występuje rzadko ze względu na skuteczność neutralizacji reakcji. Ponieważ niewchłonięte sole magnezowe mogą spowodować biegunkę osmotyczną, a sole glinu – zaparcia, środki te są zwykle podawane razem (np. Gelusil, Maalox, Mylanta) w celu zminimalizowania wpływu tych substancji na funkcję jelit. Zarówno magnez, jak i glin są wchłaniane i wydalane przez nerki. W związku z powyższym, pacjenci z niewydolnością nerek nie powinni przyjmować ich długoterminowo. Wszystkie środki zobojętniające kwas mogą wpływać na wchłanianie innych leków poprzez ich wiązanie (redukcja wchłaniania) lub poprzez podnoszenie pH w żołądku, co wiąże się ze zmianą rozpuszczalności leku (zwłaszcza środków słabo zasadowych bądź kwasowych). Dlatego też środki zobojętniające kwas nie powinny być podawane w ciągu dwóch godzin od przyjęcia tetracykliny, fluorochinolonu, itrakonazolu czy żelaza. Blokery receptora H2 Od ich wprowadzenia w 1970 roku aż do wczesnych lat 90. XX w. antagoniści receptora H2 (zwani powszechnie blokerami H2) byli najczęściej przepisywanymi lekami na świecie (patrz: „Zastosowanie kliniczne”). Wraz z odkryciem roli bakterii H. pylori w chorobie wrzodowej (która może być leczona odpowiednio dobraną terapią antybakteryjną) oraz pojawieniem się inhibitorów pompy protonowej częstotliwość stosowania blokerów H2 znacznie zmalała. Budowa chemiczna i farmakokinetyka Cztery blokery H2 są obecnie w użyciu klinicznym: cymetydyna, ranitydyna, famotydyna i nizatydyna. Wszystkie cztery substancje są szybko wchłaniane przez jelita. Cymetydyna, ranitydyna i famotydyna podlegają efektowi pierwszego przejścia przez wątrobę, co skutkuje biodostępnością na poziomie 50%. Nizatydyna w niskim stopniu podlega efektowi pierwszego przejścia. Czas połowicznego rozkładu tych czterech środków waha się od 1,1 do 4 godzin. Czas działania natomiast zależy od wielkości podanej dawki (tab. 62-1). Blokery H2 są usuwane w procesach metabolizmu wątrobowego, filtracji kłębuszkowej i sekrecji kanalikowej. Zmniejszenie dawki jest wymagane zarówno u pacjentów z umiarkowaną, jak i ciężką niewydolnością nerek (oraz możliwą ciężką niewydolnością wątroby). U osób starszych występuje zmniejszenie zdolności eliminacji leku do 50%, jak również wyraźna redukcja zdolności rozprowadzania leku.