Wyróżniona praca w formacie pdf
Transkrypt
Wyróżniona praca w formacie pdf
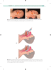
STRESZCZENIE Mikroorganizmy zimnolubne zwane psychrofilami mogą być źródłem enzymów o unikalnych właściwościach hydrolaz (β-galaktozydazy, β-glukozydazy, lipazy, esterazy i proteazy) i mogą znaleźć zastosowanie w biotechnologii i przemyśle spożywczym, tam gdzie technologia wymaga niskich temperatur. Celem pracy było wyizolowanie drożdżaków psychrofilnych z wód Morza Bałtyckiego, które wytwarzałyby naturalne enzymy wykazujące aktywność w niskich temperaturach. Pod uwagę brałam dwie grupy enzymów: proteazy i lipazy. Materiałem badawczym były próbki wody pobrane z Morza Bałtyckiego z okolic Szklanej Huty, które testowałam w kierunku określenia ich temperatury optymalnej (15°C), wzrostu w niskich temperaturach (6°C) oraz braku wzrostu w temperaturze 37°C. Wyhodowałam 15 kolonii drożdżaków, które spełniały te kryteria, co może świadczyć o ich przynależności do grupy psychrofilnych mikroorganizmów. Aktywności lipolityczną i proteolityczną sprawdziłam na podłożu stałym wzbogaconym odpowiednio w tributyrynę i mleko. Uzyskałam dwa szczepy drożdżaków, które wykazywały aktywność proteolityczną i jeden szczep wykazujący aktywność lipolityczną. Szczepy te mogą stać się punktem wyjścia do dalszych badań nad ich przydatnością w biotechnologii. WSTĘP Psychrofile są to mikroorganizmy (bakterie, grzyby, glony) ekstremofilne rosnące w skrajnie niskich temperaturach środowiska. Jako organizmy zimnolubne posiadają optymalną temperaturę wzrostu 15°C i niższą, a ich maksymalna temperatura nie przekracza 20°C, natomiast minimalna to 0°C i niżej. Organizmy zimnolubne spotykane są w rozmaitych ekosystemach, głównie w lodowcach, śniegach, wiecznych zmarzlinach, wysokogórskich glebach oraz w zimnych wodach morskich i na dnie oceanów. Mogą one również występować na terenach, gdzie temperatura obniża się tylko lokalnie lub okresowo. Do takich miejsc zaliczane jest m.in. Morze Bałtyckie, gdzie temperatura, w zależności od pory roku waha się od 0 do 2 °C w zimie i od 9 do 22 °C w lecie. Organizmy zimnolubne wytworzyły liczne molekularne mechanizmy adaptacyjne, które ułatwiają im przeżycie w skrajnie niskich temperaturach. Produkują one enzymy wykazujące aktywność w niskich temperaturach z powodu większej liczby α-helis, które odpowiedzialne są za ich elastyczność, charakteryzują się większą polarnością i mniejszą zawartością aminokwasów hydrofobowych. Niektóre z najlepiej zaadaptowanych do zimna psychrofili posiadają zdolność do wytwarzania małych, unikatowych białek, tzw. białek nukleacyjnych lodu, które działają jako zarodki kryształów lodu, wiążąc na swojej powierzchni cząsteczki wody. Powstające w ten sposób kryształy, są zbyt duże, aby mogły wniknąć do wnętrza komórki i spowodować jej destrukcję. Kolejnym przystosowaniem do niskiej temperatury jest obecność białek szoku zimna, niezbędnych w prawidłowym przebiegu transkrypcji i translacji w warunkach niskiej temperatury. Organizmy psychrofilne i psychrotolerancyjne ze względu na swoje przystosowania molekularne wykazują szereg specyficznych właściwości, które mogą być przydatne w biotechnologii, przemyśle oraz ochronie środowiska. Do najcenniejszych składników tych organizmów należą enzymy zwane psychrozymami. MATERIAŁ I METODY: Materiał 1. Materiałem badawczym była próbka wody pobrana z Morza Bałtyckiego 24 stycznia 2013 roku w miejscowości Szklana Huta (województwo kujawsko-pomorskie, współrzędne geograficzne 51.9833 °N 20.4000 °E) i przechowywana była w lodówce w temperaturze 4°C. 2. Materiały podstawowe i sprzęt: jałowe płytki Petriego, eza, głaszczka szklana, pipety automatyczne, probówki typu Eppendorf, probówki wirownicze, cieplarki, komora laminarna, mikroskop świetlny, wirówka. 3. Podłoża hodowlane: komercyjnie dostępne, gotowe podłoża do hodowli mikroorganizmów: - podłoże LA (skład: pepton K, ekstrakt drożdżowy, agar, NaCl), podłoże Sabourauda – podłoże stosowane do hodowli grzybów (skład: agar, woda destylowana, glukoza, pepton K). Do pożywki były dodawane antybiotyki: ampicylina i chloramfenikol w celu zahamowania wzrostu bakterii, które mogłyby utrudnić selekcję drożdżaków. Tak przygotowane pożywki wylewałam na płytki Petriego i podsuszałam w cieplarce w temperaturze 37°C. Metody: 1. Izolacja mikroorganizmów z próbek wody W wirówce odwirowałam 2 razy po 100 ml wody pobranej z Morza Bałtyckiego. Wodę dekantowałam, pozostawiając w każdej probówce tylko około 2 ml. Całą objętość próby wysiewałam na 40 płytek w ilości 100µl na każdą płytkę i wcierałam jałową głaszczką. Użyłam podłoża Sabourauda z antybiotykami ampicyliną i chloramfenikolem jednocześnie w celu zahamowania wzrostu bakterii. Posiane próbki inkubowałam w cieplarce przez 3 dni w temperaturze 15°C. Czystość szczepów uzyskiwałam metodą posiewu redukcyjnego. Następnie z pojedynczych kolonii zrobiłam niebarwione preparaty mikroskopowe. Preparaty drożdży oglądałam w mikroskopie świetlnym pod powiększeniem 10x10 oraz 10x40. 2. Badanie temperatury wzrostu dla wyizolowanych drożdżaków Aby określić czy badane organizmy należą do grupy zimnolubnych, zbadałam optymalną temperaturę ich wzrostu. Każdą z otrzymanych kolonii przepikowałam na 3 płytki (posiew kreskowy). Jedna płytka była inkubowana w 6°C, druga w 15°C a trzecia w 37°C. Hodowla w 37°C została przeprowadzona w celu wyeliminowania mezofilnych i potencjalnie patogennych mikroorganizmów. 3. Badanie aktywności enzymatycznych wyizolowanych szczepów drożdży - aktywność proteolityczna Wyjałowione i ostudzone do temperatury 50°C podłoże LA mieszałam z odtłuszczonym mlekiem (0% tłuszczu) w stosunku 3:1 i wylewałam na płytki Petriego. Płytki podzieliłam na sektory, na które posiewałam kreskowo wyizolowane wcześniej szczepy drożdżaków. Posiewy inkubowałam w temperaturze 15°C, wyniki odczytywałam po 2,3,4 i 5 dniach. - aktywność lipolityczna Aktywność lipolityczną wyizolowanych szczepów grzybów badałam również na podłożu LA z dodatkiem tributyryny. W tym celu przygotowałam dwuwarstwowe podłoże na płytkach Petriego. Dolna warstwa składała się z podłoża LA, a górna z podłoża LA z 1% tributyryną. Następnie płytki podzieliłam na sektory, każdemu sektorowi przypisałam numer odpowiedniego szczepu i wykonałam posiewy kreskowe. Płytki inkubowałam w temperaturze 15°C, odczytując wyniki po 2,3,4 i 5 dniach. WYNIKI 1. Izolacja mikroorganizmów z próbek wody Na podłożu Sabourauda z jednoczesnym dodatkiem ampicyliny oraz chloramfeikolu uzyskałam 33 kolonie, których czystość sprawdziłam stosując metodę posiewu redukcyjnego. W wyniku makroskopowania zauważyłam, że kolonie różnią się morfologicznie barwą i strukturą Ryc.1 Posiew redukcyjny na podłożu Sabourauda z jednoczesnym dodatkiem ampicyliny i chloramfenikolu dwóch z 15 otrzymanych kolonii drożdżaków. 2. Badanie temperatury wzrostu dla wyizolowanych drożdżaków Spośród 33, tylko 15 izolatów wykazywało wzrost w 6°C i 15°C, nie wykazując wzrostu w temperaturze 37°C i tylko tymi szczepami zajmowałam się dalej. Wzrost w 15°C był dobrze widoczny po 2-3 dniach inkubacji (Ryc.2) , w 6°C wzrost był mniej wydajny, ale wyraźny (Ryc.3). Dla tej temperatury hodowlę przedłużyłam do 4 dni. Ryc.2 Wyniki posiewu kreskowego po 3 dniach inkubacji w temperaturze 15°C Ryc.3 Wyniki posiewu kreskowego po 5 dniach inkubacji w temperaturze 6°C Ryc. 4 Wynik posiewu kreskowego po 7 dniach inkubacji w temperaturze 37°C 3. Badanie aktywności enzymatycznych wyizolowanych szczepów drożdży - aktywność proteolityczna Aktywność proteolityczną wykazały jedynie szczepy 2 i 4, co można zaobserwować jako odbarwienie na pożywce z mleka. Dookoła posiewu pożywka stała się przezroczysta. Pozostałe szczepy nie wykazały aktywności proteolitycznej w temperaturze 15°C (ryc.6, tabela1). Ryc.5 Wyniki testu na aktywność proteolityczną wszystkich kolonii po 6 dniach inkubacji w 15°C - aktywność lipolityczna Aktywność lipolityczną na pożywce z tributyryną wykazał tylko jeden szczep nr 2. Obserwujemy delikatne przejaśnienie wokół kolonii (zaznaczone strzałką ryc.7) + Ryc.7 Wynik testu na aktywność lipolityczną na podłożu z tributyryną. Numer S1 Szczepu Aktywność Proteolityczna Aktywność Lipolityczna Ryc.6 Wyniki testu na aktywność proteolityczną kolonii u których zaobserwowano zmiany. Strzałkami zaznaczono strefę proteolizy. S2 S3 S4 S5 S6 S7 S8 S9 S10 S11 S12 S13 S14 S15 + - + - - - - - - - - - - - + - - - - - - - - - - - - - Tabela 1. Wyniki obserwacji aktywności proteolitycznych i lipolitycznych drożdżaków wyizolowanych z próbki wody Morza Bałtyckiego w temperaturze 15°C. „+” – wykazuje aktywność „-” – nie wykazuje aktywności Dyskusja Od wielu lat poszukuje się biokatalizatorów przydatnych w przemyśle spożywczym, chemicznym i medycynie. Mogą być nimi enzymy produkowane przez drobnoustroje, m.in. lipazy i proteazy. Swoją pracę skupiłam na poszukiwaniu tych dwóch grup enzymów z organizmów zaadaptowanych do życia w niskich temperaturach. Wykazując aktywność enzymatyczną w niskich temperaturach, mogą one usprawnić proces technologicznego ich pozyskiwania oraz znaleźć zastosowanie tam, gdzie wskazane jest zastosowanie niskich temperatur. Psychrozymy, jako enzymy działające w niskich temperaturach, mogą być wykorzystane w przemyśle chemicznym do produkcji proszków do prania, które nie wymagają stosowania wysokiej temperatury i nie narażają tym samym tkanin na zniszczenie, w przemyśle spożywczym w serowarstwie (częściowa hydroliza białek poprawia smak i zapach produktów), w przemyśle mięsnym (kruszenie, inaczej tenderyzacja mięsa oraz poprawa smaku mięsa mrożonego). Enzymy zaadaptowane do zimna znalazły również zastosowanie do produkcji antybiotyków modyfikowanych enzymatycznie zależnych od temperatury (6-9 °C). Pierwszym etapem mojej pracy była selekcja zimnolubnych, środowiskowych mikroorganizmów drożdżowych z wód Morza Bałtyckiego, które zaliczane jest do zimnych zbiorników wodnych. Próbki wody pobierałam z okolic Szklanej Huty. Wybrałam taką lokalizację, ponieważ są to tereny niemal niezamieszkałe i pozbawione zanieczyszczeń przemysłowych i komunalnych. Postanowiłam wyizolować drożdżaki środowiskowe, ponieważ są one w przeważającej części niepatogenne (tym samym bezpieczniejsze), charakteryzują się szybkim wzrostem (możliwość uzyskania dużej biomasy w krótkim czasie), posiadają niskie wymagania pokarmowe (w przyszłości niski koszt podłóż hodowlanych). Nie posiadają również toksycznych metabolitów i są odporne na zakażenia wirusowe (w odróżnieniu od bakterii). Drożdżaki ponadto nie ulegają tak szybko jak bakterie zmienności genetycznej (przez co zachowują stabilność genetyczną danej cechy). Aby zwiększyć prawdopodobieństwo wyizolowania drożdżaków z wody, próbkę zagęściłam poprzez zwirowanie jej do małej objętości. Następnie dokonałam posiewów na stałe podłoże Sabourauda z dodatkiem antybiotyków, w celu eliminacji zimnolubnych bakterii, których w wodzie morskiej jest bardzo dużo (zwłaszcza bakterii należących do rodzaju Pseudomonas i Proteus). Po inkubacji w temperaturze ok. 15°C uzyskałam 33 kolonie i dla dalszej ich weryfikacji wykonałam posiewy redukcyjne (w celu uzyskania czystych kultur) oraz wykonałam preparaty mikroskopowe. Po obejrzeniu ich w mikroskopie świetlnym potwierdziłam ich przynależność do grzybów drożdżowych. Są to organizmy jednokomórkowe z wyraźnie widocznym jądrem i wakuolą. Do przygotowania preparatów drożdżowych nie jest wymagane stosowanie barwników. Następnie przetestowałam zdolność do wzrostu w trzech temperaturach: 6C°, 15C° i 37 C°. Założyłam, że drożdżaki psychrofilne nie będą rosły w 37 C° zaś temperatura 15 °C powinna być ich temperaturą optymalną. Na tej podstawie wyizolowałam pożądane szczepy. Wyniki badań były powtórzone dwukrotnie. Uznałam, że te szczepy mogą zostać poddane dalszej charakterystyce na podłożach stałych z dodatkiem odpowiedniego indykatora w celu wykrywania produkcji zewnątrzkomórkowych proteaz i lipaz. Umożliwiają one rozkład substancji na zewnątrz komórki, która pobiera nadtrawione cząsteczki ze środowiska. Do badania właściwości proteolitycznych zastosowałam podłoże LA z mlekiem odtłuszczonym (0% tłuszczu, ponieważ badałam drożdżaki wyłącznie pod kątem trawienia proteolitycznego). Podłoże LA nie zawierało glukozy, która jest źródłem węgla dla drożdżaków jak np. w podłożu Sabourauda, przez to cały ich metabolizm był nastawiony na wykorzystanie węgla pochodzącego z białka. Strefa przejaśnienia wokół linii posiewu świadczyła o wyższej aktywności proteolitycznej drożdżaka. Strefa proteolizy z każdym dniem powiększała się. Oznacza to, że drożdżaki wytwarzają enzym – proteazę, która trawi wiązanie peptydowe, doprowadzając do rozpadu białka w mleku. Produkcja lipaz jest wyznaczana poprzez pojawienie się strefy przejaśnienia wokół kolonii rosnących na płytkach z tributyryną. Tylko jeden szczep posiadał zdolność do hydrolizy tego substratu, szczep nr 2. (Ryc. 7). Co jest ciekawe, ten sam szczep posiadał również aktywność proteolityczną. Obie jednak aktywności dla tego szczepu były dosyć słabo wyrażane. Przeprowadzone przeze mnie badania wymagają dalszej kontynuacji. Szczepy powinny zostać również posiane na podłoża minimalne w celu określenia ich warunków pokarmowych, aby określić ich przydatność technologiczną. W celu dokonania dalszej charakterystyki szczepów wykazujących właściwości proteolityczne i lipolityczne, należałoby dokonać ich klasyfikacji w oparciu o inne cechy biochemiczne oraz zbadać ich materiał genetyczny. Praca doświadczalna była prowadzona we współpracy z Katedrą Mikrobiologii Wydziału Chemicznego Politechniki Gdańskiej. Podczas wykonywania badań prze cały czas przestrzegałam zasad bezpieczeństwa pracy, ubierając fartuchy ochronne oraz rękawiczki jednorazowe. Bibliografia 1. Gerday, C. (2000, March). Cold-adapted enzymes: from fundamentals to biotechnology. Trends Biotechnology, strony 103-107. 2. Håkanson, R. L. (1991). Środowisko Morza Bałtyckiego, zeszyt 1. Charakterystyka fizycznogeograficzna zlewiska Morza Bałtyckiego. Uppsala, Szwecja. 3. Mrozowska, J. red. (1999). Laboratorium z mikrobiologii ogólnej i środowiskowej. Gliwice: Wydawnictwo Politechniki Śląskiej, strony 76-96. 4. Miteva, V. Margesin, R (2010) Diversity and ecology of psychrophilic microorganisms. Research in Microbiology, strony 346-361. 5. Brock, T.D. Madigan, M.T. Martinko, J.M. Parker, J. (2000). Biology od Microorganisms. Southern Illinois University Carbondale: Prentice Hall International, Inc. 6. Turkiewicz, M. (2006). Drobnoustroje psychrofilne i ich biotechnologiczny potencjał. Kosmos, 55(4), strony 307-320.