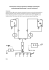HEMODIALIZA – SZTUCZNA NERKA
Transkrypt
HEMODIALIZA – SZTUCZNA NERKA
Ćwiczenie laboratoryjne nr 5 i 6: HEMODIALIZA – SZTUCZNA NERKA WSTĘP TEORETYCZNY A. ZAGADNIENIA DO PRZYGOTOWANIA 1. 2. 3. 4. 5. 6. 7. 8. Funkcje zdrowych nerek Zasada dializy pozaustrojowej. Zasada dializy otrzewnowej. Ogólny schemat aparatu „sztucznej nerki” Blokowy schemat obiegu płynu dializacyjnego. Budowa modułu krwi. Budowa i zasada działania czujników w aparacie. Przebieg zabiegu hemodializy. B. LITERATURA PODSTAWOWA 1. Augustyniak Piotr – wykład. 2. http://home.agh.edu.pl/~asior/stud/doc/Hemodializa_15.pdf UZUPEŁNIAJĄCA 3. Daugirdas J.T, Blake P.G., Ing T.S., red. wyd. pol. Andrzej Książek: Podręcznik dializoterapii. Czelej, 2008. 4. Korohoda P., Tadeusiewicz R.: Compression of sequences of thermograms documenting dynamic forearm studies in hemodialyzed patients. Thermology International, Vol 13, no. 2, s. 73–74, 2003. 5. Korohoda P., Pietrzyk J.A., Sułowicz W.: Modelowanie hemodializoterapii. Część I: Model dwuprzedziałowy, Część II: Model przepływowy. Nefrol. Dial. Pol., 8, 45-59, 2004. 6. Rutkowski B.: Leczenie nerkozastępcze. Poradnik dla pacjentów i ich rodzin. Via Medica, 2010. 7. Villee C. A.: Biologia. Wyd. VIII, Warszawa 1987. 8. Ziółko M., Pietrzyk J., Grabska-Chrząstowska J.: Accuracy of hemodialysis modeling. Kidney International, Vol. 57, pp.1152-1163, 2000. C. WPROWADZENIE TEORETYCZNE DIALIZA CZYLI PROTEZOWANIE FUNKCJI NEREK Działanie nerki człowieka W organizmie człowieka ważną rolę odgrywają nerki [5]. Jest to parzysty organ w kształcie fasoli, stosunkowo niewielki (średnio: 12 cm x 6 cm) umiejscowiony w tylnej części jamy brzusznej, w przestrzeni zaotrzewnowej. Nerki otrzymują krew z tętnic nerkowych i oddają ją do żył nerkowych. Każda nerka wydala mocz do miedniczki nerkowej, skąd spływa do moczowodu i dalej wpada do pęcherza moczowego (rys. 1a). a) b) Rys. 1. Budowa a) nerki; b) nefronu. Głównym elementem wykonawczym nerki są nefrony (rys. 1b), jednostki filtrujące krew z tętniczek nerkowych. Jedna nerka dysponuje około milionem elementów i z tego wynika, że tętnica nerkowa musi rozgałęziać się na tyle samo naczyń (tętniczek doprowadzających) wprowadzających krew do pojedynczej struktury nerkowej. Najistotniejszy proces zachodzi w elemencie nefronu zwanym torebką Bowmana: krew z tętniczki doprowadzającej wpływa do półprzepuszczalnej struktury zwanej kłębkiem, składającej się z 4 do 6 filtrów i opuszcza ją poprzez tętniczkę odprowadzająca, pozbawiona części swojej objętości. Większość cząstek o średnicy mniejszej niż pory w błonie kłębka przenika na zewnątrz kłębka, do torebki Bowmana i z częścią wody z krwi wędruje przez kolejne cewki do cewki zbiorczej. Szacuje się, że ta objętość (zwana przesączem kłębkowym lub moczem pierwotnym) w ciągu doby wynosi około 180 l. W trakcie przemieszczania się część wody i składników potrzebnych organizmowi, poprzez sieć naczyń krwionośnych, wraca do ustroju. W efekcie, na dobę nerki usuwają około 1,5 l płynu, zwanym moczem ostatecznym. Przez pory w kłębku nie przechodzą m.in. krwinki, płytki krwi, białka i witaminy. Średnie dobowe wydalanie ważniejszych składników podaje tabela (tab. 1). Tab. 1. Średnie wydalanie dobowe najważniejszych produktów przemiany materii. SUBSTANCJA WYDALANIE DOBOWE woda 1500 ml chlorek sodu 8 – 15 g potas 2,5 g mocznik 15 – 20 g kwas moczowy 0,5 - 0,8 g kreatynina 1-2 g amoniak 0,7 g Funkcje zdrowych nerek Główne funkcje nerek to funkcja wydalnicza i wewnątrzwydzielnicza. W szczególności praca nerek to: usuwanie z moczem szkodliwych produktów przemiany materii; zatrzymywanie składników niezbędnych dla organizmu, które ulegają przefiltrowaniu do moczu pierwotnego (reabsorbcja); regulacja objętości płynów ustrojowych; wydalanie leków i trucizn rozpuszczalnych w wodzie (barbiturany, salicylany, preparaty naparstnicy i większość antybiotyków); wpływ na ciśnienie tętnicze krwi (układ renina – angiotensyna - aldosteron); wpływ na prawidłową erytropoezę (produkcja erytropoetyny); wpływ na równowagę kwasowo-zasadową (pH krwi), dzięki możliwości zakwaszania moczu; wpływ na układ kostny przez produkcję aktywnych postaci witaminy D 3. Przyczyny i objawy chorób nerek Najczęstszymi przyczynami chorób nerek są choroby kłębuszków nerkowych, nefropatia cukrzycowa, choroby naczyń, choroby cewkowo-śródmiąższowe, choroby z towarzyszącymi torbielami nerek i inne. Duża część tych schorzeń ma podłoże genetycznie. Przyszli pacjenci klinik Nefrologii są do tego faktu przygotowywani od wczesnego dzieciństwa. Niestety ogromna liczba chorób nerek wynika z zaniedbania i niewiedzy, często młodych ludzi. Wiele ignorowanych infekcji zwłaszcza ropnych (angina, ból zęba, ale także powikłania po grypie) może doprowadzić do bezobjawowego zapalenia nerek. O ile ostre zapalenie nerek można stosunkowo łatwo wyleczyć antybiotykami, to przejście choroby w etap przewlekły może doprowadzić do nieodwracalnego uszkodzenia nerek. Na domiar złego pierwsze objawy niewydolności nerek mogą zostać źle zinterpretowane przez chorego a nawet lekarza internistę. Objawem pogarszającej się pracy nerek, to objawy zatrucia organizmu, mylone z zatruciem pokarmowym: osłabienie, uczucie zmęczenia, nudności, wymioty, bóle głowy itp. Najbardziej charakterystycznym objawem, które trudniej zignorować, to wysokie ciśnienie tętnicze, wielomocz lub skąpomocz, odwodnienie lub obrzęki, świąd skóry, bezsenność, zaburzenie widzenia, oczopląs czy duszność. Do pewnego momentu, przy wystarczającej liczbie pracujących nefronów, bez specjalistycznych badań nie jesteśmy w stanie stwierdzić, czy nerki nie znajdują się już na granicy swoje wydolności. Teoretycznie wystarczy nam 30 % działających elementów każdej nerki, czyli 60% aktywnych nefronów przy jednej nerce. Wydaje się, że mamy bardzo duży zapas struktur filtrujących, ale może to być bardzo złudne. Podstawową codzienną profilaktyką wydaje się dostarczanie w ciągu doby co najmniej 2 l płynów wliczając w to wszystkie produkty zawierające dużą objętość wody, czyli zupy, owoce, herbatę, kawę, soki itp. Zwłaszcza istotne jest to w okresach intensywnego pocenia się (upał, wysiłek fizyczny) i w okresie zażywania leków potencjalnie groźnych dla nerek. Im mniejsza objętość krwi tym fizjologiczne stężenie trucizn w nerkach jest wyższe i może doprowadzić do trwałych uszkodzeń. Metody zastępowania niektórych funkcji nerek W przypadku przewlekłej niewydolności nerek, która jest stanem nieodwracalnego uszkodzenia kłębuszków nerkowych chory wymaga leczenia nerkozastępczego, ratującego jego życie. Rozróżniamy trzy możliwe metody terapii [4]: transplantacja nerki; hemodializa czyli pozaustrojowe oczyszczanie krwi; dializa otrzewnowa. Przeszczep nerki jest najbardziej korzystną opcją dla pacjenta, ale z braku wystarczającej bazy nerek do przeszczepu, nie zawsze możliwą. Nerka do przeszczepu musi spełniać pewne wymogi, a przede wszystkim zgodność tkankową. W Polsce przeszczep od żywego dawcy dopuszcza się w przypadku rodziny biorcy, jak również w przypadku dawcy niespokrewnionego, ale po orzeczeniu odpowiedniego sądu rejonowego. Nerka po przeszczepie, o ile zabieg się udał i nerka podjęła swoje funkcje, pomimo środków immunosupresyjnych jest cały czas odrzucana przez organizm biorcy. Zatem, po pewnym czasie konieczna jest następna transplantacja. Zazwyczaj przeszczep umieszcza się w dolnej części jamy brzusznej nad talerzem kości biodrowej. Hemodializę czyli pozaustrojowe oczyszczanie krwi wykonuje się przy pomocy skomplikowanej aparatury zwanej potocznie „sztuczną nerką” [1]. Zabieg polega na wyprowadzeniu krwi z tętnicy pacjenta, przepuszczenie jej wzdłuż błony półprzepuszczalnej, gdzie po drugiej stronie przeciwbieżnie przepływa odpowiednio dobrany płyn dializacyjny, i powrocie wstępnie oczyszczonej krwi do żyły pacjenta (rys. 2). Zabiegowi dializy, chory z całkowitą niewydolnością nerek musi poddawać się w stacji dializ 3 razy w tygodniu, od 3.5 5 godzin. Czas trwania zabiegu zależy przede wszystkim od objętości płynów ustrojowych, która jest wprost proporcjonalna do masy pacjenta. Rys. 2. Idea hemodializy. Niepotrzebne produkty przemiany materii czyli mocznik, kreatynina, kwas moczowy, fosforany i inne nadmiarowe cząstki drogą dyfuzji i osmozy przenikają z krwi do płynu dializacyjnego i wędrują do ścieku. W praktyce, nad całym tym prostym w idei procesem, czuwa skomplikowany technicznie aparat zwany potocznie „sztuczną nerką”. Alternatywnie do agresywnej metody hemodializy stosuje się dializę otrzewnową. Jest to proces w swojej koncepcji podobny do dializy pozaustrojowej (rys. 3). W tym przypadku, rolę błony półprzepuszczalnej pełni otrzewna wyścielająca jamę brzuszną. Dostęp krwi zapewnia bogate unaczynienie otrzewnej, a płyn dializacyjny wprowadza się i wyprowadza przez odpowiednio wprowadzony cewnik Tenckhoffa do położonej w dnie otrzewnej - jamy Douglasa. Rys. 3. Schemat dializy otrzewnowej. Po pewnym okresie (kilku godzin) płyn dializacyjny nasyca się i trzeba go wymienić. Dializa otrzewnowa z przyczyn oczywistych wymaga sterylnego pomieszczenia w czasie wprowadzania i wyprowadzania płynu i dużej ostrożności przy zabiegach pielęgnacyjnych. Często stosuje się ją u dzieci w czasie nocnego odpoczynku. Do takich zabiegów stosuje się stosunkowo mało skomplikowane urządzenie zwane cyklerem. Szczegóły dotyczące zabiegu hemodializy Jak już wcześniej wspomniano hemodializa polega na kontakcie krwi z odpowiednio przygotowanym roztworem soli poprzez błonę półprzepuszczalną. Zatem podstawową część wyposażenia potrzebnego do wykonania zabiegu dializy stanowi jednorazowy dializator w formie filtra kapilarnego (rys. 4). Rys. 4. Uproszczony model dializatora. W plastikowej osłonie znajduje się tysiące bardzo cienkich kapilar (o średnicy zewnętrznej 200-300 μm) zbudowane z półprzepuszczalnej błony np. z polisulfonu. Krew przepływa wewnątrz kapilar, a na zewnątrz płynie w przeciwnym kierunku płyn dializacyjny, Część składników krwi przepływa do dializatu, a niektóre cząsteczki z płynu przedostają się do krwi wyrównując pewne niedobory pacjenta (rys. 5). W dializatorze i rurkach potrzebnych do wykonania zabiegu mieści się nie więcej niż 100 ml krwi. Parametrami dializatora są: powierzchnia czynna kapilar (np. 1,8 m2); klirens czyli hipotetyczna objętość krwi, która jest całkowicie oczyszczona z danej substancji (zazwyczaj dotyczy mocznika) w przeliczeniu na minutę (np. 700 ml/min). Aby na całej długości kapilar zachować stały gradient przepływu danej substancji (np. mocznika) stosuje się przeciwbieżny przepływ dializatu w stosunku do ruchu krwi. Rys. 5. Budowa dializatora kapilarnego. Polimery i związki nieorganiczne stosowane do wytwarzania membran: Najwcześniej zastosowane i do dziś używane: celuloza, octan i azotan celulozy, Hydrofobowe: teflon, polifluorek winylidenu, polipropylen Hydrofilowe: poliamidy, polisulfon, poliwęglany, polialkohol winylowy Nieorganiczne: tlenki metali ZrO2, grafit, szkło, metale. Rys. 6. Przepływ cząstek w kapilarze. Aby skutecznie przeprowadzić zabieg dializy trzeba dysponować wodą klasy wody destylowanej (przewodność 1w trakcie dializy trwającej 3,5 - 5 godzin należy produkować czystą wodę na bieżąco. Do tego celu przeznaczona jest stacja uzdatniania wody, gdzie wodę oczyszcza się mechanicznie i chemicznie. Przykładowy schemat takiego procesu przedstawiono na rysunku (rys. 7). Po zastosowaniu w pierwszej kolejności mechanicznego filtru do wyłapania dużych zanieczyszczeń, woda z wodociągu wędruje do pojemnika, gdzie jest dodatkowo dochlorowana i natleniona. Następnie przechodzi do kolumn pochłaniających żelazo, następnie chlor i w następnej kolejności wapń. Po przejściu przez kolejne kolumny z filtrami zanieczyszczeń biologicznych, wstępnie oczyszczona woda przechodzi do modułu odwróconej osmozy, gdzie jest pod ciśnieniem około 12 atmosfer przepychana przez odpowiednie membrany. Ostatecznie, wysokiej jakości woda wpływa do zbiornika, z którego nieustannie wędruje po całym budynku stacji dializ. Część niewykorzystanej wody wraca do zbiornika. Nieustanny ruch wody zapobiega namnażaniu się chorobotwórczych drobnoustrojów. Rys. 7. Podstawowe elementy w torze oczyszczania wody. Płyn dializacyjny to nie tylko woda, ale także koncentraty płynu dializacyjnego. Odpowiednie substancje: chlorek sodu, wapń, magnez itp. są przygotowywane w odpowiednim stężeniu w formie koncentratu, który jest w aparacie sztucznej nerki na bieżąco mieszany z wodą, w proporcji 1:30. W efekcie powstaje roztwór, tak dobrany, aby korygował zaburzenia krwi pacjenta, zarówno na plus jak i na minus. Do zabiegu używa się dwóch typów koncentratu. Skład jednego z nich tzw. kwaśnego przedstawiono w tabeli (tab. 2). Drugi, to koncentrat węglanowy. Zazwyczaj stosuje się równocześnie obydwa koncentraty w odpowiednich proporcjach. Tab. 2. Skład płynu dializacyjnego. Substancja Płyn dializacyjny [mmol/l] Surowica krwi [mmol/l] SÓD 135 135-145 POTAS 2 3,5 – 5,0 WAPŃ 1,75 2,1 –2,6 MAGNEZ 0,75 0,75 – 1,25 CHLOR 105 95-106 OCTAN 38 0 Budowa aparatu do hemodializy Aparat do dializy składa się z dwóch podstawowych części: modułu krwi i modułu płynu dializacyjnego (rys. 8). Część hydrauliczna służy do przygotowania roztworu elektrolitów, utrzymywania odpowiedniej prędkości i składu płynu oraz do wychwytywania przecieku krwi przy ewentualnej awarii dializatora. Jest również odpowiedzialna za proces ultrafiltracji czyli pozbywania się ustalonej objętości wody z płynów ustrojowych pacjenta. Moduł krwi odpowiada za cały proces wyprowadzania i wprowadzania krwi z żył pacjenta, monitorowania ciśnień w odcinkach tętniczym i żylnym oraz za niedopuszczenie do wprowadzenia powietrza do żyły dializowanej osoby. Nad całą kilkugodzinną procedurą czuwa procesor i rozbudowana część elektroniczna umieszczona w module krwi z dala od części „mokrej”. Obsługa aparatu odbywa się przy pomocy dotykowego monitora, który umożliwia testy urządzenia, wprowadzanie parametrów dializy, oczyszczanie i dezynfekcję po zakończeniu całego procesu dializy i monitorowanie całego przebiegu zabiegu. Rys. 8. Schemat aparatu sztucznej nerki. Budowa modułu płynu dializacyjnego Moduł płynu dializacyjnego składa się z kilkunastu podstawowych segmentów (rys. 9). Uzdatniona woda ze stacji wody zostaje wprowadzona do aparatu po uprzednim pomiarze ciśnienia i ewentualnym jego zredukowaniu. Odpowiednia pompa np. zębata lub perystaltyczna utrzymuje zadaną prędkość przepływu płynu (standardowo 500ml/min). Woda powinna zostać ogrzana do temperatury ciała człowieka (około 38-39oC), co gwarantuje optymalną wymianę cząstek w dializatorze i równocześnie zapewnia komfort powracającej krwi, która ogrzewa się w ciepłym dializatorze. Woda w komorze odgazowania zostaje pozbawiona pęcherzyków powietrza, które osadzając się wzdłuż kapilar filtra mogłyby zmniejszyć wydajność całego procesu dializy. Po zmieszaniu wody z koncentratem jest sprawdzana temperatura (zazwyczaj dwoma niezależnymi czujnikami typu termopara) oraz przewodność elektrolityczna. Utrzymanie właściwego stężenia elektrolitów gwarantuje bezpieczeństwo pacjenta. Odwrotność natężenia prądu to przewodność podawana w milisimensach [mS]. Do badania przewodności służą konduktometry. Jeżeli zmieszany roztwór nie spełnia warunków zadanych w aparacie, to cały płyn wędruje obejściem (bocznikiem) do ścieku, dopóki nie ustali się oczekiwana temperatura i przewodność płynu. W momencie otrzymania właściwych parametrów, roztwór poprzez przepływomierz (zazwyczaj rotametr) jest dopuszczony do dializatora, a co za tym idzie do kontaktu z krwią pacjenta poprzez błonę półprzepuszczalną. Rys. 9. Schemat modułu płynu dializacyjnego. Płyn po opuszczeniu dializatora jest testowany na obecność krwinek, które mogły dostać się do płynu w sytuacji uszkodzenia kapilar w dializatorze. Ewentualne zmętnienie w płynie jest wychwytywane metodą fotometryczną (rys. 10). Źródło światła oświetla przepływający płyn, a znajdujące się po drugiej stronie fotodetektory dzięki specjalnym filtrom zwiększającym rozdzielczość pomiaru, mierzą natężenie światła. W przypadku zmiany natężenia światła na obu elementach optycznych wzbudza się alarm, który jest informacją dla obsługi, że należy wymienić dializator. Końcowym elementem drogi płynu dializacyjnego jest pompa ultrafiltracji, która zwiększając lub zmniejszając obroty wpływa na podciśnienie w dializatorze i steruje ilością wody wyciąganej z krwi pacjenta. Rys. 10. Schemat czujnika przecieku krwi. Istotnym elementem kontroli odwodnienia pacjenta jest mierzenie ciśnienia przezmembranowego tzw. TMP (TransMembrane Pressure). Wszystkie firmy produkujące aparaty do dializy prześcigają się w konstrukcji najlepiej działających systemów pomiaru TMP. Jedno z przykładowych rozwiązań przedstawia rys. 11. Różnica ciśnień przed i po dializatorze wpływa na prędkość obrotów pompy odwadniającej. Różnica w objętości płynu przed i po przepłynięciu przez dializator jest obliczana w trakcie całego procesu i stanowi objętość wody, którą pacjent traci w czasie dializy. Rys. 11. Kontrola ultrafiltracji. Budowa modułu krwi Obieg krwi składa się z igieł, które są wpięte do żyły i tętnicy pacjenta i łączą się z plastikowymi rurkami. Do prawidłowego prowadzenia zabiegu dializy wymagany jest przepływ krwi w granicach 150-300 ml/min. Tak dużego przepływu nie można uzyskać bez zastosowania pompy krwi wymuszającej krążenie w układzie pozaustrojowym. Wyższe składniki przepływu krwi u pewnych chorych są niezbędne do wyciągnięcia pewnych trudno usuwalnych substancji np. fosforanów. Im niższe wartości prędkości pompy, tym ryzyko powikłań ze strony serca pacjenta wydają się mniejsze. Krew z tętnicy, poprzez detektor ciśnienia wpływa zatem do pompy perystaltycznej (rys. 12). Pompa, z ustaloną wydajnością, przetacza krew do dializatora i przepycha ją przez cieniutkie kapilary filtra. Rys. 12. Budowa pompy perystaltycznej gdzie r - odległość ścianki od osi pompy. Pompa przewodowa pracuje na zewnątrz rurki z krwią i jest to jej podstawowa zaleta. Rolki na poruszającym się wale przeciskają krew (ugniatając rurkę) z jednego miejsca w drugie. Nacisk rolek jest regulowany i powinien jednocześnie być tak dobrany, aby nie niszczyć krwinek (hemoliza) ale żeby przy zatrzymanej pompie nie przepuszczać krwi. W tego typu pompie stosuje się silnik krokowy, który zapewnia optymalną kontrolę prędkości skoku. Przed wejściem do dializatora, w obiegu krwi znajduje się wskaźnik ciśnienia i ujście pompki heparyny (jest ona zwykle realizowana na bazie strzykawki, lub małej pompki perystaltycznej). Obecnie w celu zapewnienia optymalnej niekrzepliwości krwi, która pozostaje poza ustrojem pacjenta, stosuje się na początku zabiegu heparynę drobnocząsteczkową (np. nadroparynę). W trakcie zabiegu substancja jest oddializowana z krwi pacjenta i po skończonej dializie nie zagraża jego zdrowiu. Na wyjściu znajduje się ultradźwiękowy detektor powietrza (rys. 13), a za nim już odpływ do pacjenta. Bardzo niebezpiecznym zdarzeniem w trakcie zabiegu może być przedostanie się powietrza do układu krążenia wskutek nieszczelności w układzie pozaustrojowym (np. pęknięcie rurki czy pusta butelka infuzyjna). Powstanie zatoru powietrznego może w ustroju pacjenta objawić się zapaścią naczyniową, która może doprowadzić do jego śmierci. W specjalnym pojemniku, na drodze krwi, monitoruje się techniką ultradźwiękową poziom krwi a nawet pojawienie się pęcherzyków powietrza. Głowica nadawcza z jednej strony pojemnika wysyła falę ultradźwiękową, którą odbiera głowica odbiorcza umieszczona po przeciwnej stronie kolbki. Pojawienie się powietrza powoduje zakłócenie przechodzeniu fali ultradźwiękowej i jest rejestrowane przez głowicę odbiorczą. W razie wystąpienia problemów jest zatrzymywana pompa krwi i zostaje zamknięty dostęp do żyły pacjenta. Rys. 13. Ultradźwiękowy detektor pęcherzyków powietrza w krwi. Aby umożliwić wielokrotny dostęp do naczyń krwionośnych pacjentach wykonuje się zabieg operacyjny wytworzenia zespolenia tętnicy z żyłą (najczęściej na przedramieniu) zwany przetoką tętniczo-żylną [2]. Krew z tętnicy pod dużym, jak na warunki żylne ciśnieniem wpływa do żyły. Po pewnym czasie (około trzech tygodni) żyła uelastycznia się, ścianki się pogrubiają i przetoka jest gotowa na częste wkłuwanie igieł, tętniczej niżej, a żylnej wyżej.