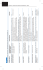Aberracje chromosomowe u płodów z wadą serca
Transkrypt
Aberracje chromosomowe u płodów z wadą serca
Perinatologia, Neonatologia i Ginekologia, tom 3, zeszyt 2, 88-91, 2010 Aberracje chromosomowe u płodów z wadą serca BARBARA PAWŁOWSKA1, JOANNA DANGEL2, ALICJA ILNICKA1, TOMASZ ROSZKOWSKI3, JOANNA BOGDANOWICZ1, ANNA TOMANKIEWICZ-ZAWADZKA1, BEATA SOBICZEWSKA1, MARZENA DĘBSKA1 Streszczenie Przedstawiono wyniki cytogenetycznych badań prenatalnych wykonanych u 255 płodów, u których badaniem USG i /lub echokardiograficznym rozpoznano wadę serca. Badania ultrasonograficzne i echokardiograficzne były wykonane w specjalistycznych ośrodkach ginekologii i położnictwa, w których po rozpoznaniu wady serca u płodu pobierano próbkę płynu owodniowego lub krwi pępowinowej. Badanie cytogenetyczne wykonywano stosując rutynowe techniki prążkowe, a w niektórych przypadkach FISH. Nieprawidłowy kariotyp stwierdzono w 91 (35%) przypadkach. Najczęstszymi aberracjami były aneuploidie: trisomię 18 zdiagnozowano w 38 przypadkach, trisomię 21 w 31 przypadkach, trisomię 13 w 5 przypadkach oraz monosomię X w 7 przypadkach. Ponadto w 10 przypadkach stwierdzono strukturalne aberracje chromosomowe, w tym w 4 przypadkach delecję 22q11.2. Najczęstszymi wadami serca stwierdzanymi prenatalnie, w których zdiagnozowano aberracje chromosomowe, były: AVSD, VSD, DORV, CoA, TOF, rzadziej HLHS. Aberracje chromosomowe zdiagnozowano w 60% przypadków z AVSD, w 57% przypadków z VSD, w 44% przypadków z DORV, 55% przypadków z TOF, w 50% przypadków z CoA, oraz w 17% przypadków z HLHS. Natomiast nie stwierdzono aberracji chromosomowych w innych wadach serca, w tym w 20 przypadkach zespołu heterotaksji. Dlatego też ultrasonograficzne rozpoznanie wady serca powinno być wskazaniem do wykonania cytogenetycznego badania prenatalnego, a w niektórych wadach, w przypadku prawidłowego kariotypu otrzymanego metodami cytogenetyki klasycznej, powinno być również wykonane badanie z zastosowaniem techniki FISH w celu wykrycia mikrodelecji 22q11.2. Słowa kluczowe: aberracje chromosomowe, wrodzone wady serca, cytogenetyczna diagnostyka prenatalna, USG, echokardiografia Wstęp Wrodzone wady serca występują u 8 -10 na 1000 żywo urodzonych noworodków i są jedną z najczęstszych przyczyn ich śmierci [1]. U płodów, zależnie od tygodnia ciąży, wrodzone wady serca stwierdzane są 3-5 razy częściej. Etiologia wad serca nie jest do końca poznana. Uważa się, że są one uwarunkowane wieloczynnikowo, ale na ich powstawanie mają również wpływ czynniki środowiskowe, np. infekcje, alkoholizm matki, leki zażywane w czasie ciąży. Są również dane wskazujące na genetyczne uwarunkowanie wad serca. Mogą to być mutacje pojedynczych genów bądź aberracje chromosomowe. Nieprawidłowości chromosomowe wykrywa się u 5% noworodków z wadą serca i aż w 33-42% u płodów z ujawnioną ultrasonograficznie wadą serca [2-4]. Najczęściej stwierdzane są aneuploidie: trisomia chromosomu 21 (zespół Downa), 18 (zespół Edwardsa), 13 (zespół Pataua), monosomia X (zespół Turnera). Obserwuje się pewną zmienność cech fenotypowych we wszystkich zespołach spowodowanych aberracjami chromosomowymi. Wady serca występują tylko w części przypadków, chociaż są charakterystyczne dla poszczególnych zespołów. W zespole Downa wadę serca stwierdza się w 70% przypadków, najczęściej występuje ubytek przegrody międzykomorowej i międzyprzedsionkowej (AVSD), ubytek przegrody międzykomorowej (VSD), tetralogia Fallota (TOF) i ubytek przegrody międzyprzedsionkowej (ASD); w zespole Edwardsa w 80% przypadków stwierdza się 1 2 3 VSD, AVSD, odejście głównych naczyń z prawej komory (DORV); w zespole Pataua VSD, ubytek w przegrodzie międzyprzedsionkowej (ASD). Dla zespołu Turnera charakterystyczne są koarktacja aorty (CoA) i ASD. W tym zespole wady serca występują w 23% przypadków. W tych trzech ostatnich zespołach chromosomowych występuje, choć rzadziej, hipoplazja lewej komory (HLHS) [2, 5]. Wady serca są charakterystyczną cechą fenotypową w zespołach mikrodelecji, np. w 75% przypadków zespołu delecji 22q11.2 najczęściej stwierdza się TOF, atrezję tętnicy płucnej (AT), VSD przerwany łuk aorty (IAA) i wspólny pień tętniczy (CAT) [6], w zespole Wiliamsa (interstycjalna delecja 7q11.23) występuje nadzastawkowe zwężenie aorty (SVAS), [7] w zespole delecji 1p36, kardiomegalia, zespół Ebsteina, ASD [8]. Wady serca występują także w zespołach związanych z mikroduplikacją fragmentu chromosomów, np. w tetraploidii 22q11.2 którą stwierdza się w zespole cat eye [2] lub występującej w części komórek (mozaikowość) tetraploidii 12p w zespole Palistera-Kiliana [9-11]. Wady serca (mitral valve prolapse) występują także w zespole kruchego X [12]. Mimo wielu badań nie znaleziono dotychczas genu lub genów, o których można by powiedzieć, że są odpowiedzialne za określoną wadę serca. Są natomiast doniesienia, że mutacja w jednym genie może być związana z różnymi wrodzonymi wadami serca, a jedna wada może być wywołana różnymi genami [9]. Instytut Psychiatrii i Neurologii, Warszawa Szpital Kliniczny im. Ks. Anny Mazowieckiej, Warszawa Klinika Położnictwa i Ginekologii, CMKP Samodzielny Szpital Kliniczny im. prof. W. Orłowskiego, Warszawa 89 Aberracje chromosomowe u płodów z wadą serca Materiał i metody Ryc. 1. Liczba różnych typów wad serca stwierdzonych prenatalnie w badaniu USG i/lub echokardiograficznym u 255 płodów: AVSD – ubytek przegrody międzykomorowej i międzyprzedsionkowej, VSD – ubytek przegrody międzyprzedsionkowej, DORV – odejście dużych naczyń z prawej komory, CoA – koarktacja aorty, HLHS – hipoplazja lewej komory, Ebstein – zespół Ebsteina, TOF – tetralogia Fallota, Heterotaksja – zespoły heterotaksji (lewy i prawy izomeryzm) 40 38 35 31 liczba przypadków W Zakładzie Genetyki w ciągu 5 lat wykonano ponad 5000 cytogenetycznych badań prenatalnych. Wady serca stwierdzono w 3% przypadków. Natomiast wśród pacjentek, u których wskazaniem do badania był nieprawidłowy obraz płodu stwierdzony badaniem USG, wady serca stanowiły aż 16% przypadków. Poniżej przedstawiono wyniki cytogenetycznych badań prenatalnych wykonanych z powodu stwierdzonej u płodu badaniem ultrasonograficznym i/lub badaniem echokardiograficznym wady serca u 255 pacjentek. We wszystkich przypadkach wykonano standardowe badanie cytogenetyczne, a w niektórych wykonano dodatkowo badanie cytogenetyczne z wykorzystaniem techniki FISH. Badanie cytogenetyczne wykonywane było w preparatach chromosomów uzyskanych z hodowli amniocytów prowadzonej na pożywce kompletnej (AmnioMax, lub AmnioGrow) oraz preparatach chromosomów otrzymanych z hodowli limfocytów krwi pępowinowej prowadzonej przez 72 godziny w 37EC w pożywce kompletnej (LymphoGrow). Prążki GTG otrzymywano po trawieniu trypsyną i barwieniu giemzą [13]. Technika FISH stosowana była w przypadku takich wad serca, które sugerowały obecność mikrodelecjii 22q11.2. Stosowano wówczas sondy specyficzne dla tego regionu: N25 lub TUPLE 1 (Cytocell). Jako sondę kontrolną stosowano sondę hybrydyzującą z okolicą subtelomerową dolnych ramion chromosomu 22. 30 25 20 15 Wyniki 10 Na rycinie 1 przedstawiono typy wad serca stwierdzone prenatalnie u 255 płodów. W badanym materiale, najczęściej stwierdzaną wadą były różne typy VSD – obserwowano ją w 56 przypadkach (22%) . Nieco rzadziej rozpoznawno AVSD – w 41 przypadkach (16%) , HLHS – w 36 przypadkach (14%) oraz DORV w 18 przypadkach (10%). Pozostałe wady stwierdzano znacznie rzadziej – poniżej 5% badanych przypadków. Aberracje chromosomowe stwierdzono w 91 przypadkach (35%) (ryc. 2 i tab. 1). Najczęstszymi były aneuploidie: trisomia 18 – w 38 przypadkach (40%) , trisomia 21 – w 31przypadkach (35%) , trisomia 13 w 5 przypadkach (6%) i monosomia X w 7 przypadkach (8%) . Ponadto w 10 przypadkach (11%) stwierdzono strukturalne aberracje chromosomowe: addycję na 15 (fragment dolnych ramion chromosomu 2), der (22), addycję na chromosomie 22 (niezidentyfikowany fragment), del 5p, interstycjalną delecję chromosomu 10, der (14). Wśród aberracji strukturalnych, delecję 22q11.2 stwierdzono w 4 przypadkach (13%) spośród 30 badanych techniką FISH w kierunku wykrycia mikrodelecji 22q11.2. W jednym przypadku delecja była odziedziczona od ojca. Wśród badanej grupy u 142 płodów (56%) stwierdzono izolowaną wadę serca, a u 113 płodów (44%) oprócz wady serca wystąpiły dodatkowe wady. W grupie z izolowaną wadą serca aberracje stwierdzono w 31 przypad- 5 7 0 5 trisomia 18 trisomia 21 6 4 trisomia 13 monosomia X del 22q11.2 inne strukturalne Ryc. 2. Aberracje chromosomowe stwierdzone u 255 płodów z rozpoznaną prenatalnie wadą serca ków (22%), natomiast jeśli wadzie serca towarzyszyły inne nieprawidłowości w obrazie USG płodu, aberracje chromosomowe stwierdzano częściej, w 60 przypadkach (53%) (ryc. 3). W tabeli 1 przedstawiono wady serca najczęściej współistniejące z aberracjami chromosomowymi. Aberracje chromosomowe zdiagnozowano w 30 przypadkach (60%) z AVSD, w 32 przypadkach (57%) z VSD, w 8 przypadkach (44%) z DORV, 11 przypadkach (55%) z TOF, w 4 przypadkach (50%) z CoA, oraz w 36 przypadkach (17%) z HLHS. Natomiast nie stwierdzono aberracji chromosomowych w przypadkach innych wad serca, np. w 20 przypadkach zespołu heterotaksji. Spośród 255 badanych ciąż w 26 przypadkach stwierdzono wewnątrzmaciczne obumarcie ciąży, w 30 przypadkach pacjentki podjęły decyzję o przerwaniu ciąży, w 20 nastąpił zgon okołoporodowy lub martwe urodzenie. Żywo urodziło się 179 noworodków, ale z tej grupy wkrótce po urodzeniu zmarło 88. Do momentu przedstawienia niniejszej pracy żyło 91 dzieci – 36% z badanych 255 płodów. 90 B. Pawłowska, J. Dangel, A. Ilnicka et al. Tabela 1. Wady serca najczęściej współistniejące z aberracjami chromosomowymi Typ wady serca (n) Aberracja chromosomowa Trisomia 21 VSD (56) 9 AVSD (51) 20 DORV (18) Trisomia 18 Trisomia 13 Monosomia X 20 1 9 1 1 1 1 1 CoA (8) 2 1 1 HLHS (36) 1 1 3 38 5 7 3 Inne aberracje Aberracje chromosomowe łącznie (%) 2 32 (57%) 1 5 TOF(20) Delecja 22q11.2 30 (60%) 4 2 8 (45%) 1 11 (55%) 4 (50%) 1 6 (17%) 6 91(100%) Heterotaksja (20) Ebstein (12) Inne Łącznie (34) 32 4 Skróty wad serca – patrz podpisy pod ryc. 1. Ryc. 3. Liczba aberracji chromosomowych w grupie z izolowaną wadą serca i w grupie z wadą serca i innymi wadami Dyskusja Powstawanie wrodzonych wad serca uwarunkowane jest wieloczynnikowo. Jedną z przyczyn są aberracje chromosomowe, najczęściej aneuploidie. W zależności od rodzaju rozpoznanej wady serca stwierdza się je w różnym odsetku przypadków. W przedstawionym materiale wskazaniem do wykonania cytogenetycznego badania prenatalnego był stwierdzony w obrazie USG i/lub echokardiograficznym nieprawidłowy obraz czterech jam serca, a w niektórych przypadkach dodatkowo ujawnione inne wady płodu. Aberracje chromosomowe stwierdzono w 91 przypadkach (35%). Wyniki te były zgodne z badaniami Tenstedta i wsp. (1999), który zdiagnozował aberracje chromosomowe w 33% badanych płodów z wadą serca, a nieco niższe od wyników otrzymanych przez Allana i wsp. (1994), który stwierdził nieprawidłowości chromosomowe w 42% płodów z wadą serca. Ale jeśli dokonano podziału na przypadki z izolowaną wadą serca oraz z wadą serca i towarzyszącymi nieprawidłowościami płodu, aberracje stwierdzano odpowiednio w 22 i 53%. Wyniki te są zgodne z danymi Raymonda i wsp. Przedstawione w tabeli 1 wyniki badań cytogenetycznych, zgodnie z wcześniejszymi doniesieniami [14, 15], potwierdzają współwystępowanie określonych wad serca z określonymi zespołami związanymi z aneuploidią. Najczęściej stwierdzanymi wadami serca w tych zespołach są VSD, AVSD, TOF, CoA i DORV. Rzadko występuje HLHS, nie stwierdzono natomiast aberracji chromosomowych w innych wadach serca, np. w przypadkach zespołów hetermotaksji. Dlatego wydaje się słuszne kierowanie na inwazyjną diagnostykę prenatalną i badanie cytogenetyczne tych pacjentek, u których rozpoznano prenatalnie AVSD, VSD, TOF, DORV, CoA, HLHS. Z danych przedstawionych w tabeli 1 wynika, że w trisomii 21 najczęściej występuje AVSD i VSD, nie stwierdza się natomiast HLHS, DORV i CoA, w trisomii 18 najczęściej obserwowaną wadą serca są VSD, AVSD i DORV. W poszukiwaniu genów odpowiedzialnych za powstawanie wad serca coraz więcej uwagi zaczęto poświęcać powiązaniu ich z mikrodelecjami, szczególnie z wykrywaną techniką FISH delecją 22q11.2. Ponieważ wiadomo, że u pacjentów z tą delecją najczęstszą stwierdzaną nieprawidłowością serca jest wada stożka [16], badanie techniką FISH z sondami ukierunkowanymi na wykrycie tej delecji wykonano tylko w 30 wybranych przypadkach i w tej grupie stwierdzono 4 przypadki (13%) mikrodelecji. We wszystkich przypadkach rozpoznano TOF. Dotychczas nie znaleziono takiego genu, ale są pewne dane wskazujące na powiązanie wad serca z znajdującym się w obszarze delecji genem TBX. W momencie zbierania materiału żyło 91dzieci (36%) z badanych 255 przypadków. Należy przypuszczać, że część dzieci, z tej grupy, u których rozpoznano cięższą wadę serca zmarło w okresie późniejszym, co nie zostało odnotowane. Wnioski Przedstawione wyniki potwierdzają fakt, że ultrasonograficzne rozpoznanie u płodu wady serca jest wskaza- Aberracje chromosomowe u płodów z wadą serca niem do inwazyjnej diagnostyki prenatalnej w celu oznaczenia kariotypu płodu. Szczególnie w przypadkach, jeśli oprócz wady serca rozpoznane są ultrasonograficznie inne wady płodu istnieje wysokie ryzyko wystąpienia aberracji chromosomowej. W przypadku prawidłowego kariotypu otrzymanego metodami cytogenetyki klasycznej, w niektórych przypadkach, powinno być również wykonane badanie z zastosowaniem techniki FISH w celu wykrycia mikrodelecji 22q11.2. Określenie kariotypu płodu pozwala na prognozowanie losów badanej ciąży oraz zapewnienie specjalistycznej opieki około i poporodowej. Uzyskany wynik badania cytogenetycznego daje możliwość określenia ryzyka genetycznego powtórzenia się wady serca w przypadku kolejnych ciąż. Piśmiennictwo [1] Allan L. (2000) Antenal diagnosis of heart disease. Heart 83: 367. [2] Allan L.D., Sharlan G.K., Milburn A. et al. (1994) Prospective diagnosis of 1,006 consecutive cases of congenital heart disease in the fetus. J. Am. Coll. Cardiol. 23: 1452-1458. [3] Tennestedt C., Chaoui R., Körner H. et al. (1999) Spectrum of congenital heart drfects and extracardiac malformations associated with chromosomal abnormalities: results of seven year necropsy study. Heart 82: 34-39. [4] Wimalasundera R.C., Gardiner H.M. (2004) Congenital heart disease and anuploidy. Prenat. Diagn. 24: 1116-1122. [5] Allan L.D., Apfel H.D., Printz B.F. (1998) Outcome after prenatal diagnosis of hypoplastic left heart syndrome Heart 79: 371-373. [6] Ryan A.K., Goodship J.A., Wilson D.I. et al. (1997) Spectrum of clinical features associated with interstitial chromosome 22q11 deletions: a European collaborative study. J. Med. Ge- 91 [7] Lowery M.C., Morris C.A., Ewart A. et al. (1995) Strong cor- relation of elastin deletion, detected by FISH, with Williams Syndrome: evaluation of 235 patients. Am. J. Hum. Genet. 57: 49-53. [8] Slavotinek A., Shaffer L.G., Shapira S.K. (1999) Monosomy 1p36. J. Med. Genet. 36: 657-663. [9] Ramegowda S., Ramachandra N.B. (2005) An understanding the genetic basis of congenital heart disease. J. Hum. Genet. 11: 14-23. [10] Abad D.E., Gabare J.A., Izquierdo A.M. et al. (2006) Pallister- Killian syndrome presenting with a complex congenital heart defect and nuchal translucency. J. Ultrasound Med. 25: 1475-1480. [11] Ryelonds J.F., Daniel A., Kelly T.E. et al. (1987) Isochromo- some 12 p mosaicism (Pallister mosaic aneuploidy or Pallister-Killian syndrome): report of 11 cases. Am. J. Med. Ge- net. 27: 257-274. [12] Prasad C., Chudley A.E. (2002) Genetics and cardiac anomalies: the heart matter. Indian J. Pediatr. 69: 321-332. [13 Seabright M. (1971) A rapid banding technique for human chromosomes. Lancet 2: 971. [14] Paladini D., Russo M.G., Teodoro A. et al. (2002) Prenatal diagnosis of congenital heart disease in the Naples area Turing the years 1994-1999 – the expirience of joint fetal-pediatric cardiology unit. Prenat. Diagn. 22: 545-552. [15] Raymond F.L., Simpson J.M., Sharland G.K. et al. (1997) Fetal echocardiography as a predictor of chromosomal abnormality. Lancet 350: 930. [16] Ziolkowska http://www.springerlink.com/content/ p7387875 306m3607/ – ContactOfAuthor1 L., Kawalec W., Turska-Kmiec A. et. al (2008) Chromosome 22q11.2 microdeletion in child- ren with conotruncal heart defects: frequency, associated cardiovascular anomalies, and outcome following cardiac surgery. Eur. J. Pediatr. 167: 1135-1140. J Barbara Pawłowska Instytut Psychiatrii i Neurologii 02-957 Warszawa, ul. Sobieskiego 9 net. 34: 798-804. Chromosomal aberrations with fetuses with congenital heart disease Analysis of cytogenetic results in 255 fetuses with congenital heart disease (CHD) are presented. Pregnant women were referred for genetic counseling due to fetal heart defect diagnosed during ultrasound and fetal echocardiography examination. Ultrasound and fetal echocardiography examinations were performed using different ultrasound machines, in two referral centers for obstetrics and fetal echocardiography. After diagnosis of a CHD, amniotic fluid or fetal blood samples were collected. Cytogenetic examinations were performed using routine cytogenetic bandings techniques and FISH. In 91 fetuses (35%) the karyotype was abnormal. The most common chromosomal aberration associated with congenital heart disease was aneuploidy: trisomy 18 in 38 cases, trisomy 21 in 31 cases, trisomy 13 in 5 cases, monosomy X in 7 cases. In 10 cases other chromosomal abnormalities were detected. In this group 4 cases of 22q11.2 microdeletion was found. Atrioventricular septal defect (AVSD), ventricular septal defect (VSD), tetralogy of Fallot (TOF), double outlet of right ventricle (DORV) and coarctation of the aorta (CoA) were the most common CHD among fetuses with chromosomal aberrations. Chromosomal aberrations were found in: AVSD – 60% of cases, VSD – 57% of cases, DORV – 44% of cases, TOF – 55% of cases, CoA – 50% of cases and hypoplastic left heart syndrome (HLHS) – 17% of cases. No chromosomal aberrations were found in other cases of CHD, e.g. in 20 cases of heterotaxy. Conclusions: Chromosomal aberrations, particularly aneuploidy were the most frequent in AVSD, VSD, DORV, TOF, and HLHS whereas no aberrations were found in other cases of CHD. In cases with abnormal USG and/or echocardiography findings, cytogenetic examination should be offered. In cases of conotruncal CHD with normal karyotype, FISH study for 22q11 del should be performed. Key words: chromosomal aberrations, congenital heart disease, cytogenetic prenatal diagnosis, USG, echokardiografia