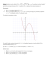laboratorium techniki cieplnej
Transkrypt
laboratorium techniki cieplnej
LABORATORIUM TECHNIKI CIEPLNEJ INSTYTUTU TECHNIKI CIEPLNEJ WYDZIAŁ INŻYNIERII ŚRODOWISKA I ENERGETYKI POLITECHNIKI ŚLĄSKIEJ INSTRUKCJA LABORATORYJNA Temat ćwiczenia: BADANIE POPRAWNOŚCI OPISU STANU TERMICZNEGO POWIETRZA PRZEZ RÓWNANIE CLAPEYRONA Sprawdzanie poprawności opisu stanu termicznego powietrza przez równanie Clapeyrona 2 1. WSTĘP Termiczne równanie stanu substancji jest podstawowym równaniem termodynamiki. Zgodnie z zerową zasadą termodynamiki jest to zależność pomiędzy ciśnieniem, temperaturą i objętością właściwą (lub gęstością). Ogólnie można je zapisać w postaci: F ( p, T , v ) = 0 , (1) F ( p, T , ρ ) = 0 . (2) lub W literaturze termodynamicznej zamieszczono już ponad dwa tysiące równań tego typu opracowanych w większości przypadków dla gazów. Wszystkie te równania podzielić na dwie grupy: • równania stosunkowo dokładne, nadające się do obliczeń właściwych, lecz o ograniczonym zakresie stosowania zarówno odnośnie do zmian parametrów termicznych stanu (p,T) jak też rodzaju gazu, • równania bardziej uniwersalne zarówno odnośnie do rodzaju gazu, jak też zakresu zmian parametrów, ale mniej dokładne i przydatne raczej do teoretycznych rozważań jakościowych lub obliczeń ilościowych przy pewnych parametrach termicznych. Przykładem równań pierwszego typu są równania termiczne dla pary wodnej podane w postaci wykresów, tablic i wzorów o skomplikowanej postaci matematycznej. Najbardziej popularnym równaniem drugiego typu jest równanie Clapeyrona. Zostało ono najpierw sformułowane w oparciu o prawa doświadczalne: Boyle’a (1662) – Mariotte'a (1676), J.L. Gay-Lussaca (1802) – Daltona (1802) oraz Avogadra (1811). Obecnie równanie to można wyprowadzić w oparciu o kinetyczną teorię gazów. Równanie Clapeyrona dotyczy wprawdzie gazów doskonałych i półdoskonałych, ale przy niskim ciśnieniu i temperaturze znacznie większej od temperatury nasycenia może być stosowane do gazów rzeczywistych. W ramach ćwiczenia laboratoryjnego równanie Clapeyrona zostanie zastosowane dla powietrza o temperaturze otoczenia (Tot < Ts) i ciśnieniu niewiele większym od ciśnienia otoczenia – p = (1...1.25)pot. Równanie Clapeyrona ma następującą postać matematyczną: p ⋅ v = R ⋅T , (3) gdzie: p – ciśnienie bezwzględne, Pa, . 3 v – objętość właściwa, m /kg, R – indywidualna stała gazowa, J/(kg·K), T – temperatura bezwzględna, K. Indywidualna stała gazowa dla gazu jednorodnego obliczana jest z zależności: (MR ) , R= (4) M przy czym M oznacza masę molową gazu, natomiast (MR) = 8314 J/(kmol·K) oznacza uniwersalną stałą gazową, jednakową dla wszystkich gazów. W przypadku roztworu gazów indywidualna stała gazowa obliczona może być z zależności: R= (MR ) ∑M i zi , i Instrukcja laboratoryjna LABORATORIUM TECHNIKI CIEPLNEJ (5) Sprawdzanie poprawności opisu stanu termicznego powietrza przez równanie Clapeyrona 3 przy czym zi oznacza udział molowy i-tego składnika w roztworze. Równanie Clapeyrona może posłużyć do wyznaczenia ilości substancji jeżeli zostanie nieznacznie przekształcone do postaci: p ⋅ V = n ⋅ (MR ) ⋅ T (6) p ⋅V = G ⋅ R ⋅ T , (7) lub gdzie: V – całkowita objętość układu, m3, n – ilość substancji gazu, kmol, G – masa gazu, kg. 2. OPIS STANOWISKA 1 H1 2 2.5 m 5 H2 3 h 4 Rys. 1 Schemat stanowiska pomiarowego Schemat stanowiska przedstawia rysunek 1. Podczas wlewania wody do lejka 1 spływa ona poprzez rurkę 2 (o wysokości 2.5 m) do zbiornika 3. W miarę podnoszenia się poziomu wody gaz, zamknięty w górnej części zbiornika, ulega sprężeniu, tak by jego ciśnienie równoważyło ciśnienie hydrostatyczne słupa wody w rurce pionowej. Poziom wody w zbiorniku może być obserwowany i mierzony dzięki poziomowskazowi 4. Wysokość słupa wody w rurce 2 może być zmierzona dzięki poziomowskazowi 5. Zbiornik wyposażony jest w górnej swej części w zawór gazowy umożliwiający wyrównanie ciśnienia Instrukcja laboratoryjna LABORATORIUM TECHNIKI CIEPLNEJ Sprawdzanie poprawności opisu stanu termicznego powietrza przez równanie Clapeyrona 4 w zbiorniku z ciśnieniem otoczenia oraz termoparę. Na całej wysokości zbiornika znajduje się podziałka umożliwiająca odczytanie poziomów wody w poziomowskazach. Dla poziomu lustra wody w zbiorniku zapisać można warunek równości ciśnień w postaci: p = p ot + ρ w (H 2 − H 1 ) ⋅ g , (8) gdzie: ρw – gęstość wody, kg/m3, g – przyspieszenie ziemskie, 9.81 m/s2, pot – ciśnienie otoczenia, Pa, p – ciśnienie panujące w zbiorniku, Pa. Średnica wewnętrzna zbiornika 3 wynosi D = 148 mm, a średnica zewnętrzna rurki 2 d = 17 mm. 3. PRZEBIEG ĆWICZENIA 1. Zanotować temperaturę i ciśnienie otoczenia. 2. Otworzyć zawór gazowy. 3. Nalać przez lejek 1 wody tak, by jej poziom znalazł się na wysokości dolnej części skali. 4. Zamknąć zawór, odczekać 5 minut i zanotować temperaturę w zbiorniku oraz jej poziom liczony od górnej krawędzi zbiornika. 5. Nalać wody, tak by jej powierzchnia w rurce 2 znajdowała się powyżej zbiornika 3. 6. Odczekać, aż temperatura spadnie do wartości zanotowanej w punkcie 3. 7. Dokonać odczytu obydwóch poziomów H 1 , H 2 oraz h. 8. Dolać wody w takiej ilości, by jej poziom w rurce 2 wzniósł się o 10 cm i powtórzyć czynności z punktów 6-8. Poniżej przedstawiono wzór tabeli pomiarowej. ∆τ, min H1, cm H2, cm h, cm t, ºC 4. OPRACOWANIE WYNIKÓW POMIARÓW Dla każdego z pomiarów obliczyć: • ciśnienie panujące w zbiorniku wg zależności (8), przy czym przy czym gęstość wody w zależności od temperatury przyjąć wg poniższej tabeli, temperatura, °C gęstość, kg/m3 5 10 15 20 25 30 999.9 999.6 999.0 998.2 997.0 995.6 Instrukcja laboratoryjna LABORATORIUM TECHNIKI CIEPLNEJ Sprawdzanie poprawności opisu stanu termicznego powietrza przez równanie Clapeyrona • 5 objętość gazu (D V =h⋅n 2 ) −d2 , 4 gdzie D i d oznaczają odpowiednio wewnętrzną średnicę zbiornika 3 oraz zewnętrzną średnicę rurki 2. • ilość kmol gazu zawartego w zbiorniku według zależności: n= pV . (MR )T Przyjmując, że równanie Clapeyrona jednakowo dobrze charakteryzuje powietrze w całym badanym zakresie ciśnień, policzyć średnią wartość ilości kilomoli gazu: k n= ∑n i =1 i k oraz odchylenie standardowe: k σ= ∑ (n i =1 i − n) 2 k ⋅ (k − 1) przy czym k oznacza liczbę pomiarów. 5. SPRAWOZDANIE Sprawozdanie powinno zawierać: 1) krótki wstęp teoretyczny, 2) schemat stanowiska pomiarowego i opis metody pomiarowej, 3) zestawienie wzorów i zależności użytych w obliczeniach, 4) zestawienie wyników pomiarów, 5) zestawienie wyników obliczeń ilości substancji powietrza, przy czym dla jednego pomiaru należy przedstawić szczegółowy tok obliczeń z podstawieniami do wzorów, 6) statystyczne opracowanie wyników pomiarów, 7) uwagi końcowe oraz wnioski. LITERATURA 1. J. Nadziakiewicz (red.): Laboratorium Techniki Cieplnej. Skrypt Politechniki Śląskiej nr 1853, Gliwice 1995. 2. J. Szargut: Termodynamika techniczna. Wydawnictwo Politechniki Śląskiej, Gliwice 1997. 3. H. Górniak, J. Szymczyk: Podstawy termodynamiki. Część I i II, Wydawnictwo Politechniki Śląskiej, Gliwice 1999. Instrukcja laboratoryjna LABORATORIUM TECHNIKI CIEPLNEJ