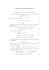Termodynamiczne ujecie procesów wzrostu
Transkrypt
Termodynamiczne ujecie procesów wzrostu
Fizyka, technologia oraz modelowanie wzrostu kryształów Stanisław Krukowski i Michał Leszczyński Instytut Wysokich Ciśnień PAN 01-142 Warszawa, ul Sokołowska 29/37 tel: 88 80 244 e-mail: [email protected], [email protected] Zbigniew Żytkiewicz Instytut Fizyki PAN 02-668 Warszawa, Al. Lotników 32/46 E-mail: [email protected] Wykład – 2 godz./tydzień – piątek 13.15 – 15.00 Interdyscyplinarne Centrum Modelowania UW Budynek Wydziału Geologii UW – sala 3089 http://www.unipress.waw.pl/~stach/wyklad_ptwk_2007/ Wykład 5. Termodynamiczne i kinetyczne ujęcie procesów wzrostu Równowaga: - pomiędzy różnymi fazami - wewnątrz pojedynczej fazy i/ przestrzenna – pojecie lokalnej równowagi ii/ pomiędzy różnymi stopniami swobody – pojęcie równowagi cząstkowej Równowaga: - mechaniczna - cieplna - chemiczna Równowaga pomiędzy fazami • Stan fizyczny układu dwu faz, niezależny od czasu, taki że po wprowadzenie przegród nie ulega zmianie • Stan fizyczny układu dwu faz, niezależny od czasu, taki że strumienie się równoważą: - mechaniczna strumień pędu - cieplna strumień energii - chemiczna strumień masy Równowaga - strumienie • Przykład układu dwu faz – faza gazowa i faza stała: • Strumień cząstek gazu uderzający o powierzchnie ciała stałego (liczba cząstek na jednostkę powierzchni i jednostkę czasu: p I= 2πmkT Gaz idealny cząstek – własności równowagowe, transportowe i strumienie • Równanie stanu p = nk BT pV = Nk BT • Średnia droga swobodna średni czas pomiędzy zderzeniami 1 λ= 2nσ τ= λ v v = 3k BT m • Średni strumień cząstek nie zależy od własności transportowych: p k BT =n I= 2πm 2πmkT Gaz idealny cząstek – własności w liczbach • Gęstość (warunki normalne) n = 2,7 *1019 cm −3 • Średnia prędkość (azot N2) v(300K ) = 3k BT m = 512 m s • Średnia droga swobodna i średni czas pomiędzy zderzeniami λ= 1 = 3 *10 −6 m 2 nσ τ= λ v Typowy rozmiar cząsteczki – d = 2R ~ 10-10 m Przekrój całkowity na zderzenie – σ = πR2 ~ 10-20 m = 5.6 *10 −9 s Geometryczne własności powierzchni • Gęstość GaN (cząsteczek) i objętość właściwa n = 4.3 *10 22 cm −3 • Objętość właściwa GaN v = 2.3 *10 −23 cm 3 • Gęstość atomów na powierzchni GaN η=n 2 3 = 1,2 *1015 cm − 2 • Powierzchnia GaN na jeden atom 2 s o = v o 3 = 8.1*10 −16 cm 2 Strumienie i równowaga powierzchni • Średni strumień cząstek (warunki normalne): I= p k T = n B = 8.7 *10 23 cm − 2s −1 2πm 2πmkT • Częstość uderzania cząsteczek w węzeł ν g = I * s o = 7,1*108 s −1 • Adsorpcja – strumień i współczynnik przyklejania (sticking coeff.) R = s o *ν * σ = I * σ • Szybkość adsorpcji – częstość i współczynnik przyklejania (sticking coefficient) r = ν*σ σ – współczynnik przyklejania Współczynnik przyklejania • Współczynnik przyklejania (sticking coefficient) – prawdopodobieństwo przejścia ze stanu początkowego do końcowego σ = P(i → f ) • Prawdopodobieństwo przejścia – wprowadzamy pojęcie stanu przejściowego „transition state - T” - ma energię wyższą niż stan wyjściowy - konfiguracja energetyczna – stan siodłowy - po osiągnięciu tego stanu układ nie może wrócić do stanu wyjściowego Stan przejściowy – ewolucja układu • Ewolucja układu – podczas reakcji chemicznej: Energia Bariery energetyczne: T ∆E(T-A) = E(T) – E(A) ∆E(T-B) = E(T) – E(B) A B Współrzędna reakcji Stan przejściowy – bariery energetyczne • Ewolucja układu – podczas reakcji chemicznej: Energia Bariery energetyczne: T ∆E(T-B) ∆E(T-A) - Przejście A B ∆E(T-A) = E(T) – E(A) - Przejście A B A B ∆E(T-B) = E(T) – E(B) Współrzędna reakcji Energia – wartość całkowitej energii układu w przybliżeniu adiabatycznym Stan przejściowy – prawdopodobieństwo • Energia swobodna układu o temperaturze T : F = −k BT ln Q = −k BT ln(Q tr Q vib Q rot ) • Prawdopodobieństwo znalezienia układu o w danym stanie makroskopowym jest proporcjonalne do objętości przestrzeni fazowej Q. • Dla współrzędnej reakcji – prawdopodobieństwo względne przejścia do stanu przejściowego jest wiec równe P (T ) Q (T ) F (T ) − F ( A ) = = exp − P ( A) Q ( A) k BT Q(T) i Q(A) – są sumami statystycznymi po innych stopniach swobody Stan przejściowy – zależność Arrheniusa • Nie występuje silne sprzężenie (dynamiczne – polegające na zmianie hamiltonianu) z innymi stopniami swobody Q(T)=Q(A) F(T ) − F(A ) P(T ) = exp − P(A ) k BT P (T ) S (T ) − S ( A ) E (T ) − E ( A ) = exp exp − P ( A) k k T B B • W przypadku gdy entropie tych stanów są w przybliżeniu równe (co zachodzi gdy nie zachodzi dekompozycja układu), otrzymujemy zależność Arrheniusa: ∆E E(T ) − E(A ) P(T ) = exp − = exp − P(A ) k BT k BT Modele wzrostu – własności energetyczne Modele dynamiczne Modele kinetyczne Energia Energia T T ∆E(T-A) ∆E(T-A) ∆E(T-B) ∆E(T-B) A B A Współrzędna reakcji ∆E r = ν * σ = ν * P(i → f ) ≅ ν * exp − k T B B Współrzędna reakcji Modele wzrostu Modele dynamiczne • Prawdopodobieństwa przejść są podobne • Należy uwzględniać przejścia w obydwu kierunkach • Występuje stan równowagi Modele kinetyczne • Prawdopodobieństwa przejść różnią się zasadniczo lub • Występują blokada na przejście w jednym kierunku – brak przejścia powrotnego • Nie występuje stan równowagi Model dynamiczny równowagi gaz - kryształ :uproszczony • Osadzanie (g k) Energia Gaz ∆E(K-G) R = I * so = p * so k BT = n * so 2πm 2πmkT • Sublimacja (k g) Kryształ Współrzędna reakcji ∆E(K − G ) R = ν * exp − k T B Model dynamiczny równowagi „roztwór – kryształ” :uproszczony • Dyfuzja • Krystalizacja R =ν Energia Ciecz ∆E(K-C) • Rozpuszczanie Kryształ Współrzędna reakcji ∆E(K − C ) R = ν * exp − k T B Wzrost – odchylenie od stanu równowagi Warunki równowagi: • Dynamicznej pl = pg=peq • Cieplnej • Chemicznej µl = µg= µeq Tl = Tg=Teq Odchylenie od stanu równowagi: • Praktycznie nie występuje (tzn. rzadko występuje lub rzadko jest stosowane) • Przechłodzenie ∆τ = Tl,g − Ts Ts • Przesycenie σ= µ l ,g − µ s k BTs Przesycenie Przechłodzenie: ∆τ = Tl,g − Ts Ts sl ∆µ σ= = ∆τ k BTs k B x ∆µ µs (p, Teq ) − µ l (p eq , Teq ) = = ln W roztworze idealnym: σ ≡ RT RT x eq x – koncentracja roztworu W gazie idealnym: p ∆µ µ s (p, Teq ) − µ l (p eq , Teq ) = = ln σ≡ RT RT p eq Przesycenie – małe wartości W roztworze idealnym: x x − x eq x − x eq ∆µ = ln = ln 1 + σ≡ ≅ RT x eq x eq x eq x – koncentracja roztworu W gazie idealnym: p p − p eq p − p eq n − n eq ∆µ = ln = ln 1 + = σ≡ ≅ RT p eq p eq n eq p eq n – gęstość gazu Stany metastabilne - przesycenie Rozważymy przejście fazowe I rodzaju np. faza stała – faza gazowa. W przypadku gdy, dla zadanej temperatury w stanie równowagi następuje zmiana ciśnienia, np. jego podwyższenie, układ nie spełnia warunków równowagi faz – powinien przejść w całości w stan stały. Różnica potencjału chemicznego fazy gazowej i fazy stałej jest ujemna – faza gazowa jest niestabilna. Prowadzi to do przesycenia: p ∆µ µ s (p, Teq ) − µ l (p eq , Teq ) = = ln RT RT p eq W równaniu tym użyto zależności dla gazu doskonałego. Stany metastabilne - bariery nukleacyjne W przypadku gdy, potencjał dla fazy stałej jest niższy, układ powinien przejść w stan stały. Jednak wytworzenie skończonego obszaru nowej fazy wymaga wydatku energii na utworzenie nowej powierzchni międzyfazowej. Oznaczmy gęstość energii na jednostkę powierzchni kryształu przez ε. Wówczas całkowita zmiana energii przy utworzeniu skończonego obszaru (kuli o promieniu R) fazy stałej jest równa 4πR 3ρ ∆U = ∆µ + 4πR 2 ε 3 Wyraz związany z powierzchnią (proporcjonalny do R2) jest zawsze dodatni, natomiast wkład objętościowy (proporcjonalny do R3) zależy od potencjału chemicznego w fazie gazowej. Dla przesycenia w fazie gazowej jest on ujemny. Stany metastabilne - bariery nukleacyjne - rozmiar 8 Całkowita zmiana energii jest równa: 6 4 4πR 3ρ ∆E = ∆µ + 4πR 2 ε 3 Ebar E 2 0 -2 Dodatni wyraz związany z powierzchnia dominuje dla promieni małych, natomiast ujemny wkład objętościowy przeważa dla dużych. -4 3 Ev=(4/3)πR ρ∆µ 2 Es=4πR ε E=Es+Ev -6 -8 0 20 40 60 80 100 120 140 160 180 200 220 R Poziom energii dla maksimum nazywamy barierą nukleacyjną. Zarodek o takim rozmiarze nazywamy zarodkiem (rozmiarem) krytycznym. Otrzymujemy: R crit = 2ε 2ε ≅ ρ ∆µ ρk BTσ Bariera nukleacyjna dla zarodka (rozmiaru) krytycznego wynosi więc ∆E bar 16πε3 16πε3 = 2 ≅ 2 2 2 3ρ (∆µ ) 3ρ (k BT ) σ 2 Stany metastabilne - szybkość nukleacji homogenicznej Proces w którym następuje utworzenie zarodka nowej fazy bez udziału innych faz nazywamy nukleacją homogeniczną. Jego szybkość wyznaczamy przez obliczenie prędkości przekraczania rozmiaru krytycznego. Szybkość nukleacji jest równa częstości zachodzenia przejść pojedynczych cząstek ν, liczby miejsc na których zachodzi przejście Ns i prawdopodobieństwa osiągnięcia stanu o energii bariery nukleacyjnej: ∆E crit r = νN s exp − RT Oznaczmy gęstość cząsteczek na powierzchni kryształu przez s. Wówczas szybkość tworzenia krytycznych zarodków fazy ciekłej jest równa 16πε 2s 16πε 3 − r=ν 2 exp 2 2 2 ρ (∆µ ) 3ρ RT (∆µ ) Dla małych przesyceń szybkości tworzenia są ekstremalnie małe – czas tworzenia pojedynczego zarodka jest porównywalny z czasem istnienia Wszechświata. Wzrost kryształu - szybkość nukleacji 2-d Proces wzrostu kryształu bez defektów strukturalnych zachodzi przez tworzenie nowych warstw. Ponieważ jest to proces powierzchniowy, zjawisko nazywamy nukleacją dwuwymiarową (2-d). Gęstość energii powierzchni jest związana ze zmiana energii wiązania na brzegu. Oznaczmy zmianę tej energii przez φ. Wówczas – analogicznie szybkość tworzenia obszaru nowej warstwy jest równa ∆E crit r = νN L exp − RT gdzie NL – liczba węzłów sieci na brzegu obszaru 2-d nukleacja na powierzchniach - (0001) and (10-10) GaN 0,030 1012 0001 hexagon square 1010 1011 1 3φ 2 3∆µ 6φ I = νxs + 6 exp − − 4 ∆µ RT ∆µ 2-d nucleation rate / νxs 0,025 0,020 0,015 0,010 0,005 0,000 0 U D 0001 1 2 3 4 supersaturation, σ 1011 1012 1010 Diagram odtwarza jakościowo: 1 2φ 2 ∆µ 4φ − 1 exp − − I = νxs 8 ∆µ RT ∆µ - anizotropię wzrostu - przyśpieszenie wzrostu w kierunku (0001) dla wysokich przesyceń xl – wysokość warstwy Dyfuzja Dyfuzją nazywamy nieuporządkowany, przypadkowy ruch atomów (cząsteczek) o następujących własnościach: • Średni kierunek przesunięcia (uśredniony po wielu przeskokach) jest równy zeru • Korelacja kierunków dwu sąsiednich skoków jest równa zeru (proces Markowa) Dyfuzją może być: • Swobodna – długości kolejnych przesunięć i ich kierunki są dowolne • Sieciowa – kolejne przeskoki zachodzą między położeniami atomów w węzłach sieci Dyfuzja sieciowa Dyfuzją sieciową nazywamy dyfuzję o następujących własnościach: • Cząsteczki są zlokalizowane w węzłach sieci • Korelacja kierunków dwu sąsiednich skoków jest równa zeru (proces Markowa) • Szybkość przeskoku do węzła końcowego dana jest wzorem: R dyf = ν * P(i → f ) τ o = ν −1 • Prawdopodobieństwo zależy od wielkości barier energetycznych i o liczby węzłów końcowych (wymiaru sieci) ∆E dyf 1 P(i → f ) = exp − C k T B Dyfuzja sieciowa - wymiar sieci Zależność od wymiaru pokażemy na przykładzie sieci kwadratowej (regularnej): • d=1 • d=2 • d=3 ∆E dyf 1 P(i → f ) = exp − C k T B • C=2 • C=4 C = 2d • C=6 d – wymiar przestrzeni Dyfuzja – średnia odległość w czasie • Wektor przesunięcia możemy wyliczyć jako różnicę współrzędnych lub jako sumę wektorów kolejnych skoków • Obliczamy kwadrat odległości n n r r r r 2 2 ∆r = [r (n ) − r (0 )] = ∑ a i ∑ a j i =1 j=1 • Okres czasu wyznacza liczbę prób kroków według wzoru n= t τo Dyfuzja – średnia odległość • Uśredniamy po wielu niezależnych cząstkach • Korzystamy z braku korelacji dla kolejnych przesunięć n ∆r 2 r n r = ∑ ai ∑ a j = i =1 j=1 n rr a ∑ ia j + j=1,i =1,i ≠ j n n r2 a ∑ i = r2 2 a = na P(i → f ) ∑ i i =1 i =1 • Korzystamy z prawdopodobieństwa kroku: ∆r 2 ∆E ta 2 ∆E na 2 = exp − = exp − C k T 2 d τ k T o B B ∆r 2 = 2Dt ∆E a2 D= exp − 4dτo k BT Dyfuzja – średnia odległość – uśrednienie po liczbie cząstek 120000 ∆r 2 = 2Dt 100000 n=100 60000 n=10 r 2 80000 n=1000 40000 20000 n=1 0 0 20000 40000 60000 80000 100000 t • Zależność liniowa jest widoczna tylko dla dużej liczby cząstek Model kinetyczny - agregacja kontrolowana przez dyfuzję - DLA (Diffusion Limited Aggregation) Proces zdefiniowany następująco • cząsteczka zaczyna wzrost w dużej odległości od rosnącego grona • kierunek ruchu jest wybierany przypadkowo • w przypadku kontaktu z gronem cząsteczka jest przyłączana w sposób nieodwracalny do grona nazywany jest procesem agregacji kontrolowanej przez dyfuzję (DLA - Diffusion Limited Aggregation) Witten i Sander- DLA wzrost obiektów fraktalnych T. A. Witten Jr. & L.M. Sander Phys. Rev. Lett. 47 (1981) 1400 Funkcja korelacji: 1 C( r ) = ∑ ρ( r ')ρ( r + r ') N r' Wyniki symulacji C( r ) ~ r −0.343± 0.004 C(r ) ~ r 2− D D ~ 1.657 D = 1.695 ± 0.002 D – wymiar fraktalny klastra (wymiar Hausdorffa-Besicovitcha) Graniczny przypadek modelu dynamicznego : model kinetyczny: wzrost dla wysokiej częstości uderzeń r = ν * σ = ν * σ * P(i → f ) ≅ ∆E ν * σ * exp − 4 k BT Dyfuzja swobodna w gazie Dyfuzją swobodną nazywamy nieuporządkowany, przypadkowy ruch atomów (cząsteczek) o następujących własnościach: • Średni kierunek przesunięcia (uśredniony po wielu przeskokach) jest równy zeru • Korelacja kierunków dwu sąsiednich skoków jest równa zeru • Długości kolejnych przesunięć spełniają warunek 1 λ= 2nσ • Średni czas pomiędzy zderzeniami τ= λ v 3k BT v = m Układy o lokalnej równowadze - gaz • Układy w których następuje zmiana własności mała na odległościach porównywalnych ze średnią drogą swobodną • Można wprowadzić lokalne wartości parametrów termodynamicznych po uśrednieniu po obszarach dużych w porównaniu ze średnią drogą swobodną • Parametry termodynamiczne zmieniają się w sposób ciągły • Pochodne przestrzenne tych parametrów również są ciągłe Układy o lokalnej równowadze – pola klasyczne T(x) n(x) p(x) r v (x ) • Parametry termodynamiczne i ich pochodne przestrzenne opisują stan układy niezbędny dla rozważenia transportu wielkości zachowanych: masy energii i pędu oraz stan naprężeń w ośrodkach sprężystych.