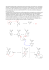Egzamin z zastosowań spektrometrii mas w chemii organicznej
Transkrypt
Egzamin z zastosowań spektrometrii mas w chemii organicznej
Egzamin z zastosowań spektrometrii mas w chemii organicznej 14-02-2004 Rozwiązania zadań i komentarze Zadanie 1. Za każde poprawne przypisanie struktury do widma przyznawano 2 pkt., a za co najmniej 3 poprawne schematy fragmentacji, w tym dwa istotne z punktu widzenia przypisania widma – 3 pkt. Łącznie: 20 pkt. Rozwiązanie Widmo A – związek 2 C4H9 α • + O + rH H - C2H4 α • m/z 116 CH3 H m/z 31 i m/z 59 - CH2=O +• O + O m/z 29 + O + + C2H5 m/z 101 (nie ma w widmie) • i +• O + m/z 71 + C2H5O mniej prawdopodobne, ale niewykluczone i + C2H5 m/z 116 + C5H11O • m/z 29 +· H O rH - C2H5OH α • + • CH3 + C4H7 m/z 55 m/z 70 m/z 116 (możliwe są też reakcje oderwania atomu wodoru z innych pozycji cząsteczki - za poprawne były uznawane wszystkie warianty) Kluczowy dla interpretacji jest jon o m/z 59, który nie pojawia się w pozostałych widmach. Podany wyżej schemat jest ‘wariantem maksymalnym’, ale aby uzyskać maksymalną liczbę punktów wystarczyło napisać reakcje powstawania jonów o m/z 59, 70 i dowolnego innego jonu. 1 Widmo B – związek 4 C3H7 • H + O + + O rH - C2H4 H m/z 31 i α + - CH2=O m/z 73 m/z 43 +• O α m/z 116 + O rH H • + O + CH3 - C4H8 H m/z 45 i m/z 101 - CH3CHO + • i +• O m/z 57 + mniej prawdopodobne, ale możliwe i + m/z 116 m/z 57 + C3H7O + C4H9O • m/z 43 +· H O m/z 116 rH - C3H7OH • + m/z 56 (możliwe są też reakcje oderwania atomu wodoru z innych pozycji cząsteczki - za poprawne były uznawane wszystkie warianty) Dla tego związku istotne jest oderwanie rodnika CH3 - jest to jedyny izomer, w którym ten rodnik może oderwać się od II-rzędowego atomu węgla, czego wynikiem jest powstawanie jonu o m/z 101 i znaczącej intensywności. Ważny jest też jon o m/z 73. Te dwa jony + dowolny inny dawały maksymalną liczbę punktów. 2 Widmo C – związek 1 α +• O • C5H11 + O + m/z 45 m/z 116 i +• O + m/z 71 • teoretycznie możliwe, ale tu nie obserwuje się i + CH3 m/z 116 + CH3O + C6H13O • m/z 15 H +· O α • - CH3 • rH + - CH3OH i - C2H4 m/z 116 m/z 84 + C5H9 m/z 69 +• C4H8 m/z 56 (możliwe są też reakcje oderwania atomu wodoru z innych pozycji cząsteczki - za poprawne były uznawane wszystkie warianty, chociaż tylko ten wyjaśnia powstawanie obu jonów wtórnych: m/z 69 i 56) Kluczowy jest jon o m/z 45 oraz jony powstające w wyniku przegrupowania. Tu również wystarczały schematy fragmentacji wyjaśniające powstawanie trzech jonów, w tym obowiązkowo m/z 45. 3 Widmo D – związek 3 C3H7 α +• O • + O + i - CH2=O m/z 73 α • m/z 116 C2H5 + O + m/z 87 + m/z 43 i - CH2=O + m/z 57 • i m/z 57 + + C3H7O +• O mniej prawdopodobne, ale niewykluczone i m/z 116 + + C4H9O • m/z 43 Obowiązkowe były fragmentacje prowadzące do jonów o m/z 87 i 73. Maksymalną ocenę dawała ponadto dowolna inna fragmentacja. Komentarz Zadanie 1 było najlepiej rozwiązywanym zadaniem (średnia 15,3 pkt na 20, czyli 76,5%). Zdecydowana większość zdających poprawnie przypisała wzory do widm, ale tylko nieliczni nie popełnili jednego z wielu możliwych błędów w schematach fragmentacji. Pierwotne rozpady α i i były zapisywane prawidłowo, ale mało kto poprawnie podał dalsze fragmentacje jonów powstających w tych reakcjach. Na ogół pomijane były też reakcje przegrupowania. Tak więc dobre oceny wynikały raczej z łagodnych kryteriów, niż jakości rozwiązań. Osoby, które będą pisać egzamin poprawkowy, powinny zwrócić uwagę na staranny zapis wzorów powstających jonów. Nagminne błędy, to pomijanie ładunku i/lub symbolu rodnika, a także częste pomijanie wiązań podwójnych lub atomów wodoru tam, gdzie musiały być narysowane dla jednoznaczności wzoru. 4 Zadanie 2 Za podanie poprawnych wzorów związków, dla których zarejestrowano widma A i B przyznawano po 5 pkt. Za podanie schematów fragmentacji prowadzących do zaznaczonych jonów można było uzyskać 5 x 2 = 10 pkt. Pozostałe 4 punkty przyznawano za poprawne uzasadnienie wyboru tych, a nie innych związków. W tekście zadania znalazł się niestety błąd: par izomerycznych związków spełniających podane warunki było 7, a nie 5, jak podano. Informacja ta nie powinna mieć jednak wpływu na rozwiązanie. Rozwiązanie 1. Pierwszy krok, to narysowanie wzorów możliwych związków (pokazano tylko izomery orto): COOCH3 COOH OCH3 OH 1 2 COOH COOH CH2OH 3 4 OCHO OH OH OH OH OCHO OCOCH3 6 5 7 Inne wzory należy odrzucić, ponieważ albo nie spełniają podanych warunków, albo odpowiadają związkom zbyt nietrwałym, aby istnieć, np. związek z ugrupowaniem -O-CO-OH. 2. Rzut oka na widma pokazuje, że w przypadku pierwszego z nich pierwszy jon fragmentacyjny ma masę o 45 u mniejszą od masy jonu molekularnego. Taka masa w tym przypadku może odpowiadać grupie –COOH, chociaż nie można też wykluczyć ugrupowania –OCHO ze związków 6 i 7. Informacja ta wyklucza więc związki 1 i 5, a także 7, ponieważ nie jest możliwe oderwanie grupy -OCHO (ani żadnej innej grupy OR) od pierścienia aromatycznego. Bardzo istotny dla poprawnego rozwiązania jest kolejny krok. Jeśli szukanym związkiem jest kwas karboksylowy, to w przypadku kwasów benzoesowych (2 i 3) należy oczekiwać przede wszystkim eliminacji rodnika OH z utworzeniem trwałego kationu benzoilowego o m/z 135: +· O OH + O - OH · R R m/z 152 m/z 135 Wskazują na to przykładowe widma znajdujące się w materiałach do wykładów. Nieobecność jonów o m/z 135 w obu widmach wskazuje więc, że struktury 2 i 3 należy wyeliminować. Pozostaje więc struktura 4, w przypadku której oderwanie grupy –COOH prowadzi do powstania bardzo trwałego kationu benzylowego (patrz schemat niżej). Teoretycznie można też sobie wyobrazić oderwanie grupy –OCHO z pozycji benzylowej związku 6, tak więc trzeba dokonać wyboru pomiędzy strukturami 4 i 6. 5 Teraz pora na przypisanie widm izomerom orto i para. W przypadku izomeru orto można spodziewać się efektu orto i tak rzeczywiście jest, na co wskazuje dużo bogatsza fragmentacja obserwowana na widmie B. Ponadto masa pierwszego fragmentu – 134 u – wskazuje na eliminację wody, czyli proces typowy dla efektu orto. Analiza wzorów 4 i 6 wskazuje jednoznacznie, że w przypadku związku 6 efekt orto polegający na oderwaniu cząsteczki wody nie jest możliwy, ponieważ nie można oderwać grupy OH od pierścienia aromatycznego (patrz np. fragmentacja fenoli), a ponadto brak jest atomu wodoru, który mógłby się przemieścić. Tak więc badana para związków to izomery para (widmo A) i orto (widmo B) kwasu hydroksyfenylooctowego. Powyżej opisano pełny tok rozumowania, ale można go też przeprowadzić „na skróty”, rozpoczynając np. od wyeliminowania struktur, które nie mogą dać efektu orto polegającego na oderwaniu cząsteczki H2O. 3. Schematy fragmentacji Widmo A, izomer para: +· COOH + CH2 - COOH · OH m/z 152 lub + albo jeszcze inne struktury HO OH m/z 107 Dalsze fragmentacje są złożone i nie było wymagane ich podanie. Widmo B, izomer orto: + O COOH OH m/z 152 CH2 O +· - CO m/z 106 O CH2 O - CO m/z 134 - COOH · + - H2O +· CH2 O· m/z 78 +· +· alternatywne struktury OH m/z 134 m/z 78 m/z 107 Produkt eliminacji wody traci następnie kolejno cząsteczki CO. Struktury tworzących się jonów można zapisać w różny sposób. Dopuszczalne było podanie tylko wzorów sumarycznych dla jonów o m/z 106 i 78. Przegrupowanie atomu wodoru odpowiedzialne za efekt orto przebiega tu 6 poprzez 7-członowy stan przejściowy. Jest to, wbrew temu co pisali niektórzy ze zdających, jak najbardziej dopuszczalne. Na odpowiednim przezroczu do wykładów 11/12 znajduje się informacja, że przegrupowanie wodoru do miejsca nasyconego może przebiegać poprzez cykliczny stan przejściowy o dowolnym rozmiarze pierścienia. Komentarz Wyniki zadania 2 były zdecydowania najgorsze (średnia ocena 8,4 pkt. na 24, czyli 35%), czyli było ono najtrudniejsze i takie miało być w założeniu. Nie mniej jednak wyniki były znacznie poniżej oczekiwań. Tylko 9 osób rozwiązało to zadanie poprawnie lub prawie poprawnie. Najczęstszym błędem był wybór związku 2, rzadziej 3. W obu przypadkach rozwiązujący nie zwrócili uwagi na brak jonu [M – OH]+, m/z 135, w widmie zwłaszcza izomeru para. W przypadku związku 2 pisano ‘na siłę’ mechanizm efektu orto, w którym atom wodoru pochodził z grupy –OCH3, co nie jest możliwe. 7 Zadanie 3 W tym zadaniu przyznawano po 4 pkt. za każdy wzór jonu z poprawnym ładunkiem, czyli łącznie 24 pkt. Można było też dostać po jednym punkcie za każdy poprawnie obliczony ładunek jonu. Rozwiązanie Rozwiązywanie zadania należało rozpocząć od obliczenia ładunków wszystkich zaznaczonych jonów. Ponieważ widmo pochodziło ze spektrometru o wysokiej zdolności rozdzielczej, widoczne były wszystkie jony izotopowe nawet dla jonów o wysokich ładunkach. Dzięki temu wystarczyło obliczyć odwrotności różnic masy pomiędzy sąsiadującymi pikami w profilu izotopowym, np. 1/(188,84 – 188,59) = 4. Kolejny krok, to przyjrzenie się profilom izotopowym i porównanie ich z profilami dla Cu i Cu2. Wpływ izotopów pozostałych pierwiastków można w pierwszym przybliżeniu pominąć, tym bardziej, że pierwiastki wchodzące w skład anionu PF6- są, bardzo szczęśliwie, monoizotopowe. Wniosek jest jednoznaczny: wszystkie jony kompleksowe zawierają po dwa jony miedzi, na co zresztą wskazuje też wyraźnie struktura ligandu. W każdym jonie kompleksowym należy więc oczekiwać fragmentu LCu2, któremu odpowiada masa nominalna 754 (dokładna: 754,30, ale nie było to konieczne). Teraz trzeba obliczyć masy kolejnych jonów mnożąc masę najlżejszego jonu izotopowego przez ładunek i porównać je z podaną wyżej masą LCu2. Trzeba też mieć obliczoną masę anionu PF6-: 145 (dokładnie: 144,96). Oto wyniki: 1. Ładunek 4+: 188,59 * 4 = 754,36 Jest to masa układu LCu2, a ponadto zgadza się ładunek: 2+ ligand jest obojętny, a dwa jony Cu dają łącznie ładunek 4+. Wniosek: [L + 2Cu2+]4+ 2. Ładunek 3+: 215,13 * 3 = 753,39 Jest masa o jednostkę mniejsza od masy LCu2, a ponadto o jednostkę jest też mniejszy ładunek, co świadczy o oderwaniu protonu. Wniosek: [L + 2Cu2+ - H+]3+. 3. Ładunek 3+: 299,79 * 3 = 899,37 Różnica między tą masą a masą LCu2 wynosi 145 jednostek, co odpowiada jonowi PF6-. Zgadza się też ładunek. Wniosek: [L + 2Cu2+ + PF6-]3+. 4. Ładunek 2+: 449,18 * 2 = 898,36 Jest to masa o jednostkę mniejsza niż w p. 3, a mniejszy o jednostkę ładunek sugeruje oderwanie protonu. Wniosek: [L + 2Cu2+ + PF6- - H+]2+. 5. Ładunek 2+: 522,17 * 2 = 1044,34 Różnica między tą masą a masą LCu2 wynosi 290 jednostek, co odpowiada dwom jonom PF6-. Zgadza się też ładunek. Wniosek: [L + 2Cu2+ + 2PF6-]2+. 6. Ładunek 1+: 1189,32 Różnica między tą masą a masą LCu2 wynosi 435 jednostek, co odpowiada trzem jonom PF6-. Zgadza się też ładunek. Wniosek: [L + 2Cu2+ + 3PF6-]+. 8 Komentarz W założeniu miało to być najłatwiejsze zadanie, którego celem było dostarczenie punktów niezbędnych do zdania egzaminu. Niestety, rzeczywistość okazała się całkiem inna: średnia ocena 10,6 pkt., czyli 44%. Jest to jednak średnia, ponieważ w praktyce zadanie miało charakter ‘zero-jedynkowy’. W pełni poprawnie rozwiązało go 9 osób, kilka popełniło pewne błędy, a dalszych kilka obliczyło tylko ładunki jonów. Zupełnym zaskoczeniem był całkowity brak chociażby próby rozwiązania u 11 osób! Jest to tym dziwniejsze, że problem obliczenia masy jonu wielokrotnie naładowanego na podstawie profilu izotopowego pojawiał się kilkakrotnie zarówno na wykładzie, jak i na egzaminach w poprzednich latach. Omawiany był też przykład widma kompleksu w ESI, zawierającego jony o różnych składach. Problem poruszony w tym zadaniu jest bardzo ważny z praktycznego punktu widzenia. Umiejętność obliczenia ładunku jonu, a następnie jego prawdziwej masy jest niezbędna przy interpretacji widm ESI, a z nimi, prędzej czy później, każdy chemik – organik spotka się w swojej pracy. Wiele osób pracuje też ze związkami kompleksowymi i dla nich konieczność rozwiązywania problemów, takich jak pokazany w zadaniu, pojawia się na co dzień. Widmo prezentowane w zadaniu jest rzeczywistym widmem zarejestrowanym kilka lat temu dla związku otrzymanego w jednym z zespołów naszego Instytutu. Jest to więc przykład „z życia”. 9 Zadanie 4 To zadanie, w odróżnieniu od poprzednich w większym stopniu sprawdzało wiedzę, niż umiejętność jej praktycznego wykorzystania. Poniżej podano wyczerpujące odpowiedzi i, w razie potrzeby, dodatkowe komentarze. W praktyce wystarczały odpowiedzi znacznie krótsze. 1. Wzrost stopnia fragmentacji w kolejności: izobutan – metan – wodór. Kolejność ta wynika z kolejności powinowactwa do protonu izobutylenu, metanu i wodoru. Entalpia protonowania przy pomocy H3+ jest więc najwyższa, a przy pomocy C4H9+ - najniższa, tak więc jony wtórne tworzące się w reakcji z H3+ mają najwyższą energię, a w reakcji z C4H9+ - najniższą, co już bezpośrednio przekłada się na stopień fragmentacji. Za samo uszeregowanie przyznawano 1 pkt, za uzasadnienie – kolejne 2. Ten punkt był na ogół rozwiązywany poprawnie. 2. Obliczamy masę jonu C12H20N2O4: 256 u. Skoro błąd względny pomiaru ma wynosić 5 ppm, to błąd bezwzględny wyniesie: 256 * 5 / 1 000 000 = 0,00128 u czyli 1,28 mmu. Chociaż wydaje się to niewiarygodne, to zadanie rozwiązały poprawnie 2 (słownie: dwie) osoby. Zadziwiający sposób ‘rozwiązania’ zademonstrowany przez kilka osób polegał na wykorzystaniu informacji z jednego z przezroczy z wykładu, na którym był podany przykład dopasowania wzorów do dokładnie zmierzonej masy. Ponadto znalazła się tam informacja, że w tym konkretnym przypadku 2 mmu błędu odpowiada ok. 8 ppm. Wiele osób układało więc proporcję: 2 mmu to 8 ppm, czyli x mmu to 5 ppm, co w rezultacie dawało wynik 1,25 mmu, czyli nawet bliski poprawnemu. Tak było jednak tylko dlatego, że przez zupełny przypadek masa jonu w przykładzie z wykładu wynosiła 260 u, czyli prawie tyle samo co w tym zadaniu (256 u). Następnym razem za takie ‘rozwiązanie’ będą przyznawane punkty ujemne. 3. W tym punkcie należało obliczyć liczby miejsc nienasycenia analizowanych jonów i wyciągnąć wnioski: a) b) c) d) e) f) C7H5Cl3NO: C4H12N2O4: C5H8BrIN2: C6H15O6: C3H7PO4 C11H13F2N2 N = 4,5 ⇒ jon peudomolekularny (ESI itp.) N = 0 ⇒ jon molekularny w EI N = 2 ⇒ jon molekularny w EI N = -0.5 ⇒ jon peudomolekularny (ESI itp.) N = 1 ⇒ jon molekularny w EI N = 5.5 ⇒ jon peudomolekularny (ESI itp.) Zadanie było na ogół rozwiązywane poprawnie, chociaż wielu rozwiązujących zadowalało się obliczeniem masy cząsteczkowej i wykorzystaniem reguły azotowej. Dla przykładów podanych w zadaniu było to wystarczające, ale w ogólnym przypadku nie pozwoliłoby wyeliminować wzorów, które spełniają regułę azotową, ale mają ujemne (mniejsze od –0,5) liczby miejsc nienasycenia. Dlatego też w zadaniach tego typu należy zawsze obliczać liczbę miejsc nienasycenia – jest to też szybsze niż obliczanie masy cząsteczkowej. 4. Poprawne, zwięzłe odpowiedzi to: a) zarówno większą czułością, jak i selektywnością charakteryzuje się metoda SRM (MRM). Większa selektywność wynika z faktu, że w metodzie SIM śledzi się jony o danej masie, 10 co do których jest znaczne prawdopodobieństwo, że mogą pochodzić od różnych związków, w tym tzw. tła, czyli niewielkich ilości zanieczyszczeń. W metodzie SRM rejestruje się natomiast wybrane procesy fragmentacji, które są w znacznie większym stopniu charakterystyczne tylko dla oznaczanego związku. Dzięki temu maleje też zasadniczo poziom tła (czyli tzw. szumu chemicznego), co zwiększa też czułość; b) metodę SIM można zastosować na dowolnym spektrometrze z pojedynczym analizatorem masy. SRM wymaga spektrometru tandemowego, np. potrójnego kwadrupola, ew. pułapki jonowej. Liczba poprawnych odpowiedzi na te pytania to ok. 50%. Częstym błędem było dyskutowanie wpływu czasu rejestracji jonów na czułość pomiaru, co oczywiście w tym przypadku nie ma znaczenia: w obu metodach czasy te mogą być takie same. Wiele osób też wymagało spektrometru tandemowego dla metody SIM, co świadczy o braku zrozumienia jej istoty. Przy okazji warto przypomnieć, że metody SIM nie ma sensu stosować w spektrometrach z analizatorem czasu przelotu – kto wie dlaczego? 5. Ogromną większość energii absorbuje matryca, której jest duży nadmiar w stosunku do badanego związku. Ponadto jony uwalniane z powierzchni próbki mogą w obszarze stosunkowo wysokiego ciśnienia bezpośrednio nad tą powierzchnią pozbyć się nadmiaru energii w wyniku zderzeń z cząsteczkami par matrycy. Pytanie było łatwe, o czym świadczy duża liczba poprawnych odpowiedzi. Nie ma czego komentować. 6. Dwa jednoimienne ładunki odpychają się, co powoduje zwiększenie energii jonu i w związku z tym jego łatwiejszą fragmentację. Niewielu rozwiązujących podało tę odpowiedź. Wiele osób pisało, że łatwość fragmentacji jonów podwójnie naładowanych wynika z ich wyższej energii, ale zabrakło już wyjaśnienia, skąd bierze się ta wyższa energia. 7. Tok rozumowania jest następujący: jeśli badany związek nie ma wymienialnych atomów wodoru, to zamiana CH3OH na CH3OD prowadzi do zamiany jonu M + H+ na M + D+, czyli zwiększa masę o jednostkę. Analogicznie, wzrost masy o 3 jednostki świadczy o obecności 2 wymienialnych atomów wodoru. Związek A nie ma więc wymienialnych atomów wodoru, a związek B ma ich 2. Wyniki rozwiązania tego zadania były zaskakująco złe. Bardzo wiele osób podało, że związek A ma 1 wymienialny atom wodoru, a związek B – 3. Tak byłoby rzeczywiście, gdyby pomiar wykonano techniką EI. W ESI należało wziąć poprawkę na przyłączony proton, który ulegał wymianie na deuteron. Warto przypomnieć, że odpowiedni przykład z pełną interpretacją był w materiałach wykładowych. 8. Jony pseudomolekularne wytwarzane łagodnymi metodami jonizacji, do których zaliczają się m. in. LSIMS i ESI charakteryzują się bardzo niską energią wewnętrzną, czyli wysoką trwałością. Aby skłonić je do rozpadu konieczne jest dostarczenie energii np. w wyniku zderzeń z cząsteczkami gazu kolizyjnego w technice CID. Punkt ten zyskał najwięcej poprawnych odpowiedzi. Nie ma czego komentować. 11 9. Podstawową fragmentacją jonów molekularnych 1-n-alkanoli jest utrata cząsteczki wody, prowadząca do powstania jonu molekularnego 1-n-alkenu o tej samej długości łańcucha. Dalsza fragmentacja obu tych grup związków jest więc jednakowa, a zatem i widma są bardzo podobne, tym bardziej, że w widmach alkanoli nie obserwuje się jonów molekularnych. Pomocny przy identyfikacji jest czas retencji, który jest zdecydowanie dłuższy dla alkoholi, jako związków bardziej polarnych i wyżej wrzących. Pełną odpowiedź na te pytania podało niewielu zdających, ale znacznie więcej było odpowiedzi cząstkowych. Dla ułatwienia można było zajrzeć do przykładowych widm alkenów i alkoholi, które były w materiałach treningowych. 12