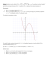MK05 Atom Wodoru
Transkrypt
MK05 Atom Wodoru
Rozdział 5 Atom Wodoru 5.1 Zastosowanie równania Schrödingera do rozwiązania zagadnienia Atomu wodoru 5.2 Rozwiązanie równania Schrödingera dla atomu wodoru 5.3 Liczby kwantowe 5.4 Efekt Zeemana 5.5 Spin 5.6 Uogólniona zasada nieokreśloności 5.7 Prawdopodobieństwa przejść. Reguły wyboru 5.8 Superpozycja stanów Werner Heisenberg (1901-1976) Atom współczesnej fizyki jest reprezentowany jedynie poprzez równanie różniczkowe cząstkowe w abstrakcyjnej przestrzeni w wielu wymiarach, z równania można wyprowadzić wszystkie jego cechy. Atom nie ma bezpośrednio żadnych materialnych cech a jego zrozumienie, w tradycyjny, oparty na zmysłach sposób, jest niemożliwe. - Werner Heisenberg Przygotowanie Marek Szopa, na podstawie Rick Trebino, Georgia Tech, www.physics.gatech.edu/frog/lectures 5.1: Zastosowanie równania Schrödingera do rozwiązania zagadnienia Atomu wodoru Z elektrostatyki wiemy, jaka jest energia potencjalna układu elektronproton : V (r ) = − e2 4πε 0 r Wykorzystamy trójwymiarowe, bezczasowe równanie Schrodingera. ∂ 2ψ ( x, y, z ) ∂ 2ψ ( x, y, z ) ∂ 2ψ ( x, y, z ) ℏ2 1 − + + = E −V (r ) 2 2 2 2 m ψ ( x, y , z ) ∂x ∂y ∂z Dla atomów wodoropodobnych, takich jak (He+ or Li++), e2 należy zastąpić przez Ze2 (Z jest liczbą atomową). We wszystkich przypadkach, dla większej dokładności, m należy zastąpić masą zredukowaną µ. Współrzędne sferyczne Potencjał siły centralnej V(r) zależy od odległości protonu od elektronu. Z powodu takiej (sferycznej) symetrii zagadnienie należy przetransformować do współrzędnych sferycznych: x = r sin θ cos ϕ y = r sin θ sin ϕ z = r cos θ r = x2 + y2 + z 2 z θ = cos r y ϕ = tan −1 x −1 ( kąt zenitalny ) ( kąt azymutalny ) Równanie Schrödingera we współrzędnych sferycznych Równanie Schrödingera przetransformowane do współrzędnych sferycznych ma następującą postać: 1 ∂ 2 ∂ψ 1 ∂ ∂ψ 1 ∂ 2ψ 2µ + 2 ( E − V )ψ = 0 r + 2 sin θ + 2 2 2 2 r ∂r ∂r r sin θ ∂θ ℏ ∂θ r sin θ ∂ϕ Rozwiązanie w rozseparowanych zmiennych Funkcja falowa ψ zależy od 3 zmiennych r, θ, φ. Jako taka może być potencjalnie bardzo skomplikowana. Bądźmy jednaj optymistami i załóżmy, że dla ψ możliwe jest rozdzielenie (separacja) zmiennych, tzn. że jest ona iloczynem trzech funkcji jednaj zmiennej: ψ (r , θ , φ ) = R(r ) f (θ ) g (φ ) Pochodne ψ ze względu na poszczególne zmienne są więc: ∂ψ ∂R = fg ∂r ∂r ∂ψ ∂f = Rg ∂θ ∂θ ∂ 2ψ ∂2g = Rf 2 ∂φ ∂φ 2 To założenie znacznie upraszcza sprawę, a co najważniejsze działa! 5.2: Rozwiązanie równania Schrödingera dla atomu wodoru Rozwiążmy więc równanie Schrodingera zakładając separowalność ψ : 1 ∂ 2 ∂ψ 1 ∂ ∂ψ 1 ∂ 2ψ 2µ + 2 ( E − V )ψ = 0 r + 2 sin θ + 2 2 2 2 r ∂r ∂r r sin θ ∂θ ℏ ∂θ r sin θ ∂ϕ ∂ψ ∂R Podstawmy: = fg ∂r ∂r ∂ψ ∂f = Rg ∂θ ∂θ ∂ 2ψ ∂2g = Rf 2 ∂φ ∂φ 2 fg ∂ 2 ∂R Rg ∂ ∂f Rf ∂2 g 2µ + 2 (E −V )Rfg = 0 r + 2 sinθ + 2 2 2 2 r ∂r ∂r r sinθ ∂θ ∂θ r sin θ ∂φ ℏ Mnożąc obie strony przez −r2 sin2θ / R f g: ∂f 1 ∂2 g sin2 θ ∂ 2 ∂R 2µ 2 2 sinθ ∂ − r − 2 r sin θ (E −V ) − sinθ = R ∂r ∂r ℏ f ∂θ ∂θ g ∂φ 2 Rozwiązanie równania Schrödingera dla atomu wodoru sin2 θ ∂ 2 ∂R 2µ 2 2 sinθ ∂ ∂f 1 ∂2 g − r − 2 r sin θ (E −V ) − sinθ = R ∂r ∂r ℏ f ∂θ ∂θ g ∂φ 2 Lewa strona równania zależy tylko od r i θ a prawa tylko od φ. Lewa strona nie może się zmienić jak zmieniamy φ . Prawa strona nie może się zmienić jak zmieniamy r lub θ. Żeby równanie było spełnione obie strony muszą więc być stałą niezależną od żadnej zmiennej. Oznaczmy tą stałą przez −mℓ2 d 2g 2 = − m ℓ g 2 dφ równanie azymutalne ℓ , choć również Jak wiemy rozwiązaniem tego równania są funkcje ℓ sin i cos je spełniają. Pamiętamy jednak, że = cos ℓ + sin ℓ Rozwiązanie równania Schrödingera dla atomu wodoru Równanie azymutalne d 2g 2 = − m ℓ g 2 dφ ℓ Jest spełnione przez dla dowolnej wartości mℓ. Jednak aby rozwiązanie miało sens musi być jednowartościową funkcją φ: g (φ ) = g (φ + 2π ) Konkretnie: Więc: g (φ = 0 ) = g (φ = 2π ) eimℓφ e 0 = e 2πimℓ Aby ten warunek był spełniony mℓ musi być liczbą całkowitą (dodatnią, ujemną lub zerem). Rozwiązanie równania Schrödingera dla atomu wodoru sin2 θ ∂ 2 ∂R 2µ 2 2 sinθ ∂ ∂f 1 ∂2 g − r − 2 r sin θ (E −V ) − sinθ = R ∂r ∂r ℏ f ∂θ ∂θ g ∂φ 2 Teraz przyrównajmy lewą stronę do −mℓ2: sin2 θ ∂ 2 ∂R 2µ 2 2 sinθ ∂ ∂f 2 θ θ − r − r sin ( E − V ) − sin 2 = −mℓ R ∂r ∂r ℏ f ∂θ ∂θ Po przekształceniu i podzieleniu przez sin2(θ) mamy: mℓ ∂ ∂f 1 ∂ 2 ∂R 2µr 2 1 r + 2 (E − V ) = 2 − sinθ ∂θ R ∂r ∂r ℏ sin θ f sinθ ∂θ 2 Teraz lewa strona zależy tylko od r, a prawa tylko od θ. Możemy zastosować jeszcze raz tą samą metodę! Rozwiązanie równania Schrödingera dla atomu wodoru 1 ∂ 2 ∂R 2µr 2 mℓ 1 ∂ ∂f ( ) r + E − V = − sin θ R ∂r ∂r ℏ2 sin2 θ f sinθ ∂θ ∂θ 2 Tym razem przyjmijmy, że obie strony są równe stałej: ℓ(ℓ + 1). 1 ∂ 2 ∂R 2 µ r + 2 2 r ∂ r ∂r ℏ ℏ 2 ℓ (ℓ + 1) E − V − R = 0 równanie radialne 2 2µ r 2 mℓ 1 d ∂f sinθ + ℓ(ℓ +1) − 2 f = 0 sinθ dθ sin θ ∂θ równanie zenitalne Tym sposobem rozseparowaliśmy równanie Schrödingera na trzy równania różniczkowe zwyczajne drugiego rzędu, jednej zmiennej. Rozwiązanie równania radialnego Równanie to nazywamy równaniem stowarzyszonym Laguerre’a a jego rozwiązania R funkcjami stowarzyszonymi Laguerre’a. Funkcji tych jest nieskończenie wiele dla n = 1, 2, 3, … Załóżmy, że stan podstawowy ma n = 1 i ℓ = 0. Poszukajmy rozwiązań. Równanie radialne jest: 1 d 2 dR 2 µ r + 2 (E −V ) R = 0 2 r dr dr ℏ Pochodna ma dwa składniki: d 2 R 2 dR 2 µ e2 R = 0 + + 2 E + 2 dr r dr ℏ 4πε 0 r Rozwiązanie równania radialnego dla −r /a Podstawmy rozwiązanie R( r ) = Ae 0 A jest stałą normalizacyjną n = 1, l = 0 a0 jest stałą o wymiarze długości. Po zróżniczkowaniu i podstawieniu do równania radialnego dostajemy. d 2 R 2 dR 2 µ e2 R = 0 + + 2 E + 2 dr r dr ℏ 4πε 0 r ⇒ 1 2µ 2µe 2 2 1 2 + 2 E+ = 0 − 2 a ℏ a0 r 0 4πε 0 ℏ Aby to równanie było spełnione dla dowolnego r, oba wyrażenia w nawiasach muszą być równe zeru. Po przyrównaniu do zera i rozwiązaniu drugiego wyrażenia względem a0: 4πε 0 ℏ 2 a0 = µe 2 Po przyrównaniu do zera i rozwiązaniu pierwszego wyrażenia względem E: ℏ2 e2 E=− =− = − E0 2 2 µ a0 8π e0 a0 Ale a0 znamy jako promień Bohra, a E jako energie stanu podstawowego atomu Bohra! Energie Atomu wodoru Bohra (dla przypomnienia) 2 e Klasyczna E = − formuła dla 8πε 0 r energii: 2 2 oraz: rn = 4πε 0 n ℏ 2 = a n 0 me 2 Tak więc energie stanów stacjonarnych są: e2 e2 En = − =− 8πε 0 rn 8πε 0 a0 n 2 lub: En = − E0/n2 gdzie E0 = 13.6 eV. 4πε 0 ℏ 2 a0 ≡ me 2 Główna liczba kwantowa n 1 ∂ 2 ∂R 2 µ r + 2 2 r ∂ r ∂r ℏ ℏ 2 ℓ (ℓ + 1) E − V − R = 0 2 2µ r Równanie radialne ma wiele rozwiązań, po jednym dla każdej dodatniej całkowitej wartości n. Skwantowana energia wyraża się wzorem znanym z prac Bohra: E0 − µ e2 1 2 = − 2 En = 2 4πε 0 ℏ n n Energia ujemna oznacza, że elektron i proton są trwale związane. 5.3: Liczby kwantowe W wyniku rozwiązanie otrzymujemy 3 liczby kwantowe: n: Główna liczba kwantowa ℓ : Liczba kwantowa pędu orbitalnego mℓ: Magnetyczna liczba kwantowa Liczby kwantowe spełniają następujące ograniczenia: n = 1, 2, 3, 4, . . . ℓ = 0, 1, 2, 3, . . . , n − 1 mℓ = − ℓ, − ℓ + 1, . . . , 0, 1, . . . , ℓ − 1, ℓ Równoważnie: n>0 ℓ<n |mℓ| ≤ ℓ Poziomy energetyczne: E0 En = − 2 n Radialne funkcje falowe atomu wodoru Kilka pierwszych funkcji radialnych Rnℓ Indeksy przy R oznaczają wartości n i ℓ. wielomiany stowarzyszone Laguerre’a Rozwiązania równań azymutalnego i zenitalnego d 2g = −mℓ g 2 dφ 2 1 ∂ 2 ∂R 2µr 2 mℓ 1 ∂ ∂f r + 2 (E −V ) = 2 − sinθ R ∂r ∂r ℏ sin θ f sinθ ∂θ ∂θ 2 Rozwiązania równania azymutalnego są postaci: e im ℓφ Rozwiązania równań azymutalnego i zenitalnego są związane ponieważ oba zawierają tą samą liczbę mℓ. Zazwyczaj grupuje się te rozwiązania w funkcje znane jako harmoniki sferyczne: Y (θ , φ ) = f (θ ) g (φ ) harmoniki sferyczne Znormalizowane harmoniki sferyczne ( , ) Rozwiązania równań azymutalnego i zenitalnego Radialna funkcja falowa R i harmonika sferyczna Y wyznaczają gęstość prawdopodobieństwa opisywanych stanów kwantowych. Pełna funkcja falowa ( , , ) zależy od n, ℓ, i mℓ. Funkcja falowa ma postać: ψ nℓm (r , θ , φ ) = Rnℓ (r ) Ynℓm (θ , φ ) ℓ ℓ Gęstość rozkładu prawdopodobieństwa Funkcje falowe mogą być wykorzystane do obliczania rozkładów prawdopodobieństwa elektronów. "Pozycja" elektronu jest rozproszona po całej przestrzeni i nie jest dobrze zdefiniowana. Radialną funkcję falową R(r) możemy wykorzystać do obliczania radialnego rozkładu prawdopodobieństwa elektronu. Prawdopodobieństwa znalezienia elektronu w różniczkowym elemencie objętości dτ jest: dP = ψ * ( r , θ , φ ) ψ ( r , θ , φ ) dx dy dz Gdzie ten element objętości we współrzędnych sferycznych jest dany wzorem: dx dy dz = r 2 sin θ dr dθ dφ Gęstość rozkładu prawdopodobieństwa Na chwilę weźmiemy pod uwagę tylko zależność radialną Po scałkowaniu po wszystkich wartościach θ i φ: π P (r ) dr = r R*(r ) R (r ) dr ∫ f (θ ) sin θ dθ 2 2 0 ∫ 2π 0 g (φ ) dφ 2 Całki po θ i φ są stałymi. Zatem radialna gęstość prawdopodobieństwa to P(r) = r2 |R(r)|2 i zależy tylko od n i ℓ. P(r ) dr = r R(r ) dr 2 2 Radialny rozkład prawdopodobieństwa R(r) i P(r) dla najniżej leżących stanów w atomie wodoru. Zauważmy, że Rn0 ma w r = 0 maksimum! Jednak czynnik r2 redukuje w tym miejscu prawd. do zera Tym niemniej jest niezerowe prawd. że elektron jest wewnątrz jądra. Funkcje rozkładu prawdopodobieństwa Gęstość prawdopodobieństwa dla trzech różnych stanów elektronowych w atomie wodoru. Liczba kwantowa ℓ orbitalnego momentu pędu. Poziomy energetyczne są zdegenerowane ze względu na ℓ (energia nie zależy od ℓ). Dla oznaczenie różnych wartości liczby ℓ używamy liter: ℓ= 0 1 2 3 4 5... litera = s p d f g h... Stany atomowe nazywamy zazwyczaj poprzez podanie dwu liczb kwantowych n i ℓ. Na przykład stan o n = 2 i ℓ = 1 nazywamy stanem 2p. Liczba kwantowa ℓ orbitalnego momentu pędu. Występuje w częściach R(r) i f(θ) funkcji falowej. Klasycznie orbitalny moment pędu jest równy = × " oraz L = m vorbital r. Kwantowomechanicznie jednak, L wiąże się z ℓ poprzez: L = ℓ(ℓ + 1)ℏ A w stanie ℓ = 0, = 0(1)ℏ = 0 Tan wynik jest niezgodny z semiklasycznym „planetarnym” modelem Bohra elektronów krążących wokół jądra L = nħ, gdzie n = 1, 2, … W mechanice kwantowej nie istnieją takie jak te orbity klasyczne. Z warunków brzegowych równania azymutalnego na g(φ) wynika, że mℓ jest liczba całkowitą związaną z z-tą składową L: Lz = mℓ ℏ Na przykład dla ℓ = 2: L = ℓ(ℓ + 1)ℏ = 6ℏ Tylko niektóre orientacje dopuszczalne są Ponadto (za wyjątkiem kiedy ℓ = 0) nie znamy Lx i Ly! Magnetyczna liczba kwantowa mℓ Szkic dowodu, że ‹L2› = ℓ(ℓ+1)ħ2 W związku, z symetrią sferyczną atomu, możemy zakładać, że wszystkie składowe momentu pędu mają takie same wartości średnie: Lx Ale, jak wiemy & = 2 = Ly 2 = Lz 2 ℓ% Średniując po wszystkich wartościach mℓ (zakładamy, że są tak samo prawdopodobne) mamy: L2 = 3 Lz 2 ℓ 2 2 = 3 ∑ mℓ ℏ (2ℓ + 1) = ℓ (ℓ + 1)ℏ 2 mℓ =− ℓ ℓ bo: ∑ n = −ℓ m 2 = ℓ(ℓ + 1)(2ℓ + 1) / 3 5.4: Efekt Zeemana Holender, Pieter Zeeman w 1896 zaobserwował, że linie spektralne emitowane przez atomy w polu magnetycznym rozszczepiają się na szereg poziomów. Nukleon Gdyby elektron traktować jako ładunek krążący wokół jądra to wytwarza on prąd ' = ()/(+. Jeśli okres tego ruchu jest dany przez , = 2. //, to: 1 2 1 ' = − = − 345 = − 6 7 8 Pętla z prądem ma moment magnetyczny : − / µ = IA = . 2. 2 − = 2 / e µ=− L 2m gdzie L = mvr jest wielkością orbitalnego momentu pędu µ=− Efekt Zeemana e L 2m Energia potencjalna pola magnetycznego jest równa: VB = − µ ⋅ B Jeśli pole magnetyczne ma tylko składową z, to i moment magnetyczny µ ma tylko składową z : e e µz = − Lz = − (mℓ ℏ) = − µ B mℓ 2m 2m gdzie 9: = 1ħ inazywa się magnetonem Bohra Efekt Zeemana Widzimy, że pole magnetyczne rozszczepia poziomy mℓ. Energia potencjalna jest skwantowana i również zależy od magnetycznej liczby kwantowej mℓ. Aby rozwiązać równanie Schrödingera z polem magnetycznym trzeba wprowadzić nowy człon do energii: VB = − µ z B = − µ B mℓ B µ z = − µ B mℓ Po przyłożeniu pola magnetycznego, poziom 2p atomu wodoru ulega rozszczepieniu na trzy poziomy o różnej energii oddalone od siebie o ∆E = µBB ∆mℓ. mℓ Energia 1 E0 + µBB 0 E0 −1 E0 − µBB Efekt Zeemana Energia Poziomy przejścia z 2p do 1s, również ulegają rozszczepieniu przez pole magnetyczne Eksperyment Sterna Gerlacha Wiązka atomów w stanie ℓ = 1 przechodzi przez niejednorodne pole magnetyczne skierowane w kierunku osi z. ekran atomy p VB = − µ z B źródło atomów Fz = −(dVB / dz ) = µ z (dB / dz ) = − µ B mℓ ( dB / dz ) Stan o mℓ = +1 będzie odchylany w dół, stan mℓ = −1 w górę, a stan mℓ = 0 nie będzie odchylany. 5.5: Spin S W 1925, holenderscy doktoranci Samuel Goudsmit i George Uhlenbeck, zapostulowali, że elektrony muszą mieć wewnętrzny moment pędu a, co za tym idzie i moment magnetyczny. Nie byłoby z tym problemu gdyby nie obliczenia Paula Ehrenfesta, który pokazał, że powierzchnia takiego elektronu musiałaby wirować z prędkością nadświetlną! Aby wyjaśnić obserwacje eksperymentalne, Goudsmit i Uhlenbeck zaproponowali że elektrony muszą mieć wewnętrzną spinową liczbę kwantową s = ½. Spin Elektron obdarzony spinem reaguje na pole magnetyczne podobnie jak elektron orbitalny. S Magnetyczna spinowa liczba kwantowa ms może przyjmować tylko dwie wartości, ms = ±½. Podobnie jak dla & , również Sz = ms ħ. Spin elektronu jest albo „do góry” (ms = +½) albo „w dół” (ms = −½) lecz nigdy jego cały moment magnetyczny µS nie jest skierowany wzdłuż osi z, gdyż S = s ( s + 1) ℏ = 3 / 4 ℏ Notacja bra-ket dla atomu wodoru Za pomocą notacji bra-ket możemy łatwo i skrótowo zapisać dany stan atomu wodoru. Jako, że liczby n, ℓ, mℓ, i ms całkowicie determinują stan kwantowy, możemy zapisać stan atomu jako: ψ nℓm m = n ℓ mℓ ms ℓ s Nie ma potrzeby zapisywania wielkości spinu s, gdyż ona zawsze jest dla elektronów równa ½. Szczególna postać funkcji falowej określona przy pomocy funkcji w wielu przypadkach nie jest istotna i można ją pominąć. W notacji bra-ket możemy również zapisać funkcję zespolenie sprzężoną: ψ n*ℓm m = n ℓ mℓ ms ℓ s Ile wynoszą Sx i Sy? Mechanika kwantowa mówi, że niezależnie jak byśmy się starali to nie możemy ich jednoczesnie zmierzyć! S Jeśli by się to nam udało, uzyskalibyśmy ±½ ħ, tak jak dla Sz. Ale wtedy ten pomiar zaburzyłby pomiar Sz, która to wielkość pozostałaby nieznana! Całkowity spin jest S = s ( s + 1) ℏ = 3 / 4 ℏ = ( 12 ) 2 + ( 12 ) 2 + ( 12 ) 2 ℏ , więc byłoby kuszące stwierdzenie, że każda współrzędna elektronu jest albo „do góry” (+½ ħ) albo „w dół” (ms = −½ ħ). Ale tak nie jest! Te składowe są niemożliwe do wyznaczenia. Jak dalej zobaczymy, nieokreśloność każdej z tych pozostałych składowych jest równa ich maksymalnej możliwej amplitudzie (½ ħ)! 5.6: Uogólniona zasada nieokreśloności Zdefiniujmy komutator dwu operatorów A i B: [ A, B ] ≡ AB − BA Jeśli <, : = 0 to mówimy, że < i : komutują z sobą. Uogólniona zasada nieokreśloności pomiędzy obserwablami < i : ma postać: ∆A ∆B ≥ 1 2 ∫ Ψ * [ A, B ] Ψ Gdzie ∆< i ∆: są nieokreślonościami tych obserwabli. Jeśli < i : komutują z sobą, to odpowiadające im wielkości fizyczne można mierzyć jednocześnie. W przeciwnym wypadku nie można. ∂ ∂ Przykład: p, xɵ Ψ ≡ pxɵ − xɵ p Ψ = −iℏ ( xΨ ) − x −iℏ Ψ ∂x ∂x ∂x ∂Ψ ∂Ψ x i = −iℏ Ψ − iℏx − − ℏ = −i ℏΨ ∂x ∂x ∂x Zasada nieokreśloności p, xɵ = −iℏ czyli: więc: ∆ p ∆ x ≥ ℏ / 2 Heisenberga ( ) Nieokreśloność momentu pędu i spinu Jak już widzieliśmy, całkowity moment pędu, jego >-ta składowa i spin mogą być mierzone jednocześnie. Z kolei ?-owa i @-owa składowe nie mogą. Oto dlaczego. Okazuje się, że: Lx , Ly = iℏLz ∆A ∆B ≥ Korzystając z: S x , S y = iℏS z i 1 2 ∫ Ψ * [ A, B ] Ψ Widzimy, że: ∆Lx ∆Ly ≥ 1 2 ∫ Ψ *iℏLz Ψ = 1 2 ∫ Ψ *iℏ(mL ℏ)Ψ = mL ℏ 2 2 A zatem uzyskaliśmy zasadę nieokreśloności pomiędzy ?-ową i @ową składową momentu pędu (o ile ≠ 0). Taka sama zasada obowiązuje dla pozostałych par składowych oraz dla spinu. Dwa rodzaje nieokreśloności w mechanice kwantowej 1. Niektóre wielkości, mogą być zmierzone z dowolną precyzją ale ich pomiar zaburza pomiar innych, np. B i +, " i ?, Lx i Ly,, Sx i Sy. Jeśli zmierzymy precyzyjnie jedną wielkość to zasada nieokreśloności nie pozwoli nam zmierzyć dokładnie drugiej, która z nią nie komutuje. Na przykład, energię można zmierzyć jedynie z dokładnością ħ /2∆t, gdzie ∆t jest czasem naszego pomiaru, bo CBC+ ≥ %⁄ . 2. Jest jeszcze jeden rodzaj nieokreśloności związany z nierozróżnialnością obiektów kwantowych o tych samych zestawach liczb kwantowych. Według tej zasady, jeśli dwa obiekty są w dokładnie tym samym stanie kwantowym – mają identyczne zestawy liczb kwantowych, np.: |GH IH ℓH JH 〉 = |G I ℓ J 〉 to ich rozróżnienie jest niemożliwe. Wszystkie atomy w stanie podstawowym są nierozróżnialne. 5.7: Prawdopodobieństwa przejść. Reguły wyboru Poziomy energetyczne (bez pola magnetycznego) zależą od głównej liczby kwantowej n. Elektrony mogą przechodzić z dowolnego stanu n na dowolny inny. Jakie znaczenie mają tu pozostałe liczby kwantowe ℓ i mℓ ? Aby obliczyć prawdopodobieństwa przejścia elektronu z jednego stanu do innego można wykorzystać funkcję falowe Reguły wyboru Prawdopodobieństwo jest proporcjonalne do średniego momentu dipolowego ∫ d = Ψ er Ψ p * k gdzie Ψp oraz Ψk są początkowym i końcowym stanem elektronu Dopuszczalne przejścia: Electrony absorbując lub emitując fotony mogą zmieniać swój stan tak aby ∆ℓ = ±1 oraz ∆mℓ = 0, ±1. Przejścia zabronione: Inne przejścia są możliwe lecz dużo mniej prawdopodobne ∆G = dowolne ∆I = ±1 ∆ Q = 0, ±1 5.8: Superpozycja stanów Energia Atom może być w stanie stacjonarnym ale może też być w stanie zwanym superpozycją (sumą) stanów stacjonarnych. Będąc w stanie superpozycji atom porusza się… E2 stan wzbudzony ∆E = hν E1 stan podstawowy Ψ (r , t ) = a1ψ 1 (r ) exp(−iE1t / ℏ) + a2ψ 2 (r ) exp(−iE2t / ℏ) gdzie |ai|2 jest prawdopodobieństwem, że atom znajduje się w stanie i. Ciekawe jest, że prawdopodobieństwo znalezienia atomu a takim stanie oscyluje w czasie: Ψ (r , t ) = a1ψ 1 (r ) + a2ψ 2 (r ) + 2 2 2 2 Re[a1ψ 1 (r )a2*ψ 2* (r )]cos[( E2 − E1 )t / ℏ ] Oscylacje mają częstość proporcjonalną do różnicy energii stanów stacjonarnych.