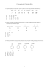Przykładowy test 2
Transkrypt
Przykładowy test 2
DRUGI PRZYKŁADOWY TEST MAGISTERSKI NA ROK AKADEMICKI 2004/2005 1. Konfiguracja elektronowa atomu fosforu w stanie podstawowym jest następująca: a) [Ar] 4s24p3 b) [Ne] 3s23p3 c) [Ne] 3s23p2 d) [Ne] 3s23p5 2. Substancja, która charakteryzuje się występowaniem międzycząsteczkowych wiązań wodorowych, to: a) CH4 b) H2 c) HF d) LiH 3. Określ barwy roztworów soli, ustawionych w kolejności: CuSO4, NiCl2, Pb(NO3)2, K2CrO4: a) żółta, bezbarwna, zielona, niebieska b) zielona, niebieska, bezbarwna, żółta c) niebieska, żółta, bezbarwna, zielona d) niebieska, zielona, bezbarwna, żółta 4. pH roztworu kwasu solnego o stężeniu 10-4 mol dm-3 po rozcieńczeniu go 105 razy będzie wynosiło: a) 4 b) 5 c) 7 d) 9 5. Wskaż parę pierwiastków charakteryzujących się największą różnicą elektroujemności: a) b) c) d) Ba, Mg Na, Cl F, Cs H, I 6. Zasadowy odczyn wykazuje roztwór: a) NH4Cl b) Na2CO3 c) CuSO4 d) AlCl3 7. Związki kompleksowe Fe2+ (o oktaedrycznej symetrii cząsteczki) z diamagnetycznymi ligandami są: a) zawsze diamagnetyczne b) zawsze paramagnetyczne c) paramagnetyczne z ligandami silnego pola, a diamagnetyczne z ligandami słabego pola d) paramagnetyczne z ligandami słabego pola, a diamagnetyczne z ligandami silnego pola 8. W potencjometrycznym oznaczaniu jonów żelaza(II) za pomocą miareczkowania roztworem manganianu(VII) potasu stosuje się wskaźnikową elektrodę: a) wodorową b) platynową c) chlorosrebrową d) szklaną 9. Typowym produktem redukcji jonów MnO4- w środowisku kwaśnym jest: a) MnO2 b) Mn2+ c) Mn3+ d) MnO42- 10. Jednostką molowego współczynnika absorpcji jest: a) dm3 cm-1 mol-1 b) cm dm-3 mol-1 c) mol-1 cm-1 d) mol-1 2 11. Największe straty oznaczanego Ba(II) obserwuje się podczas przemywania wytrąconego osadu BaSO4 za pomocą: a) 20 cm3 H2O b) 100 cm3 H2O c) 20 cm3 roztworu K2SO4 o stężeniu 0,01 mol dm-3 d) 100 cm3 roztworu NaNO3 o stężeniu 0,1 mol dm-3 12. Oznaczając zawartość wodorowęglanów w węglanach należy przeprowadzić miareczkowanie alkacymetryczne za pomocą roztworu HCl wobec następujących wskaźników: a) tylko oranżu metylowego b) tylko fenoloftaleiny c) fenoloftaleiny, a następnie oranżu metylowego d) żadnego z powyższych, ponieważ takie oznaczenie nie jest możliwe 13. W czasie miareczkowania mocnego kwasu mocną zasadą pH w punkcie równoważności: a) jest < 7 b) jest >7 c) jest = 7 d) zależy od stosunku stężeń titranta i oznaczanego kwasu 14. Biało-żółty osad z roztworem AgNO3, nierozpuszczalny w kwasie azotowym, tworzy grupa anionów: a) S2-, NO2-, CH3COOb) SO32-, CO32-, Clc) F-, SO42-, S2d) SCN-, Br-, I- 15. Równanie Ilkoviča przewiduje, że prąd graniczny w polarografii jest: a) niezależny od stężenia elektrolizowanej substancji b) jest wprost proporcjonalny do pierwiastka ze stężenia c) jest wprost proporcjonalny do logarytmu ze stężenia d) jest wprost proporcjonalny do stężenia 3 16. Zmierzono widmo 1H-NMR związku o wzorze sumarycznym C4H10O, uzyskując następujące sygnały: singlet δ=1,28 (9H), singlet δ=1,35 (1H). Związkiem tym jest: a) b) c) d) n-butanol t-butanol izobutanol sec-butanol 17. Wśród związków opisanych poniższymi wzorami wskaż te, które występują w konformacji antiperiplanarnej: H Br H H H H H Br H HO H CH3 H b) 2 i 3 H H H H OH H 4 3 2 1 a) 1 i 2 H H CH3 c) 1 i 3 d) 2 i 4 18. Trwałość przedstawionych niżej rodników wzrasta w szeregu: CH 3 CH 3 C CH C 3 4 2 CH 3 CH 3 1 a) 1,3,4,2 2 b) 1,2,3,4 c) 4,3,2,1 d) 4,3,1,2 19. W wyniku addycji bromu do podwójnego wiązania w cykloheksenie powstaje: a) b) c) d) cis-dibromocykloheksan trans-dibromocykloheksan 3-bromocykloheks-1-en 1,2,3-tribromocykloheksan 4 Br Br 20. W którym z poniższych izomerów najłatwiej przebiegnie reakcja eliminacji cząsteczki bromu (Br2) typu E2, zachodząca pod wpływem jonu jodkowego? Br Br Br a) 1 Br Br Br 1 2 b) 2 c) 3 Br Br 3 4 d) 4 21. Związek o następującym wzorze strukturalnym CH2CH2OH to: a) b) c) d) 1,2-cykloheksanodiol 1-cykloheksyloetanol 2-cykloheksyloetanol 1,2,4-cykloheksylotriol 22. Anilinę poddano następującym przemianom: NH2 (CH3CO)2O A HNO3/H2SO4 B 1mol Br2/AlBr3 Otrzymany produkt F to: a) b) c) d) o-bromonitrobenzen m-bromonitrobenzen p-bromonitrobenzen bromoanilina 5 C H2O/H+ D 1 mol HNO2 CuBr E H 3PO 2 F 23. Wśród poniższych schematów wskaż te, które przedstawiają błędne produkty reakcji podstawienia elektrofilowego: COOH NO2 NO2 Br2/FeBr3 1 COOH Br Br2/FeBr3 4 Br OH OH 1 mol Br2 2 CN CN Br2/FeBr3 5 Br Br O NH-C-CH3 O NH-C-CH3 Br Fe/Br2 3 Br Br Br2/AlBr3 6 Br a) 1,2 b) 4,6 c) 3,5 d) 2,5 24. Wskaż, które równanie reakcji jest błędne: HNO3 a) CH3 H b) OH c) H 2SO 4 Na d) a) b) c) C O CH3 CH 3M gI C CH3 CH3 d) 6 (CH3) 3COH CH3CH=CH2 (CH3)2CHONa 25. Na aldehyd fenylooctowy podziałano jodkiem metylomagnezowym, a otrzymany produkt potraktowano kwasem siarkowym. Powstały alken poddano ozonolizie. Otrzymanymi produktami są: a) b) c) d) aldehyd benzoesowy i aldehyd octowy aldehyd fenylooctowy i aldehyd mrówkowy benzen i aldehyd propionowy n-propylobenzen 26. W narysowanym poniżej wzorze związku wskaż wiązanie, które najłatwiej będzie ulegało reakcji hydrolizy. O CH2 CH CH2 CH2 O CH2O CN a) b) c) CH2 C NH2 O b) a) C c) d) d) 27. W następujących szeregach kwasów wskaż kwas najmocniejszy: A: BrCH 2COOH ClCH2COOH 1 2 COOH FCH2COOH ICH2COOH 3 4 COOH COOH COOH NO2 CH3 B: 1' a) b) c) d) 3' 2' 4, 1’ 3, 2’ 2, 4’ 1, 3’ 7 Cl 4' 28. Który z niżej wymienionych związków będzie produktem reakcji furanu z akrylonitrylem, przeprowadzonej w podwyższonej temperaturze oraz w nieobecności kwasów Lewisa i światła? a) b) CN O CH2CH2CN O c) d) O O CN a) b) c) C O CH CH2 d) 29. Aminokwasem kodowanym nie jest: a) seryna b) hydroksyprolina c) kwas glutaminowy d) tryptofan 30. Enzymy restrykcyjne uczestniczą w procesie: a) kontroli poprawności przyłączenia nukleotydu w procesie replikacji b) przyłączania aminokwasu do tRNA posiadającego charakterystyczny dla niego antykodon c) przecinania podwójnej nici DNA w wybranym miejscu d) wycinania intronów w trakcie starzenia RNA 31. Woda znajduje się w punkcie potrójnym (trzy fazy: lód, woda ciekła i para wodna w stanie równowagi ). Wzrost ciśnienia przy niezmienionej temperaturze spowoduje, że a) ilość faz nie zmieni się b) ilość faz nie zmieni się ale zmieni się ich stosunek wagowy c) zniknie faza ciekła, a pozostałe są w stanie równowagi d) pozostanie tylko faza ciekła 8 32. Stała szybkości pewnej reakcji chemicznej wynosi 0,14 dm3mol-1s-1. Wynika z tego, że jest to reakcja rzędu: a) zerowego b) pierwszego c) drugiego d) ułamkowego = 1/2 33. Potencjał chemiczny czystej substancji podczas wrzenia pod stałym ciśnieniem: a) zmniejsza się b) zwiększa się c) nie zmienia się d) najpierw zwiększy się a potem zmaleje 34 Współczynniki aktywności roztworu elektrolitu wraz ze wzrostem rozcieńczenia dążą do: a) 0; b) 1; c) 0.5; d) ∞. 35. Jeżeli przyjmie się, że swobodna entalpia reakcji w ogniwie wynosi ∆Gr = -100 kJ mol-1 oraz n (liczba ładunków elementarnych, przeniesionych w wyniku jednego stechiometrycznego przebiegu reakcji) = 1, to napięcie ogniwa w warunkach bezprądowych wynosi w przybliżeniu: a) 0.5 V; b) 0.1 V; c) -2 V; d) 1 V. 36. Współczynnik dyfuzji jonu nie zależy od a) temperatury b) gradientu stężeń c) lepkości środowiska d) promienia jonu 37. Izolowany układ składa się z dwóch pojemników zawierających dwa początkowe rozdzielone gazy doskonałe. Po usunięciu przegrody między nimi zmieni się: a) entalpia układu b) energia wewnętrzna układu c) entropia układu d) każda z funkcji termodynamicznych wymienionych w punktach a, b, c. 9 38. Standardowa molowa entalpia spalania grafitu w tlenie wynosi ∆H1o=-393,5 kJ, a spalania diamentu w tlenie ∆H2o=-395,4 kJ. Standardowa molowa entalpia przemiany diamentu w grafit wynosi zatem: a) b) c) d) 1,9 kJ -1,9 kJ -788,9 kJ zero 39. Prawdopodobieństwo znalezienia się cząstki w pewnym obszarze może wyrażać liczba: (a) 2 (b) –1 1 (c) 2 1 (d) i , gdzie i = (-1)1/2 3 40. Z punktu widzenia teorii LCAO-MO trwałym układem jest: (a) (b) (c) (d) He2 He2+ HeHF22- 41. Promieniowanie rentgenowskie jest falą elektromagnetyczną w zakresie długości: a) b) c) d) 10-2-10-4 m. 10-4-10-6 m. 10-6-10-8 m. 10-8-10-11 m. 42. Które z rodzajów oddziaływań w krysztale są najsłabsze?: a) b) c) d) wiązania wodorowe. wiązania van der Waalsa. wiązania jonowe. wiązania koordynacyjne. 10 43. Jaki jest związek między sumą mas swobodnych nukleonów a masą utworzonego z nich jądra? Wybierz poprawną odpowiedź: a) są równe - zgodnie z prawem zachowania masy b) masa jądra jest nieco większa, gdyż część energii uwalnianej podczas syntezy ulega zamianie na masę c) masa jądra jest trochę mniejsza, jeżeli jest ono trwałe, lub trochę większa, jeżeli jest nietrwałe d) masa jądra jest zawsze mniejsza niż suma mas nukleonów 44. Konwekcja ciepła jest procesem: a) b) c) d) polegającym na przekazywaniu ciepła w postaci energii promieniowania wymiany ciepła związanej z ruchem gazów lub cieczy polegającym na przekazywaniu ciepła w próżni wymagającym zastosowania katalizatora 45. Wskaż główną reakcje przebiegającą podczas konwersji metanu z parą wodną: a. b. c. d. CH4 CH4 3CH4 3CH4 + + + + H2O 2H2O H2O 2H2O = = = = 3H2 4H2 C2H2 C2H6 11 + + + + CO CO2 CO CO2 + + 6H2 5H2 ODPOWIEDZI 1. b 2. c 3. d 4. c 5. c 6. b 7. d 8. b 9. b 10. a 11. d 12. c 13. c 14. d 15. d 16. b 17. c 18. b 19. b 20. b 21. c 22. b 23. b 24. b 25. a 26. c 27. b 28. c 29. b 30. c 31. d 32. c 33. c 34. b 35. d 36. b 37. c 38. b 39. c 40. b 41. d 42. b 43. d 44. b 45. a 12